Anti-melanogeninio gedunino, gauto iš Neemo medžio, molekuliniai mechanizmai
Mar 28, 2022
Kontaktai: Audrey Hu Whatsapp/hp: 0086 13880143964 El. paštas:audrey.hu@wecistanche.com
Hwang-Ju Jeon 1, Kyeongnam Kim 1, Chaeeun Kim 2, Myoung-Jin Kim 1, Tae-Oh Kim 3,4,5,† ir Sung-Eun Lee 1,2,*,†
Santrauka:Melanogenezė yra daugybė procesų, kurių metu susidaro melaninas – apsauginis odos pigmentas (nuo ultravioletinių spindulių) ir nulemia žmogaus odos spalvą. Cheminės medžiagos, mažinančios melanino gamybą, visada buvo paklausios kosmetikos rinkoje dėl odos priežiūros interesų, tokių kaip balinimas. Pagrindinis melanino gamybos slopinimo mechanizmas yra tirozinazės (TYR), pagrindinio melanogenezės fermento, slopinimas. Čia įvertinome tikrąjį (Ged), tipišką limonoidą, dėl jo anti-melanogenezės poveikio. Melanino gamybą in vitro stimuliavo alfa melanocitus stimuliuojantis hormonas (-MSH) pelės B16F10 melanomos ląstelėse. Ged sumažino -MSH stimuliuojamą melanino gamybą, slopindamas TYR aktyvumą ir baltymų kiekį. Šį rezultatą patvirtinome in vivo zebrafish melanogenezės modelyje. Vystantis visoms apdorotoms koncentracijoms nebuvo jokių zebrafishembryo toksiškumo ir apsigimimų požymių. Gedas sumažino susidarančių zebrafinių embrionų pigmentinių taškų skaičių ir embrionų melanino kiekį. Labai aktyvi Ged koncentracija (100 µM) buvo daug mažesnė nei teigiamos kontrolės kojinės rūgšties (8 mM). Taigi Gedas gali būti patrauklus kandidatas į anti-melanogenezės reagentus.
Raktiniai žodžiai: MITF; su mikroftalmija susijęs transkripcijos faktorius; TYR; tirozinazė; DQ; dopachinonas;TRP-1; su tirozinaze susijęs baltymas 1; TRP-2; su tirozinaze susijęs baltymas 2; MC1R; melanokortino 1 receptorius; -MSH; -melanocitus stimuliuojantis hormonas; AKTH; adrenokortikotropinis hormonas; ASP; signalizuojantis baltymas; cAMP; ciklinis adenozino monofosfatas; CREB; cAMP atsako elementas
1. Įvadas
Melaninas sintetinamas melanosomoje, į lizosomas panašiose melanocitų organelėse. Melanosomoje melaniną gamina du pigmentai – eumelaninas ir feomelaninas, atitinkamai atstovaujantys rudai juodai ir raudonai geltonai [1]. Šių melaninpigmentų sintezė prasideda nuo pirmtako L-tirozino, vykstant L-tirozino oksidacijos reakcijai į junginį, vadinamą dopachinonu (DQ) ir L-DOPA [2]. Šiame oksidacijos etape tirozinazė (TYR) veikia kaip viso melanino biosintezės kelio greitį ribojantis fermentas [2,3]. TRP-1ir TRP-2, glaudžiai susiję su melanogenezės baltymais, katalizuoja eumelanino biosintezės kelią ir stabilizuoja bei skatina TYR aktyvumą [1]. Melanino pigmentų gamybos procesas (vadinamas melanogeneze) vyksta melanocitų melanosomoje, formelanino sintezės ir saugojimo vietoje [4]. Melanogenezės signalizacijos kelyje melanokortino1 receptorius (MC1R) yra su G baltymu susietų receptorių narys. MCIR yra melanogenezės signalizacijos pradžios taškas ir jį aktyvuoja MC1R agonistai, tokie kaip melanocitus stimuliuojantis hormonas (-MSH), adrenokortikotropinis hormonas (AKTH) ir agouti signalinis baltymas (ASP) [1,2]. -MSH-MC1R signalizacijos kelio aktyvinimas padidina ciklinio adenozinemonofosfato (cAMP) koncentraciją ir fosforilina cAMP atsako elementą (CREB). Fosforilintas CREB sukelia su mikroftalmija susijusio transkripcijos faktoriaus (MITF), transkripcijos faktoriaus, reguliuojančio su melanino sinteze susijusius genus, TYR, su tirozinaze susijusio baltymo -1 (TRP-1) ir su tirozinaze susijusio baltymo, baltymų kiekį. -2 (TRP-2) surišant šių genų M langelį [1,5,6]. Tarp penkių melanokortino receptorių MC1R turi daugiausiai melanocitų. Jis pirmiausia reguliuoja eumelanino (juodai rudo pigmento) gamybą aktyvuodamas MC1R, kai šio receptoriaus agonistai, tokie kaip a-MSH ir ACTH, perjungiami į šį receptorių [2,4,7].
Nors yra skirtumų tarp žinduolių ir žuvų, zebrafish turi MC5R ir MC3R ekstrakopiją, kurios žuvienė neturi [7], o šis signalizacijos kelias vis dar egzistuoja zebražuvėse ir veikia lygiai taip pat, kaip žinduolių melanocituose [7]. melanino pigmento susidarymo slopinimo tyrimų skaičius išaugo dėl jo tyrimų pranašumų, tokių kaip greitas ankstyvos stadijos embrionų vystymasis ir stebėjimo paprastumas [8–11]. Dėl šių reiškinių daugelis ankstesnių tyrimų parodė, kad šio signalizacijos kelio slopinimas sumažina melanino gamybą ir randa keletą inhibitorių, įskaitant bisabololį-angeloną, 4-hidroksi-3-metoksicinamaldehidą ir difenil-metilen-hidrazino karbotiaminą [12]. –14].
Geduninas (Ged), gerai žinomas šilumos šoko baltymo 90 inhibitorius, yra limonoidas, randamas Meliaceae augalų gentyje. Šio limonoido gausu daugiausia jaunų indiško neemo medžio (Azadirachta indica) vaisių epikarpe ir pasižymi įvairiu biologiniu aktyvumu, įskaitant priešvėžinį, priešmaliarinį, priešuždegiminį, antidiabetinį, antialerginį, insekticidinį, herbicidinį ir priešgrybelinį poveikį [15–18]. Nėra pranešimų apie Ged anti-melanogeninio poveikio mechanizmą.
Kaip vaistinis preparatas ar kosmetikos priemonė, skirta gydyti su melaninu susijusias ligas ar odos spalvos pokyčius, Ged gali turėti pranašumų dėl savo saugių, natūraliai atsirandančių augalų savybių [19]. Anti-melanogeninis Ged poveikis buvo įvertintas in vitro ir in vivo naudojant B16F10 pelių melanomos ląsteles ir zebrafinių žuvų embrionus, siekiant rasti tinkamą merlangų agentą, vieną didžiausių komercinės kosmetikos rinkos dalių. Taip pat buvo atliktas testas, siekiant parodyti, kaip Ged galimai veikia gyvūnus.
2. Medžiaga ir metodai
2.1. Cheminės medžiagos ir reagentai
Ged buvo nupirktas iš Microsource Discovery Systems, Inc. (Gayloardville, CT, JAV). Melanogenezės stimuliatorius, -MSH, anti-melanogeninis junginys ir kojic rūgštis buvo įsigyti iš Sigma-Aldrich (St. Louis, MO, JAV). Visi kiti reagentai buvo aukštesni už molekulinės biologijos laipsnį.
2.2. Ląstelių kultūros
Pelės melanomos ir karcinomos ląstelių linija B16F10 buvo gauta iš American TypeCulture Collection (ATCC, Manassas, VA, JAV) ir kultivuojama su 10 procentų galvijų vaisiaus serumo (v/v), o penicilinu tiekiama Dulbecco modifikuota Erelio terpė (GE) Sveikatos priežiūra, Čikaga, IL, JAV) drėgnoje atmosferoje su 5 procentais CO2. Ląstelės buvo kultivuojamos tol, kol susiliejimas pasiekė 80 procentų ir dalijamos tris kartus per savaitę dalijimosi santykiu 1:8. Ląstelės buvo stebimos kas 12 valandų ir tikrinami morfologiniai pokyčiai. Naudotų ląstelių perėjimo skaičius buvo mažas.
2.3. Ląstelių gyvybingumo tyrimas
Norint įvertinti Ged proliferacinį poveikį B16F10 pelių melanomos ląstelių linijai, MTS tyrimas buvo atliktas pagal anksčiau pateiktą protokolą [20], naudojant CellTiter96 Aqueous One Solution Cell Proliferation Assay rinkinį (Promega, Madison, WI, JAV). Trumpai tariant, 1 × 103 ląstelės buvo pasėtos į kiekvieną 96- šulinio plokštelės šulinėlį ir inkubuojamos 24 valandas, kol atsigauna. Po inkubacijos Ged buvo apdorotas įvairiomis koncentracijomis: 0, 3,12, 6,25, 12.{14}}, 50 ir 75 µM. Po 48 valandų į kiekvieną šulinį, kuriame yra 100-µL terpės su Ged ir be Ged, buvo pridėta 20 µL MTS tyrimo tirpalo. Po papildomos inkubacijos 4 valandas, absorbcija buvo išmatuota esant 490 nm, naudojant Multiskan GO spektrofotometrą (ThermoScientific, Waltham, MA, JAV). Absorbcijos duomenys buvo normalizuoti naudojant kontrolę ir pateikti kaip procentinis slopinimo santykis.
2.4. Melanino kiekio nustatymas
Tarpląstelinis ir intracelulinis melanino kiekis buvo nustatytas naudojant modifikuotą metodą, apie kurį buvo pranešta anksčiau [21]. -MSH (200 nM) iš anksto apdorotos melanomos ląstelės buvo inkubuojamos 72 valandas su ir be kojinės rūgšties (200 µM) ir Ged (25 ir 50 µM). Po inkubacijos buvo surinkta fenolio raudonumo neturinti auginimo terpė, o kultivuotos ląstelės buvo surinktos naudojant RIPA lizės buferį. Surinktos ląstelės buvo centrifuguojamos 4 ◦ C temperatūroje, 13, 000 aps./min. 15 min., o granulės buvo ištirpintos 1 M NaOH, 10 procentų DMSO tirpale 95 ◦ C temperatūroje 2 valandas. Surinktos terpės ir ištirpusio melanino absorbcija buvo matuojama esant 470 nm, naudojant spektrofotometrą. Visi mėginiai buvo normalizuoti, jų baltymų koncentracija nustatyta BCA metodu.
2.5. Intraląstelinės tirozinazės aktyvumo tyrimas
Ląstelių tirozinazės aktyvumas buvo nustatytas matuojant L-dihidroksifenilalanino (L-DOPA) oksidacijos greitį, kaip buvo pranešta anksčiau, su nedideliais pakeitimais [22]. B16F10 pelių melanomos ląstelės buvo iš anksto apdorotos 200 nM -MSH 1 valandą, po to apdorotos 200 µM kojinės rūgšties su Ged ir be jo (25 ir 50 µM) ir inkubuojama 72 valandas. Po inkubacijos ląstelės buvo surenkamos lizės buferiu, turinčiu proteinazės inhibitorių, ir mėginys centrifuguojamas 13,000 × g, 4 ◦C 15 min. Supernatantas buvo perkeltas į naują mėgintuvėlį. Kiekvienas mėginys (20 µL) ir 80 µL 40 mM L-DOPA buvo sumaišyti 96-šulinėlių plokštelėje ir 2 valandas inkubuojami 37 ◦ C temperatūroje. Oksiduoto L-DOPA absorbcija prie 475 nm buvo nustatyta naudojant mikroplokštelių skaitytuvą. Absorbcijos vertė buvo normalizuota pagal kiekvieno mėginio baltymų koncentraciją.

Cistanche ekstrakto nauda: slopina tirozinazės ekspresiją.
2.6. RNR išskyrimas ir qRT-PGR
Bendra RNR išskyrimas ir qRT-PCR buvo atlikti pagal anksčiau aprašytą metodą [18]. Bendra RNR buvo trumpai išgauta iš kiekvieno mėginio naudojant Trizol reagentą (Ambion, Austin, TX, JAV). Išskirta bendra RNR koncentracija buvo nustatyta pagal absorbciją esant 260 nm, o visos RNR kokybė buvo patikrinta naudojant 260:280 ir 260:230 nm absorbcijos santykį, naudojant Multiskan GO mikroplokštelių skaitytuvą (Thermo Scientific). TotalRNR (5 µg) buvo susintetinta į kDNR su Maxima pirmosios krypties cDNR sintezės rinkiniu (Thermo Scientific) ir susintetinta kDNR. Mitf, Tyr, Trp-1 ir Trp-2 mRNR ekspresijos lygiai buvo nustatyti naudojant Luna Universal qPCR Master Mix (New England Biolabs, Ipswich, MA, JAV) ir QuantStudio 3 Real-Time PGR instrumentą ( Applied Biosystems, Foster City, CA, JAV) pagal instruktoriaus protokolą. Genų ekspresijos lygis buvo normalizuotas naudojant gliceraldehido 3-fosfato dehidrogenazę (GAPDH).
2.7. Imunoblotų analizė
Imunoblotinė analizė atlikta pagal anksčiau aprašytus metodus [23]. B16f10 ląstelių baltymai buvo surinkti naudojant Ceti lizės buferį (Translab, Daejeon, Korea), o koncentracija nustatyta naudojant Pierce BCA baltymų tyrimo rinkinį (Thermo Scientific). Vienodas kiekvieno mėginio baltymų kiekis (30 µg) buvo įdėtas į natrio dodecilsulfato-poliakrilamido gelį ir atliktas elektroforezė. Po atskyrimo baltymai buvo perkelti į nitroceliuliozės membraną, o membrana buvo užblokuota 10 procentų neriebaus pieno tirpale 2 valandas. Užblokuotos membranos buvo inkubuojamos su pirminiais antikūnais per naktį 4 ◦ C temperatūroje, po to dar 2 valandas inkubuojamos su antriniu antikūnu 26 ◦ C temperatūroje. Pirminiai ir antriniai antikūnai buvo atskiesti atitinkamai 1:1000 ir 1:3000. Galiausiai, blotingos membranos buvo dokumentuojamos naudojant ChemiDoc (Bio-Rad, Hercules, CA, JAV) su ECL reagentu (SuperSignal, Thermo Scientific). Pirminiai ir antriniai antikūnai buvo įsigyti iš Santa Cruz Biotechnology (Dallas, TX, JAV).
2.8. Zebrafish embriono testas
Wild-type zebrafish were thankfully obtained from Professor Tae-Lin Huh, the School of Life Science and Biotechnology, Kyungpook National University, Daegu, Republic of Korea. The strain was kept for more than eight generations in a laboratory condition of 26 ◦C ± 1 ◦C, and a day-to-night ratio of 8:16. General fish care and breeding conditions, as previously described, were followed [24]. Ten groups of zebrafish were mated to obtain embryos with a mating ratio (male: female, 1:2), and among obtained embryos, healthy embryos had >80 procentų tręšimo norma ir buvo atrinkti bei panaudoti eksperimentui. Dvylika sveikų embrionų kiekvienoje apdorotoje grupėje buvo kiekviename 96-šulinėlio plokštelės šulinyje su ir be Ged (25, 50, 75 ir 100 µM) ir kojinės rūgšties (8 mM) E3 terpėje ekrano stadijoje. Praėjus 24 valandoms po apvaisinimo (h/pf), embrionai buvo dechorionuoti, o anomalijos tikrinamos kas 24 valandas iki 72 h/pf. Embrionų fenotipas buvo nufotografuotas iš šono ir nugaros, kad būtų galima palyginti grupių skirtumus naudojant BX53 vertikalią mikroskopą su DP80CCD (Olympus Life Science Solutions, Waltham, MA, JAV). Nufotografavus, embrionai buvo homogenizuoti Ceti lizės buferiu (TransLab) ir atlikta melanino koncentracijos nustatymas, kuris buvo lygus B16F10 ląstelių melanino kiekio nustatymui.
2.9. Statistinė analizė
Visos šiame tyrime pateiktos statistinės analizės buvo atliktos naudojant GraphPad Prismv.8.{1}} (GraphPad Software, San Diego, CA, JAV). Daugkartiniam palyginimui buvo naudojama vienpusė ANOVA su Tukey testu. Visi duomenys pateikiami kaip vidurkis ± standartiniai nuokrypiai. Reikšmingi skirtumai buvo laikomi statistiškai reikšmingais, kai p <>
3. Rezultatai
3.1. Citotoksinis Piperlongumino poveikis B16F10 ląstelėse
Prieš tirdami anti-melanogeninį Ged poveikį, atlikome B16F10 ląstelių linijos gyvybingumo testą, kad nustatytų šio tyrimo dozių diapazoną. Koncentracijų diapazone nuo 3,12 iki 50 µM ląstelės neturėjo jokio slopinamojo poveikio augimui, o jų santykinis proliferacija buvo nuo 91,0 procento iki 118,7 procento (1 pav.). Priešingai, nors statistinės reikšmės nebuvo, 75 µM gydytų grupių augimas buvo šiek tiek slopinamas (89,3 proc.; 1 pav.). Todėl likusiuose ląstelių linijos eksperimentuose didžiausia koncentracija buvo nustatyta iki 50 µM.
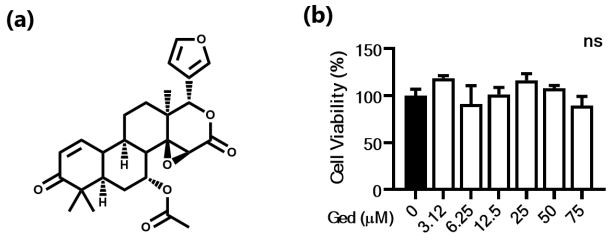
1 pav. Gedunino (Ged) citotoksiškumas B16F10 ląstelėse
3.2. Geduninas slopina melanino gamybą ir tarpląstelinį tirozinazės aktyvumą pelės B16F10 melanomos ląstelėse
Mes įvertinome anti-melanogeninį Ged poveikį B16F10 pelių melanomos ląstelėse. MC1R agonistas -MSH efektyviai sukėlė intracelulinį ir ekstraląstelinį melanino gamybą (2a–c pav.). Surinktos terpės spalva buvo tamsi su -MSH (2a pav.). Spalva išbluko pridėjus Ged, o poveikis priklausė nuo dozės (2a pav.). Dėl bendro melanino kiekio -MSH padidino melanino gamybą melanocituose maždaug septynis kartus daugiau nei kontrolinėje grupėje ir paskatino melanino sumažėjimą, pridėdamas kojinės rūgšties, gerai žinomos teigiamos melanogenezės kontrolės (2d pav.). Gedas taip pat sutrumpino dirgiklius sukeliantį melanino gamybą melanocituose visomis šio tyrimo metu ištirtomis koncentracijomis (2d pav.). Be to, tirozinazės aktyvumo teste Ged parodė stiprų slopinamąjį poveikį greitį ribojančiam fermentui tirozinazei melanogenezėje (2e pav.). Santykinis tirozinazės aktyvumas 50 µM Ged gydytoje grupėje sumažėjo atitinkamai 20 proc. ir 12,24 proc., palyginti su kontroline ir a-MSH stimuliuota grupe.

2 pav. Anti-melanogeninis tikrojo (Ged) poveikis alfa melanocitus stimuliuojančio hormono (-MSH) stimuliuojamai melanino gamybai B16F10 ląstelėse.
3.3. Geduninas sumažina su MSH sukeltą melanogenezės genų ekspresiją
-MSH (200nM) sukeltas Mitf mRNR lygis; melanogenezės transkripcijos faktorius; ir tiksliniai genai Tyr, Trp-1 ir Trp-2 (3 pav.). Gydymas Ged sumažino visų genų mRNR lygį priklausomai nuo dozės, kai koncentracija buvo 25 ir 50 µM (3 pav.). Palyginti su teigiama kontrole, kojo rūgštimi (200 µM), Ged buvo veiksmingesnis mažinant mRNR. su melanogeneze susijusių genų lygis B16F10 ląstelėse. Be to, Mitfand Tyr lygis sumažėjo atitinkamai 010- ir 026- kartų mažesnis nei -MSH sukeltos ląstelės, esant 50 µM koncentracijai (3a, b pav.). Sumažėjęs šių genų mRNR lygis sumažino Tyr lygį ir sumažino melanino TYR gamybą mažiau nei kontrolinė grupė.

3 pav. Redukcijos poveikis su melanogeneze susijusiems genams.
3.4. Gedunino sumažintas TYR ir TYR-1 suma
TYR vaidina lemiamą vaidmenį melanogenezėje, o šio fermento baltymų lygis tiesiogiai veikia melanogenezę. Imunobloto analize bandėme patvirtinti baltymo TYR kiekio pasikeitimą, kurį sukėlė sumažėjęs mRNR lygis. TYR buvo pastebimai sumažintas, palyginti su kontroline, ir -MSH buvo gydomas priklausomai nuo dozės (4a pav.). Be to, TRP-1, esminis TYR transkripcijos faktorius, buvo šiek tiek sumažintas (4a pav.). Rezultatai buvo akivaizdesni, kai kiekvieną baltymo juostą normalizavo namą išlaikantis baltymas GAPDH (4b, c pav.).
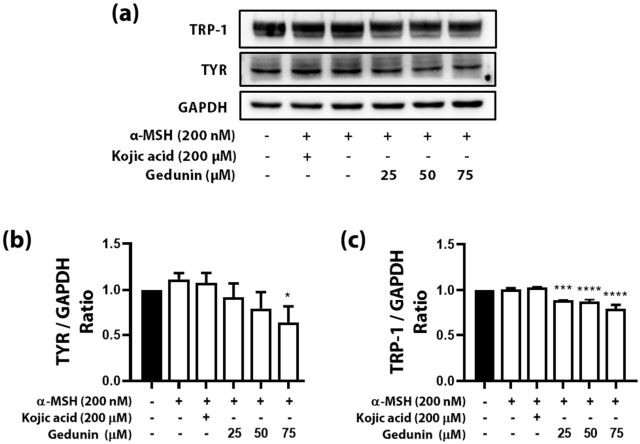
4 paveikslas. Alfa-melanocitus stimuliuojančio hormono (-MSH) sukeltų B16F10 ląstelių Western blot tyrimas naudojant originalų gydymą.
3.5. Gedunino toksiškumas zebrafish ankstyvoje vystymosi stadijoje
Prieš įvertinant anti-melanogeninį Ged testą in vivo, buvo atliktas Ged toksikologinis zebrafinių žuvų vystymosi ankstyvosios stadijos įvertinimas. Zebrafish embrionų morfologinių anomalijų nepastebėta jokioje apdorotoje Ged koncentracijoje (5a pav.). Ištirtos Ged koncentracijos, 25, 50, 75 ir 100 µM, Ged gydytų grupių išgyvenamumas reikšmingų skirtumų neturėjo 72 val. cheminiu būdu apdoroto laikotarpio (5b pav.).
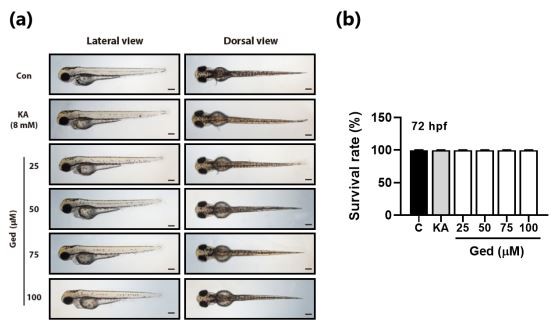
5 pav. Genuine (Ged) toksiškumas zebrafinių žuvų ankstyvoje vystymosi stadijoje.
3.6. Geduninas sumažino melanino kiekį zebrafish embrionuose
Kadangi Ged neturi toksinio poveikio zebrafinių embrionų vystymuisi, mes ištyrėme anti-melanogeninį poveikį, kai buvo keletas Ged koncentracijų, 25, 50, 75 ir 100 µM. Teorinio stebėjimo metu patikrinome pigmentinės zebrafish taškelius; zebrafinių žuvų embrionų vaizdas iš šono parodytas 5a paveiksle. Kojic rūgštis slopina zebrafinių embrionų pigmento gamybą. Ged apdorotų zebrafinių embrionų galvoje taip pat buvo mažiau pigmentinių taškų (6a pav.). Be to, bendras melanino kiekis, ekstrahuotas iš viso zebrafinių embrionų, sumažėjo po Ged poveikio 72 valandas tiek kojinės rūgšties, tiek teigiamos kontrolės, tiek Ged apdorotose grupėse (6b, c pav.)

6 pav. Genuine poveikis melanino gamybai in vivo.
4. Diskusija
Šiame tyrime buvo įvertintos Ged slopinimo savybės prieš melanino gamybą. Remiantis mūsų išvadomis, Ged slopinimo gebėjimas buvo maždaug 11{1}} kartų didesnis nei kojinės rūgšties (2 pav.), o Ged koncentracija (2 pav.) 50 µM) buvo mažesnis nei kojinės rūgšties (200 µM), teigiamos kontrolės. Jis buvo suderintas su susilpnėjusiu intracelulinės tirozinazės aktyvumu, fermentu, kuris paverčia L-Dopą į DQ, pirminį eumelanino ir feomelanino pirmtaką. Sumažėjęs Tyr aktyvumas reiškia viso melanino gamybos procesų sulėtėjimą ir abiejų galutinių produktų – eumelanino ir feomelanino – trūkumą [1–3]. Nuorašo ir TYR lygius reguliavo daugybė transkripcijos faktorių: Mitf, Trp-1 ir Trp-2 [1,2]. Sumažėjęs baltymų ir mRNR kiekis reiškia, kad suaktyvintas MC1R per -MSH – MC1R –PKA – CREB signalizacijos ašį buvo sumažintas apdorojant Ged 25 ir 50 µM koncentracijomis, priklausomai nuo dozės tiek atliekant kiekybinį PGR, tiek atliekant Western bloting. Kaip aprašyta anksčiau, sumažinus MITF kiekį atsiranda Tyr, Trp-1 ir Trp-2 trūkumas, nes sumažėja šių genų promotorių regionas [25–27]. Sumažinus šiuos transkripcijos faktorius, TYR sumažėja iki žemesnio lygio ir slopinama melanino pigmento gamyba B16F10 ląstelėse. Be to, dabartiniai rezultatai rodo TYR slopinamąjį Ged poveikį, dar vieną kritinį melanino gamybos tašką melanocituose. In vitro ir in vivo modeliuose Ged taip pat parodė pigmento produkcijos slopinimo poveikį ankstyvosios zebražuvės vystymosi stadijos metu. Mūsų rezultatai parodė, kad gydymas Ged 72 valandas žymiai sumažino zebrafinių embrionų pigmentaciją. Bendras melanino kiekis ir susijusių genų mRNR lygiai sumažėjo esant Ged, o šių rezultatų tendencija tvirtai patvirtino Ged in vitro anti-melanogenezės savybę.
Be to, Ged slopinimo gebėjimas buvo daug stipresnis nei kojinės rūgšties, vieno iš dažniausiai kosmetikos pramonėje žinomų junginių kaip balinimo reagentas [6,28]. Koncentracija, kuriai Ged veikė, buvo santykinai mažesnė nei kojinės rūgšties. Be to, ankstesnė ataskaita parodė, kad kitas įprastas balinamasis reagentas, arbutinas, turėjo panašų anti-melanogeninį poveikį kaip kojo rūgštis [2]. Todėl Ged turėtų būti laikomas balinamuoju reagentu, pakeičiančiu šiuo metu naudojamą arbutiną arba kojo rūgštį, ir kaip anti-melanomadrugą, atsižvelgiant į jo perspektyvias savybes.
Anti-melanogeninės Ged savybės buvo pasiūlytos anksčiau [29, 30], tačiau šiuose tyrimuose dėmesys nebuvo sutelktas į specifinius poveikio mechanizmus, o tiesiog stebėjo citotoksinio poveikio ir melanino gamybos kiekio pasikeitimą in vitro, o antiproliferacinį ir slopinamąjį poveikį. HSP 90 išraiška buvo paryškinta [31–33]. Buvo pranešta apie Ged kaip anti-melanogenetinio agento galimybę; tačiau šie tyrimai nebuvo orientuoti į specifinius poveikio mechanizmus, o tiesiog stebėjo citotoksinio poveikio ir melanino gamybos kiekio pokyčius in vitro. Bandėme nustatyti ląstelių lygio mechanizmą, patvirtindami su melanino gamyba susijusių genų mRNR lygį ir baltymų kiekį. Kartu su ankstesnėmis ataskaitomis šis tyrimas atskleidė naują kosmetikos ingrediento Gedo perspektyvą dėl dviejų privalumų – išskirtinio priešvėžinio ir anti-melanogenezės, kuris gali būti taikomas tiek UV sukeltai melanomai, tiek pigmento kaupimuisi, ypač tuo pačiu metu.

cistanche ekstrakto milteliai: skaidrūs laisvieji radikalai
5. Išvados
Apibendrinant, visi šie rezultatai parodė, kad naujas junginys Ged gali būti naudojamas kaip depigmentacijos reagentas melanino biosintezei, kuris sutrumpino pasroviui esančius baltymus TYR, TRP{0}} ir TRP-2 mažesniu kiekiu, palyginti su pagrindiniu. reguliavimo baltymas, MITF, tiek in vitro, tiek in vivo zebrafish modelio sistemose.
cistanche tabletės



