Nauji daug žadantys kurkumino terapiniai būdai sergant smegenų ligomis
Jun 24, 2022
Prašau susisiektioscar.xiao@wecistanche.comDaugiau informacijos
Santrauka:Kurkuminas, maistinis polifenolis, išskirtas iš Curcuma longa (ciberžolės), visame pasaulyje plačiai naudojamas kaip žolė ir prieskonis. Dėl savo biofarmakologinio poveikio kurkuminas taip pat vadinamas „gyvybės prieskoniu“, iš tikrųjų pripažįstama, kad kurkuminas turi svarbių savybių, tokių kaip antioksidantas, priešuždegiminis, antimikrobinis, antiproliferacinis, priešnavikinis, ir anti-senėjimo. Neurodegeneracinės ligos, tokios kaip Alzheimerio ligos, Parkinsono ligos ir išsėtinė sklerozė – tai grupė ligų, kurioms būdingas laipsniškas smegenų struktūros ir funkcijos praradimas dėl neuronų mirties; šiuo metu nėra veiksmingo gydymo šioms ligoms gydyti. Apsauginis kurkumino poveikis nuo kai kurių neurodegeneracinių ligų buvo įrodytas in vivo ir in vitro tyrimais.cistanche varpos dydisŠioje apžvalgoje pabrėžiamos naujausios išvados apie neuroprotekcinį kurkumino poveikį, jo biologinį prieinamumą, veikimo mechanizmą ir galimą pritaikymą neurodegeneracinių sutrikimų prevencijai ar gydymui.

Norėdami sužinoti daugiau, spustelėkite čia
Raktiniai žodžiai:kurkuminas; natūralus flavonoidas; neurouždegimas; priešuždegiminis; neurodegeneracinės ligos; Alzheimerio ligos; Parkinsono ligos; išsėtinė sklerozė; daugiaformė glioblastoma; epilepsija
1. Įvadas
Naujausi įrodymai rodo, kad maistinių medžiagų ir maisto papildų naudojimas gali apsaugoti centrinę nervų sistemą (CNS), nes apsaugo neuronus nuo streso sukeltos žalos, slopina neurouždegimą ir padidina neurokognityvinę veiklą.
Kurkuminas yra viena iš kurkuminoidinių sudedamųjų dalių, esančių ciberžolėje (Curcuma longa Limn), ir yra daugiametis Zingiberaceae šeimos augalas. Ciberžolė, dar vadinama „auksiniu prieskoniu“, naudojama kaip tradicinės medicinos priemonė, taip pat plačiai naudojama Azijos virtuvėje kaip maisto priedas ir dažiklis gėrimų pramonėje [1].
(1E,6E)-1,7-bis(4-hidroksi-3-metoksifenilas)-1, 6-heptadienas-3, 5-dionas yra IU-PAC kurkumino pavadinimas, jo cheminė formulė yra CanHzoOg, o jo molekulinė masė yra 368,38 g/mol. Įvairius kurkumino biologinius aktyvumus ir gydomąsias savybes lemia jo chemija, ypač fenolio hidroksilo grupės, centrinis bis-, -nesočiasis -diketonas, dvigubos konjuguotos jungtys ir metoksi grupės yra atsakingos už jo biofarmakologinį poveikį. Kurkuminas yra lipofilinė molekulė, blogai tirpstanti vandenyje arba hidrofiliniuose tirpaluose, vietoj to jis lengvai tirpsta organiniuose tirpikliuose, tokiuose kaip metanolis, etanolis, acetonas ir dimetilsulfoksidas, chloroformas [2].
Kurkuminoidų kompleksą sudaro kurkuminas, demetoksikurkuminas ir bis-deme toksoksikurkuminas [3].

Cistanche gali kovoti su senėjimu
Kurkuminas, kaip ir kitos fitocheminės medžiagos, pasižymi pleiotropiniu poveikiu ląstelėms, iš tikrųjų dėl gebėjimo sąveikauti su daugeliu baltymų kurkuminas gali išprovokuoti ląstelių reakciją į išorinius dirgiklius. Be to, kurkuminas aukštyn ir žemyn reguliuoja įvairias miRNR ir gali sukelti epigenetinius pokyčius ląstelėse. Keletas in vitro, in vivo ir klinikinių tyrimų buvo sutelktas į galimą terapinį kurkumino poveikį, įskaitant antioksidantą [4], imunomoduliuojantį, širdies apsaugą [5], nefroprotekcinį [6], hepatoprotekcinį [7,8], antinavikinį [9]. ,10], antimikrobinis, antidiabetinis [11] antireumatinis[12] senėjimą stabdantis [13], priešuždegiminis, ypač prieš neurouždegiminis [14], taip pat mikrogliją slopinantis poveikis [15].
Nepaisant daugybės gydomųjų savybių, šis biologiškai aktyvus junginys turi prastą biologinį prieinamumą dėl nepakankamos absorbcijos, cheminio nestabilumo ir greito metabolizmo organizme.
Siekiant padidinti kurkumino biologinį prieinamumą, buvo įrodyta, kad nanonešikliai yra perspektyvi strategija, siekiant sustiprinti jo gydomąjį poveikį.
Dėl savo nanometrinio dydžio ir cheminių savybių nanodalelės [16], liposomos [17,18]micelės, fosfolipidinės pūslelės [19] ir polimerinės nanodalelės [20,21] gali padidinti kurkumino efektyvumą.
Tarp natūralių nanonešiklių tarpląstelinės pūslelės, ypač egzosomos, yra naudojamos kaip vaistų tiekimo sistema.cistanche milteliaiEgzosomos iš ląstelių išsiskiria egzocitozės būdu, subrendus multivezikuliniams kūnams.
Egzosomos gali tarpininkauti ląstelių ryšiui su savo baltymų, lipidų ir nukleorūgščių sudėtimi [22]. Egzosomos lipidinėje membranoje kurkuminas yra dėl sąveikos tarp hidrofobinių uodegų ir hidrofobinės veikliosios medžiagos. Įterpimas į lipidų dvigubą sluoksnį garantuoja kurkumino apsaugą nuo skilimo [23]. Tiesą sakant, kurkuminas su egzosomine formule yra veiksmingesnis, palyginti su liposominiu kurkuminu ir laisvuoju kurkuminu [23].
Zhang ir kt. įrodė, kad intranazališkai vartojami kurkumino turintys ex yra uždegimo sukeltų ligų modeliuose, tokiuose kaip lipopolisacharido (LPS) sukeltas smegenų uždegimo modelis, eksperimentinis autoimuninis encefalitas ir GL26 smegenų auglio modelis, mažina neurologinį uždegimą arba naviko dydį [24]. ].
Išemijos-reperfuzijos (I/R) sužalojimų atveju kurkuminu pakrautos egzosomos gali sumažinti reaktyviųjų deguonies rūšių (ROS) gamybą pažeidimuose, sumažinti kraujo-smegenų barjero (BBB) pažeidimus ir slopinti mitochondrijų sukeltą neuronų apoptozę [25]. ]. Liposomos yra nanopūslelės, sudarytos iš vieno arba kelių dvigubų fosfolipidų sluoksnių, apimančių hidrofilines, lipofilines ir amfifilines molekules [26], kurios gali būti naudojamos vaistams tiekti į tikslines vietas.
Mohajeri ir kt. parodė polimerizuoto nano-kurkumino priešuždegiminį ir antioksidacinį poveikį, kuris turėjo teigiamą poveikį eksperimentiniam išsėtinės sklerozės autoimuninio encefalomielito modeliui ir paskatino mielino atstatymo mechanizmus [27].

Nano-kurkuminas turi neuroprotekcinį poveikį ankstyviems smegenų sužalojimams, jis iš tikrųjų gali susilpninti BBB disfunkciją po subarachnoidinio kraujavimo, nes neleidžia sunaikinti sandarios jungties baltymo (ZO-1, okludino ir klaudino-5). . Be to, nano-kurkuminas padidina glutamato transporterio-1 reguliavimą, kuris sumažina glutamato koncentraciją smegenų skystyje (CSF) po subarachnoidinio kraujavimo ir slopina mikroglijos aktyvaciją [28]. W{7}} riebalų rūgščių ir nano-kurkumino derinys žymiai sumažina migrenos priepuolių dažnį, nes moduliuoja IL-6geno ekspresiją ir C reaktyviojo baltymo lygį, kaip įrodo klinikinių tyrimų rinkinys [29 ]. CUR pakrautos liposomos sumažina angiotenziną konvertuojančio fermento aktyvumą tikslinėse smegenų srityse ir stiprina atmintį žiurkėms, sergančioms Alzheimerio liga (AD) [30].
Pasaulyje ilgėjant gyvenimo trukmei, daugėja neurodegeneracinių ligų, o tai sukelia didesnę socialinio ir ekonominio diskomforto naštą pacientams, šeimoms ir bendruomenėms [31]. Neurodegeneracinėms ligoms būdingi sutrikimai, dėl kurių laipsniškai pažeidžiama neuronų struktūra ir (arba) funkcija ir jų sinapsinis tinklas, galiausiai prarandama smegenų funkcija.
AD, Parkinsono liga (PD), Hantingtono liga (HD), išsėtinė sklerozė (MS) ir amiotrofinė šoninė sklerozė (ALS) yra dažniausios neurodegeneracinės ligos, kuriomis serga vyresnio amžiaus žmonės.
Veiksniai, lemiantys neurodegeneracines ligas, yra genetiniai polimorfizmai, didėjantis amžius, lytis, prastas išsilavinimas, endokrininės ligos, oksidacinis stresas, uždegimai, insultas, hipertenzija, diabetas, rūkymas, galvos trauma, depresija, infekcija, navikai, vitaminų trūkumas, imuninės ir medžiagų apykaitos sutrikimai. , ir cheminio poveikio [32].
Uždegiminis atsakas smegenyse arba nugaros smegenyse yra žinomas kaip neurouždegimas. Neurouždegimas būdingas daugeliui smegenų ligų, įskaitant AD, PD, MS ir daugelį kitų. Šis procesas vyksta gaminant citokinus, chemokinus, reaktyviąsias deguonies rūšis ir antrinius pasiuntinius, kurie gali sunaikinti BBB, dėl to pažeidžiamos ląstelės ir prarandamos neuronų funkcijos [33]. Glia, endotelio ląstelės ir periferinės imuninės ląstelės gamino šiuos tarpininkus. Tarp glijos ląstelių mikroglijos ir astrocitai vaidina pagrindinį vaidmenį neurodegeneracinių ligų patofiziologijoje. Astrocitai veikia kartu, kad palaikytų CNS homeostazę ir skatintų neuronų išgyvenimą reguliuodami metabolitų srautą ir kraujotaką. Mikroglijos ląstelės suvokia smegenų audinio homeostazės sutrikimą ir veikia kaip CNS fagocitai [34,35]. Šios apžvalgos tikslas – pabrėžti kurkumino svarbą gydant AD, PD, MS glioblastomą ir epilepsiją, sutelkiant dėmesį į galimą jo veikimo mechanizmą gerinant jų eigą.
2. Kurkuminas ir AD
AD yra pagrindinė demencijos priežastis visame pasaulyje ir sudaro 60-80 proc. atvejų, kuriems diagnozuojama demencija [36]. Klinikiniu požiūriu AD paprastai pasireiškia atminties praradimu, laipsnišku pažinimo nuosmukiu ir ankstesnio funkcionavimo bei našumo darbe ar įprastoje veikloje pablogėjimu. Neurodegeneracija buvo priskirta ir skatinama tarpląstelinių amiloidinių (A) plokštelių ir tarpląstelinių neurofibrilinių raizginių (NFI), sudarytų iš hiperfosforilinto tau baltymo, žmogaus smegenų žievės ir limbinėse srityse [37l. A plokštelės susidaro dėl anomalaus amiloido pirmtako baltymo (APP) apdorojimo sekretazėmis (BACE1) ir sekretazėmis, dėl kurių susidaro įvairių tipų A monomerai, tarp kurių yra A 40 ir A 42 (labai netirpūs ir agreguojami). -linkęs). Dėl to A monomerai toliau oligomerizuojasi ir agreguojasi į plokšteles. NFT yra antrasis patologinis AD požymis ir susideda iš hiperfosforilinto tau, lokalizuoto neuronų citoplazmoje [38]. Tau turi mikrovamzdelius surišantį domeną ir susijungia su tubulinu, todėl susidaro stabilūs mikrovamzdeliai. A gali suaktyvinti kelias kinazes, įskaitant glikogeno sintazės kinazę 3 (GSK-3), nuo ciklino priklausomą kinazę 5 (CDK5) ir kitas, pvz., baltymų kinazę C, baltymų kinazę A, ekstraląstelinio signalo reguliuojamą kinazę 2 (ERK2), serino/treonino kinazė, kuri fosforilina tau ir sukelia jo oligomerizaciją [39. Dėl to mikrotubulai tampa nestabilūs, o jų subvienetai virsta dideliais tau gijų gabalais, kurie toliau kaupiasi į NFI. NFI yra labai netirpūs ir dėl to nenormaliai nutrūksta ryšys tarp neuronų ir signalo apdorojimui ir galiausiai neuronų apoptozė [40]. Remiantis amiloido hipoteze, patologiniai tau pokyčiai laikomi A nusėdimo įvykiais. Tačiau taip pat buvo iškelta hipotezė, kad A ir tau veikia lygiagrečiais keliais, kurie sukelia AD ir sustiprina vienas kito toksinį poveikį [41]. Atsižvelgiant į socialinį ir ekonominį poveikį, svarbu suprasti, kurie rizikos veiksniai gali turėti įtakos AD išsivystymui, taip pat rasti vaistus, kurie gali užkirsti kelią ligos atsiradimui arba sustabdyti ligos eigą. prieinami AD gydymui, pvz., acetilcholinesterazės inhibitoriai (donepezilas, rivastigminas ir galantaminas) ir glutamato antagonistas memantinas, kurie nėra veiksmingi stabdant progresuojančią ligos eigą 42].cistanche salsos ekstraktasNeseniai FDA patvirtino pirmojo vaisto su numanomu ligą modifikuojančiu mechanizmu Aducanumab, kuris yra žmogaus monokloninis antikūnas, selektyviai reaguojantis su A agregatais ir mažinantis A plokšteles smegenyse, naudojimą, taip numatant svarbią klinikinę naudą. Tačiau norint patikrinti tikrąją vaisto klinikinę naudą, reikia atlikti klinikinius tyrimus po patvirtinimo [43]. Neseniai buvo ištirti keli natūralūs junginiai, siekiant geriau suprasti galimą jų veiksmingumą „gydant“ AD[44]. Dabartiniai tyrimai yra skirti kurkumino veikimo mechanizmui ir jo vaidmeniui moduliuojant AD progresavimą.
Kurkumino veikimo mechanizmai yra pleiotropiniai (S1 lentelė)[45] ir nukreipti į A ir tau (žr. 1 pav.). Be to, jis moduliuoja kitus ligos proceso aspektus: taip pat suriša varį, mažina cholesterolio kiekį, keičia mikroglijos aktyvumą, slopina acetilcholinesterazę, stiprina insulino signalizacijos kelią ir veikia kaip antioksidantas [45]. Atrodo, kad kurkuminas yra skirtas A skirtingais lygiais. Tiesą sakant, buvo aprašyta, kad jis slopina A gamybą; be to, kurkuminas slopina agregaciją tiek in vitro, tiek pelių modeliuose, taip užkertant kelią apnašų susidarymui ir skatina fibrilinės formos skaidymąsi [46].
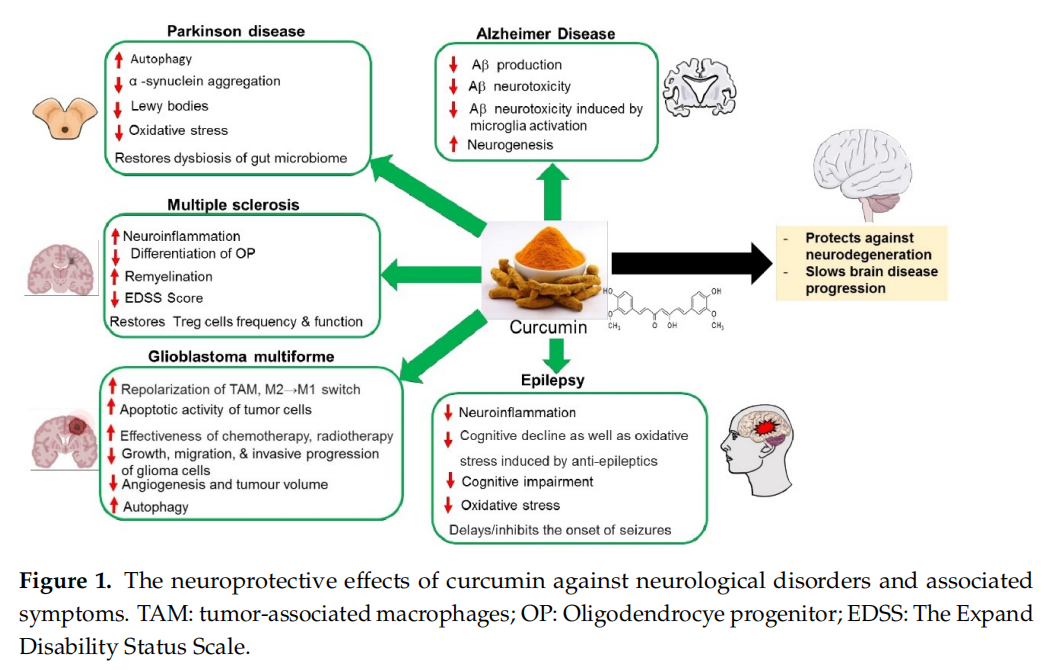
Kalbant apie A gamybą, in vitro tyrimai parodė, kad kurkuminas veikia kaip BACE1 inhibitorius, kuris dalyvauja skaidant APP[47l. Šie rezultatai buvo patvirtinti AD pelių modeliuose, parodydami, kad kurkuminas sumažina BACE1 ekspresiją, taip sumažindamas A susidarymą [48].
Be to, atrodo, kad kurkuminas slopina nuo GSK{0}}priklausomą presenilino 1(PS1) aktyvaciją ir dėl to mažina A gamybą. Iš tikrųjų kurkuminu gydomose neuroblastomos SHSY5Y ląstelėse ženkliai sumažėjo PS1 ir GSK{5}} lygis. ryškus A gamybos sumažėjimas priklausomai nuo dozės ir laiko [49]. GSK-3 aktyvuojamas, kai yra defosforilinamas Ser9 vietoje. Jo aktyvumą prieš srovę reguliuoja Akt, serinui / treoninui būdinga baltymų kinazė. Fosfatidilinozitolis (PIP) ir PDK sukeltas Akt fosforilinimas Ser473 ir Thr308 vietose sukelia Akt aktyvavimą ir dėl to fosforilinimą bei GSK slopinimą-3. Akt aktyvumą neigiamai reguliuoja PTEN, kuris katalizuoja fosfoinozitidą, kad defosforilintų deaktyvuojantį PIP3 signalą. PI3K/Akt/GSK-3 signalizacijos kelią taip pat tiesiogiai veikia A ekspozicija [50], iš tiesų, oligomerai aktyvūs GSK-3 per defosforilinimą Ser9 vietoje. Be to, A sukelia sumažėjusį Akt fosforilinimo reguliavimą, taip pat per didelę PTEN, jo neigiamo reguliatoriaus, ekspresiją, o tai lemia GSK aktyvavimą pasroviui-3. Kurkuminas slopina ir per didelę PTEN mRNR ekspresiją, sumažėjusį fosforilinimo sukeltos Akt aktyvacijos reguliavimą, taip pat A sukeltą GSK-3 aktyvaciją [51,52], taip sumažindamas A gamybą ir apnašų susidarymą (2 pav.). .

Kalbant apie kurkumino vaidmenį slopinant A agregaciją, buvo pasiūlyta, kad kurkuminas destabilizuoja patrauklias jėgas, reikalingas lakštams susidaryti amiloidinėse plokštelėse dėl jo hidrofobiškumo arba sąveikos tarp keto arba enolio žiedų ir aromatinio A dimerų žiedo. [53]. Lakštų destabilizacijai taip pat įtakos turi sąveika tarp kurkumino hidroksilo grupių aromatiniuose žieduose ir A poliarinių kišenių [54].
Įdomu tai, kad naujausi in vitro tyrimai buvo skirti kurkumino vaidmeniui užkertant kelią A neurotoksiškumui. Thapa ir kt. parodė, kad kurkuminas sumažina A įterpimo į plazmos membraną greitį ir todėl veikia kaip apsauginis faktorius nuo A membranos toksiškumo. Išsamiau kurkuminas sumažino plazminės membranos sutrikimą dėl A, taip išvengdamas padidėjusio kalcio antplūdžio ir ląstelių mirties [55]. Atrodo, kad neuroprotekcinis kurkumino poveikis, tikriausiai sukeltas membranos, mažina toksiškumą, kurį sukelia daugybė A konformerių, įskaitant monomerinius, oligomerinius, priešfibrilinius ir fibrilinius A [56]. Įdomu tai, kad taip pat buvo aprašyta, kad kurkuminas skatina netoksiškų „ne kelio“ tirpių oligomerų ir ikifibrilinių agregatų susidarymą [56]. Kitas Huang ir kt. tyrimas. parodė, kad kurkuminas gali susilpninti A sukeltą glutamato NMDA receptorių aktyvavimą ir taip slopina intracelulinį Ca 2 plius, kuris yra susijęs su glutamato toksiškumu, padidėjimą. Atrodo, kad kurkumino poveikis NMDA receptorių/Ca2 plius kelio slopinimui užkerta kelią A sukeltam ląstelių pažeidimui [57]. Nepaisant šių įdomių rezultatų, norint išversti šias išvadas ir rasti galimą klinikinį panaudojimą, vis dar reikia atlikti in vivo tyrimus. Kalbant apie NFI, GSK{11}} reguliuoja tau fosforilinimą, pridedant fosfatų grupių ant serino ir treonino aminorūgščių liekanų. Nustatyta, kad kurkuminas apsaugo nuo tau hiperfosforilinimo, veikdamas kaip GSK-3 inhibitorius [45,47]. Išsamiau Huang ir kt.[51] parodė, kad kurkuminas slopina A sukeltą tau hiperfosforilinimą, apimantį PTEN/Akt/GSK-3 kelią žmogaus ląstelių kultūrose, ir todėl turi įtakos tau hiperfosforilinimo slopinimui, užkertant kelią agregacijai NFI.
Kurkuminas taip pat gali turėti įtakos NFT klirensui ir dėl to sumažėja tau sukeltas toksiškumas. Iš tiesų, pelių neuronų ląstelių kultūrose kurkuminas, esant mažai koncentracijai, padidina su BCL2 susijusio atanogeno 2 (BAG2), molekulinio šaperono, kuris tiekia tau į proteasomą skaidymui, ekspresiją [58].cistanche stiebasTačiau kadangi šis tyrimas nebuvo atliktas su patologiniais neuronais, šiuos rezultatus reikia patvirtinti. Kitas tyrimas, kurį atliko Miyasaka ir kt. aprašė, kad acetilinto tubulino, mikrotubulų stabilizavimo rodiklio, lygiai buvo žymiai didesni kurkuminu apdorotuose nematoduose, o tai rodo, kad kurkuminas gali sušvelninti tau sukeltą neurotoksiškumą, pagerindamas mikrotubulų stabilizavimą [59]. Be A ir NFT, AD patogenezėje reikia atsižvelgti į kitus veiksnius. Mikroglijos vaidina svarbų vaidmenį įgimtame CNS imuniniame atsake ir gali būti klasifikuojamos į M1 (kuris išskiria neurotoksinius citokinus, prostaglandinus, ROS ir azoto oksidą) ir M2 fenotipą (kuris išskiria neuroprotekcinius ir priešuždegiminius mediatorius bei fagocitams toksiškus baltymų agregatus). ). Mikroglijos vaidmuo sergant AD buvo nuodugniai ištirtas [60]. A nukrypsta nuo neuroprotekcinio M2 mikroglijos iki neurotoksinio M1 fenotipo [61]. Be to, A kaupimasis suaktyvina mikrogliją, kuri gamina uždegiminius mediatorius, taip skatinant tolesnį A kaupimąsi, o tai lemia šią teigiamą grįžtamojo ryšio kilpą. Atrodo, kad kurkuminas vaidina svarbų vaidmenį mažinant neurotoksiškumą dėl A sukeltos mikroglijos aktyvacijos [62]. Šiuo atžvilgiu buvo pranešta, kad kurkuminas blokuoja ERK1/2 ir p38 kinazės signalus A suaktyvintose mikroglijose, taip sumažindamas TNF-x, IL-1 ir IL-6 gamybą [63] ir, be to, susilpnina azoto oksido išsiskyrimą ]64]. Be to, kurkuminas slopina fosfoinozitido 2 kinazes (PI3K) / Akt fosforilinimą ir branduolinio faktoriaus-kB (NF-kB), kurie skatina mikroglijų aktyvaciją ir neurouždegimo kelius, aktyvavimą [64]. Įdomu tai, kad kurkuminas padidina peroksisomų proliferatorių aktyvuotų receptorių y (PPARy) baltymų kiekį, taip padidindamas PPARy priešuždegiminį aktyvumą mažinant NF-kB ir ERK takų reguliavimą. Kita vertus, kurkuminas gali sustiprinti neuroprotekcinį M2 mikroglijos poveikį: iš tikrųjų, atrodo, kad A fagocitozė padidėja mikroglijose AD pacientams, gydytiems kurkuminoidais in vitro [65].
Žymus neurogenezės sumažėjimas buvo plačiai aprašytas sergant AD ir kitomis neurodegeneracinėmis ligomis [66]. Ankstesniuose darbuose nustatyta, kad kurkuminas reguliuoja neurogenezę aktyvuodamas Wnt kelią in vitro ir suaugusių žiurkių hipokampo ir subventrikulinėje zonoje. Wnt sąveikauja su 7-transmembraniniu „frizzled“ receptoriumi ir fosforilintu koreceptoriumi mažo tankio lipoproteinu (LRP-5/6), taip suaktyvindamas citoplazminį suskaidytą (Dvl) baltymą. Suaktyvintas Dvl baltymas sąveikauja su Axin/APC/GSK-3 naikinimo kompleksu ir slopina GSK-3. GSK-3 slopinimas lemia citoplazminio katenino kaupimąsi ir jo perkėlimą į ląstelės branduolį. Branduolyje -kateninas sąveikauja su TCF/LEF promotoriaus kompleksu, todėl aktyvuojami tiksliniai genai, dalyvaujantys CNS proliferacijoje ir diferenciacijoje. Atrodo, kad kurkuminas įvairiais lygmenimis veikia šį kelią. Išsamiau kurkuminas sąveikauja su Wif-1 ir Dkk-1, kurios yra Wnt slopinančios molekulės, todėl padidėja Wnt lygis. Be to, kurkuminas gali sąveikauti su GSK-3, taip padidindamas citoplazmos -katenino kiekį ir sustiprindamas -katenino branduolio translokaciją, dėl to sustiprėja TCF/LEF ir ciklin-D1 promotoriaus aktyvumas ir padidėja neurogenezė. Įdomu tai, kad nors maža kurkumino koncentracija smegenyse (500 nM) stimuliuoja neurogenezę, didelė koncentracija smegenyse (10 μM) slopina neurogenezę ir neuroplastiškumą [67]. Todėl kurkumino koncentracijos pasirinkimas turėtų būti kruopščiai parinktas. Ikiklinikiniai modeliai daugiausia parodė teigiamą kurkumino poveikį AD, tačiau tik nedaugelis klinikinių tyrimų ištyrė kurkumino poveikį žmogaus pažinimo funkcijai sergant AD, o rezultatai yra ne tokie nuoseklūs. Išvados apie A mažinimą yra dviprasmiškos, nes tarp kurkumino ir placebo reikšmingų A arba tau koncentracijos pokyčių plazmoje ar likvore nenustatyta [68, 69]. Kita vertus, neurovizualinis tyrimas patvirtina, kad kurkuminas sumažina A nuosėdas smegenyse 2-(1-{6-[(2-[F-18]fluoretilo) (metil)amino-2-naftil}etilideno) malononitrilo pozitronų emisijos tomografija (FDDNP-PET) nesergantiems demencija [70]. Šie neatitikimai gali būti susiję su metodologijos ir įtrauktos populiacijos skirtumais |71. Be to, kurkuminas pasižymi mažu biologiniu prieinamumu ir jo poveikiu antioksidantų keliams bei neurogenezei tikriausiai reikia daugiau laiko, kad žymiai pagerėtų pažinimo pajėgumai ir A sumažinimas. Taigi, anksčiau aprašytas nestiprus poveikis taip pat gali atsirasti dėl gana trumpos gydymo trukmės. Reikia atlikti tolesnius tyrimus, siekiant pagerinti kurkumino biologinį prieinamumą ir geriau ištirti kurkumino poveikį A ir NFT, kad būtų galima suprasti, ar kurkuminas gali būti naujas potencialus AD prevencijos ir gydymo veiksnys.
3. Terapinis kurkumino poveikis sergant PD
PD yra antra pagal dažnumą neurodegeneracinė liga po AD. Apskaičiuota, kad 2020 m. pasaulyje PD kenčia apie 10 milijonų žmonių (https://www.epda.eu.com/, pasiekiama 2021 m. spalio 27 d.)[72]. PD daugiausia paveikia dopaminą gaminančius neuronus, esančius vidurinių smegenų juodojoje substantoje, sukeldama sunkius motorinius ir pažinimo sutrikimus. Idiopatinio PD atveju patofiziologiniai mechanizmai apima -sinukleino ir mitochondrijų kvėpavimo disfunkciją paveikiančio komplekso, kurį sukelia ROS, gamybą [73]. Jam taip pat būdingas baltymų agregatų, daugiausia susidedančių iš -sinukleino, kaupimasis dėl baltymų skaidymo mechanizmų, tokių kaip lizosominė sistema, gedimo [74,75]. Dauguma esamų gydymo būdų yra tik simptominiai. Tai apima dopamino priedą, kuris laikinai kontroliuoja motorinę disfunkciją, kurią sukelia dopaminerginės nigrostrialinės sistemos degeneracija. Gilioji smegenų stimuliacija (DBS) naudojama vaistams atspariam PD.
Siekiant užkirsti kelią oksidaciniam stresui ir sumažinti ligos progresavimą, natūralių antioksidantų naudojimas išlieka galima alternatyvia terapija. Atsižvelgdami į neuroprotekcinį, priešneurouždegiminį ir antioksidacinį poveikį prieš streso sukeltą kurkumino neurodegeneraciją, čia aptariame naujausius atradimus, susijusius su teigiamu kurkumino poveikiu mažinant PD progresavimą ir prevenciją [12].
Nors PD patogenezė vis dar plačiai neaiški, buvo pasiūlyti keli mechanizmai ir įvairūs įrodymai patvirtina svarbų mitochondrijų disfunkcijos vaidmenį PD patogenezėje [76].
Neseniai atliktas tyrimas praneša apie apsauginį kurkumino poveikį nuo mitochondrijų disfunkcijos ir ląstelių mirties siRNR tarpininkaujamame PINK1 numušimo PD modelyje [77]. Kitame tyrime aprašomas kurkumino poveikis mitochondrijų disfunkcijai parakvato sukeltame PD toksiškumo modelyje fibroblastuose, gautuose iš LRRK2-mutacijai teigiamo PD ir sveikatos kontrolės. Tiesą sakant, iš anksto apdorojant šį ląstelių modelį kurkuminu prieš gydymą parakvatu, pagerėjo maksimalus kvėpavimas ir su ATP susijęs kvėpavimas, nepažeidžiant kvėpavimo pajėgumų. Po gydymo parakvatu fibroblastų gydymas kurkuminu nepagerino mitochondrijų kvėpavimo pagal tris parametrus (maksimalus kvėpavimas, su ATP susijęs kvėpavimas ir atsarginis kvėpavimo pajėgumas), todėl galima daryti prielaidą, kad kurkuminas turėjo prevencinį poveikį prieš prasidedant PD. 78].

Neseniai atliktas Motawi ir kt. [79] tiriant kurkumino ir maisto papildų poveikį rotenono pelių PD modeliui, nustatytas bendras statistiškai reikšmingas pagerėjimas. Iš tiesų, kurkumino skyrimas rotenonu gydomoms pelėms pagerino -sinukleino kiekį ir sumažino Lewy kūnus. Gyvūnų elgesys taip pat pagerėjo, o uždegimo mediatorių kiekis žymiai sumažėjo kurkuminu gydytose pelėse, palyginti su kontroline grupe. Tai apima IL-6, CRP ir Ang Il, kurie anksčiau buvo rodomi priešuždegiminį ir profibrozinį poveikį, kuris prisideda prie laipsniško organų funkcijos blogėjimo sergant PD[80]. Vertinant PD žymenis, nustatytas reikšmingas adenozino A2AR geno ekspresijos lygio sumažėjimas pelėms, gydytoms kurkuminu, palyginti su rotenono grupe. Kitas daug žadantis dopamino ir serotonino lygio pagerėjimas buvo pastebėtas kurkuminu gydytų pelių PD modeliuose. Be to, gydymas kurkuminu sumažina oksidacinį stresą PD pelių modeliuose [79]. Kiti patvirtinamieji įrodymai rodo panašius rezultatus žiurkių PD modeliuose su didesniu žiurkių atsaku į gydymą kurkuminu, atsižvelgiant į oksidacinį stresą ir energetinius rodiklius. Todėl kurkuminas susilpnino sunkų PD poveikį žiurkių modeliui ir gali būti laikomas galimu maisto papildu [81].
Literatūros įrodymai parodė, kad autofagijos-lizosomų kelio (ALP) pažeidimas vaidina lemiamą vaidmenį PD patogenezėje. Neseniai atliktas tyrimas, skirtas kurkumino poveikiui alfa-sinukleino (S) oligomerui, naudojant molekulinės dinamikos modeliavimo metodą, parodė, kad kurkuminas sumažino S-oligomero struktūrinį stabilumą, sutrikdydamas jo bendrąsias savybes. Be to, kurkuminas užkirto kelią -sinukleino oligomerų agregacijai, o fibrilių susidarymą slopino [82].
Dėl kurkumino gebėjimo sumažinti netinkamai sulankstytą -sinukleiną skatinant autofagiją, naujausi tyrimai ištyrė jo poveikį autofagijos reguliavimui. Taigi, PD gydymas ląstelių modeliu parodė padidėjusią su mikrotubuliais susijusio baltymo 1 lengvosios grandinės 3 (LC3-II) ekspresiją, branduolio plazmos baltymo nustatymą, branduolinės transkripcijos faktoriaus EB (TFEB) ir autofagijos giminingo baltymo lizosomos membranos baltymas 2 (ALAMP2A). Dėl to skatinama autofagijos-lizosomų sintezė ir autofaginis -sinukleino klirensas [83,84].
TFEB buvo nustatytas kaip vienas iš svarbiausių autofagijos ir lizosomų biogenezės reguliatorių [8586]. Tai sustiprino hipotezę, kad TFEBcan laikomas nauju terapiniu PD taikiniu. Tiesą sakant, kurkumino darinys, vadinamas E4 (kurkumino analogas), sugebėjo suaktyvinti ir skatinti TFEB perkėlimą iš citoplazmos į branduolį. Šį perkėlimą lydi autofagijos ir lizosomų biogenezės stimuliavimas. Mechaniškai junginys E4 aktyvavo TFEB slopindamas AKT-MTORC1 kelią. Be to, PD ląstelių modeliuose buvo įrodyta, kad E4 sumažina -sinukleino kiekį ir apsaugo nuo MPP plus (1-metil-4-fenilpiridinio jonų) citotoksiškumo nervų ląstelėse. Šie daug žadantys duomenys, rodantys apsauginį E4 poveikį in vitro, vis dar reikalauja papildomų in vivo eksperimentinių bandymų, nes E4 biologinis prieinamumas smegenyse vis dar nežinomas. Neuroprotekcinis E4 veiksmingumas turi būti toliau tiriamas naudojant PD gyvūnų modelius [87].
Be to, in vivo intraperitoninė kurkumino injekcija skatino LC3-II baltymo ekspresiją ir slopino P62 ekspresiją autofagijos naudai. Kurkuminas slopino a-sinukleino ekspresiją ir dopamino neuronų apoptozę MPTP sukeltame PD pelės modelyje (kurkuminas 80 mg/kg 14 dienų) ir pagerino pelių judėjimo sutrikimą 33]. Įrodyta, kad sevoflurano anestezija sukelia pažinimo sutrikimus, aktyvindama autofagiją jaunų pelių hipokampe [88]. Įdomu tai, kad kurkuminas šešias dienas galėjo moduliuoti autofagiją 300 mg/kg doze ir slopinti sevoflurano sukeltą pelių atminties sutrikimą [89]. Apsauginis kurkumino poveikis buvo ištirtas vartojant per burną 6-hidroksidopamino (6-OHDA) – sukelto PD gyvūnų modelio.cistanche tubulosa nauda ir šalutinis poveikisKurkumino neuroprotekcinis poveikis (200 mg/kg) 2 savaites prieš ir po operacijos buvo įvertintas atliekant morfologinę ir elgesio analizę. Motorinė funkcija buvo įvertinta praėjus trims savaitėms po operacijos. Kurkuminas žymiai pagerino nenormalų motorinį elgesį ir buvo įrodyta, kad apsaugo nuo sumažėjusių dopaminerginių neuronų juodosios medžiagos ir caudate-putamen branduolyje, kaip rodo tirozino hidroksilazės (TH) imunoreaktyvumas.
Intraperitoninis 7-nAChR selektyvaus antagonisto metilakonitino vartojimas panaikino šį neuroprotekcinį poveikį. Tai patvirtino 7-nAChR poveikį kurkumino sukeliamam poveikiui. Šiame tyrime buvo įrodyta, kad kurkuminas turi neuroprotekcinį poveikį 6-hidroksidopamino (6-OHDA) žiurkės PD modelyje per 7-nAChR tarpininkaujamą mechanizmą [90]. Zhang ir kt. parodė, kad G2385R-LRRK2 ekspresija sukėlė neurodegeneraciją žmogaus neuroblastomoje SH-SY5Y ir pelės pirminiuose neuronuose. Šis neurotoksiškumas, kurį sukelia oksidacinis stresas, sukelia apoptozinio kelio aktyvavimą. Kurkuminas, pasižymintis antioksidaciniu aktyvumu, reikšmingai apsaugojo nuo kombinuotos G2385R-LRRK{17}}sukeliamos neurodegeneracijos, nes susilpnino mitochondrijų ROS lygį, kaspazės-3/7 aktyvaciją ir PARP skilimą bei sumažino ląstelių aplinkos stresorių H. , O (2 pav.). Šie rezultatai suteikia naujų įžvalgų apie su G2385R-LRRK{23}}susijusios neurodegeneracijos mechanizmus ir galimą terapinį kurkumino poveikį PD sergantiems pacientams, nešiojantiems G2385R [91].
Be aukščiau aptartų kurkumino neuroprotekcinių mechanizmų nuo PD, naujas augantis susidomėjimas žarnyno ir smegenų ašimi PD gali paaiškinti kurkumino neuroprotekcines savybes, nepaisant riboto jo biologinio prieinamumo. Tiesą sakant, kurkuminas gali netiesiogiai veikti CNS per mikrobiotos ir žarnyno ašį. Sudėtinga dvikryptė sistema, kuri atlieka esminį vaidmenį smegenų sveikatai, vis dar nėra visiškai suprantama.
Naujausi tyrimai parodė, kad kurkuminas atkuria žarnyno mikrobiomo disbiozę. Disbiozė apibrėžiama kaip stabili mikrobų bendruomenės būklė, kuri funkciškai prisideda prie ligos etiologijos, diagnozavimo ar gydymo [92]. Tačiau kurkumino modifikacijos, kurias sukelia bakterijos, nesudaro aktyvesnių kurkumino metabolitų [93]. Ši abipusė sąveika galėtų išlaikyti subalansuotas fiziologines funkcijas ir atlikti pagrindinį vaidmenį neuroprotekcijoje ir PD vystymosi bei progresavimo prevencijoje. Nepaisant padidėjusio mokslinių tyrimų susidomėjimo su PD susijusiais nemotoriniais simptomais, tokiais kaip depresija, uoslės trūkumas, vidurių užkietėjimas, miegas ir elgesio sutrikimai, kurkumino poveikis PD reikalauja tolesnių tyrimų.
Apibendrinant, kurkuminas parodė daug žadantį poveikį gydant PD (S1 lentelė) (žr. 1 paveikslą). Tačiau ištyrus daugiau kurkumino formulių in vivo modeliuose ir atliekant klinikinius tyrimus, kurkuminas būtų naudojamas kaip prevencinė terapija, skirta blokuoti arba sulėtinti PD atsiradimą.
4. Kurkuminas kaip terapinis kandidatas sergant IS
IS yra lėtinė neurouždegiminė, autoimuninė demielinizuojanti jaunų suaugusiųjų CNS liga, kuria serga milijonai žmonių [94]. IS yra susijusi su keliais patofiziologiniais procesais, įskaitant lėtinį uždegimą, pakitusią imuninę sistemą, BBB pažeidimą kaip recidyvuojančius-remituojančius (RR) epizodus, didelio skaičiaus leukocitų infiltraciją, oksidacinį stresą, demielinizaciją, dėl kurios pažeidžiami aksonai ir neuronai, remielinizacija. ir taisymo sistemų aktyvinimas [95-98]. Nors pagrindinė IS priežastis vis dar nežinoma, mokslininkai mano, kad IS yra daugiafaktorinė liga, kuriai būdingi genetiniai, aplinkos ir autoimunologiniai veiksniai, didinantys IS išsivystymo riziką [99]. Pradinei uždegimo fazei būdingas IL-22, IL-17 ir T ląstelių indėlis, sukeliantis uždegiminės kaskados aktyvavimą ir kitus patofiziologinius MS požymius, kurie yra demielinizacijos ir demielinizacijos priežastis. aksonų pažeidimas [100].
Iki šiol galimas tik simptominis IS gydymas, kurio pagrindinis dėmesys skiriamas ligos atkryčių ir remituojančių epizodų gydymui. Dabartinis IS gydymas yra žinomas kaip ligą modifikuojantis gydymas (DMT), kurio metu buvo sukurti įvairūs junginiai. Dauguma šių terapijų yra imunomoduliuojantys junginiai, patvirtinti įvairių tipų IS gydymui ir skirti skirtingiems patofiziologiniams keliams [101,102]. Naudojamos kitos gydymo strategijos, apimančios naudojamą kamieninių ląstelių terapiją, pvz., autologinę kraujodaros kamieninių ląstelių transplantaciją (HSCT) ir B ląsteles ardančius monokloninius gydymo būdus [102]. Recidyvai yra dominuojantis RRMS klinikinis požymis, tačiau pasitaiko ir pradinėje antrinės progresuojančios IS fazėje [103]. Gydymo strategijos pasirinkimas recidyvuojančiai ir remituojančiai IS (RRMS), kuri yra 85-90 proc. IS sergančių pacientų, tebėra prieštaringa [104]Taip yra dėl to, kad su IS susiję simptomai kiekvienam asmeniui skiriasi. Nepaisant daugybės galimų gydymo būdų, iškilo naujų iššūkių, susijusių su tinkamos gydymo strategijos nustatymu kiekvienam konkrečiam atvejui. Be to, šių junginių saugumo ir veiksmingumo profilis, taip pat galimo šalutinio poveikio supratimas tebėra sudėtingas. Šalutinis poveikis, terapijos nesėkmės, toksiškumo ataskaitos ir didelė dabartinių cheminių vaistų kaina yra veiksniai, skatinantys vaistinių augalų, įskaitant kurkuminą, svarstymą gydymo tikslais. Neseniai buvo nustatytos kelios kurkumino savybės, kai kurios iš jų gali būti veiksmingos gydant IS, ypač jos priešuždegiminės savybės, nes slopina uždegimą skatinančių citokinų sekreciją (1 pav.)[103]. Čia apžvelgsime įvairias kurkumino savybes ir pagrindinį poveikį gydant MS (S1 lentelė). Atsižvelgiant į nepakeičiamą astrocitų vaidmenį gerinant ir sveikstant nuo IS, ankstesniame tyrime žmogaus astrocitų ląstelių linija (U373-MG) buvo naudojama kaip MS ląstelių modelis [105]. LPS iš anksto apdorotose ląstelėse kurkuminas sumažino IL6 ir MMP9 aktyvumo išsiskyrimą, nors jis neturėjo įtakos nei į insuliną panašaus augimo faktoriaus (IGF)-1, nei neurotropino-3 mRNR lygiui. Tai palaiko priešuždegiminį kurkumino poveikį astrocitams CNS[106]. Eksperimentinis autoimuninis encefalomielitas (EAE), gautas suleidus mieliną pelėms, buvo naudojamas kaip eksperimentinis modelis tiriant MS. Taip pat auga susidomėjimas kurkuminu, kaip galimu terapiniu kandidatu sergant MS. Įdomu tai, kad naujausi išvados apie kurkumino poveikį Lewis žiurkių EAE modeliams parodė, kad polimerizuotas nanoCUR (PNC), vartojamas 12, 5 mg / kg dozėmis, turėjo veiksmingą gydomąjį poveikį, reikšmingą poveikį EAE balams ir parodė mielino atstatymo mechanizmus. Tiesą sakant, PNC padidino mielinizaciją per patobulintą taisymo mechanizmą, kuris sukelia sustiprintus neurotrofinius veiksnius. Be to, jis panaikino EAE sukeltą neurouždegimą, nes slopino uždegimą skatinančio geno ekspresiją NF-kB, IL-1, IL-17, TNF-, MCP-1 ir padidino priešuždegiminį poveikį. genų ekspresija IL-4, IL-10, FOXP3 ir TGF- . Be to, PNC moduliavo oksidacinio streso žymenų raišką. Dar įdomiau, kad išankstinis gydymas PNC padidino progenitorinių ląstelių žymenis ir sulėtino EAE vystymąsi [27, 107, 108]. Atsižvelgiant į oligodendrocitų ir jų nesubrendusių pirmtakų, kurie yra svarbūs demielinizuojančių ligų gydymo terapinių strategijų taikiniai, svarbą, buvo tiriamas kurkumino poveikis oligodendrocitams. Kurkumino poveikio oligodendrocitų pirmtakų (OP) diferenciacijai tyrimas, ypač sergant uždegiminėmis ligomis, parodė, kad kurkuminas pagerina OP diferenciaciją padidindamas žymenų, susijusių su skirtingais vystymosi etapais, ekspresiją. Kurkuminas sugebėjo aktyvuoti PPAR-y OP, parodydamas nuo kurkumino priklausomą PPAR-【109】 branduolinį perkėlimą. Kurkumino gebėjimas skatinti OP diferenciaciją į (nesubrendusius oligodendrocitus) OL apėmė keletą mechanizmų, įskaitant PPAR-y ir ERK1/2 aktyvavimą ir TNF- - sukelto žalingo poveikio prevenciją. Neseniai atliktas tyrimas patvirtino kurkumino nanoformuliacijos veiksmingumą pacientų, sergančių IS, uždegiminėms savybėms. Iš tiesų, kurkuminas žymiai sumažino miRNR, įskaitant miR-145, miR-132 ir miR-16, taip pat uždegiminių mediatorių, tokių kaip STAT-1, NF-kB, ekspresiją, AP-1, IL-1, IL-6, IFN-y, CCL2, CCL5, TNF-. Kita vertus, nanoCUR sukėlė reikšmingą Sox2, Sirtuino ekspresijos lygio padidėjimą -1, Foxp3 ir PDCD1. Be to, IFN-, CCL2 ir CCL5 sekrecijos lygis buvo drastiškai sumažintas kurkuminu gydomų pacientų grupėje, palyginti su placebo grupe [110]. T pagalbinės 1 (Th1) ir T pagalbinės 17 (Th17) ląstelės dalyvauja IS patogenezėje ir manoma, kad jos yra terapiniai taikiniai [111] (žr. 2 pav.). Naujausi EAE modelių ir IS pacientų tyrimai pabrėžė svarbų Th17 ląstelių vaidmenį tarpininkaujant autoimuniniam neurouždegimui. Manoma, kad Th17, priešuždegiminė efektorinių Th ląstelių linija, yra svarbiausias IL17 citokinų gamintojas [112]. Taigi šios ląstelės dalyvauja demielinizacijoje ir aksonų / neuronų degeneracijoje. Įdomu tai, kad, palyginti su placebo grupe, Th17 ląstelių dalis ir RORyt bei IL-17 ekspresijos lygis buvo reikšmingai mažesnis pacientams, sergantiems IS, kurie kas savaitę gavo interferono -1a(Actovex) injekcijas ir papildomai NanoCUR 6 mėnesiams [113]. Dažniausiai EDSS balai IS pacientų, kuriems buvo papildomas nanoCUR, grupėje buvo geresnės kokybės, palyginti su placebo grupe. Apskritai nanoCUR gali slopinti MS pacientų ligos progresavimą. Apibendrinant galima teigti, kad nanoCUR gali būti vertinamas kaip neuroprotekcinis agentas nuo MS progresavimo, visų pirma nukreiptas į MS uždegimines savybes. Kiti tyrimai, naudojantys EAE modelius, parodė pagrindinį CD4 ir reguliuojančių T(Treg) ląstelių vaidmenį IS patogenezėje ir paūmėjime [114-117]. Svarbu pabrėžti, kad pacientams, sergantiems IS, yra sutrikęs Treg ląstelių dažnis ir slopinamoji funkcija[118,119]. Kitas neseniai atliktas Dolati ir kt. aprašytas nanoCUR poveikis Treg funkcijai ir dažniui pacientams, sergantiems IS. Grupė jų gavo nanoCUR kapsulės poveikį mažiausiai šešis mėnesius, kita grupė gavo placebą kaip kontrolinė grupė. Pacientams, sergantiems IS, buvo pastebėtas padidėjęs cirkuliuojančio Treg dažnis su didesne FoxP3 ekspresija. Apskritai, kurkumino nanoformuluotė sumažino EDSS balą pacientams, sergantiems IS, palyginti su pradiniu lygiu, o tai rodo, kad atsigavo po atkryčio, o ne iš tikrųjų pagerėjo. Remiantis aukščiau pateiktais rezultatais, nustatyta, kad nanoCUR yra laikomas imunomoduliuojančiu agentu, reguliuojančiu imuninės sistemos funkciją ir užkertant kelią autoreaktyvumui, moduliuodamas Treg ląstelių proporciją ir funkciją MS pacientams [120]. Šie stebėjimai rodo, kad nanoCUR gali atkurti Treg ląstelių dažnį ir funkciją pacientams, sergantiems IS, išryškindamas naujus terapinius kurkumino mechanizmus gydant IS kaip strategiją, skatinančią remielinizaciją.
5. Terapinis kurkumino poveikis daugiaformei glioblastomai
Glioblastoma (GBM) yra agresyviausia difuzinė astrocitinės kilmės glioma ir klasifikuojama kaip IV laipsnio glioma pagal PSO klasifikaciją [121]. GBM yra labiausiai paplitęs piktybinis pirminis smegenų auglys ir sudaro 54 procentus visų gliomų ir 16 procentų visų pirminių smegenų navikų [122]. GBM išlieka nepagydomu naviku, kurio išgyvenamumas yra 14-15 mėnesiai po diagnozės [123 124]. Nepaisant chirurginės rezekcijos pažangos, pacientų, sergančių GBM, prognozė išlieka prasta ir niūri [125]. Standartinis GBM gydymo metodas yra maksimali chirurginė rezekcija, po kurios kasdien taikoma pooperacinė spinduliuotė ir chemoterapija. Temozolomidas, geriamasis alkilinantis agentas, galintis prasiskverbti per BBB, yra labiausiai paplitęs pirmosios eilės GBM gydymas po operacijos. Jis vartojamas kartu su spinduline terapija [126].
Atsižvelgiant į invazinį GBM metastazavimo potencialo pobūdį, visiška naviko rezekcija yra sudėtinga. Daugelis veiksnių gali turėti įtakos šių kombinuotų terapinių priemonių veiksmingumui, įskaitant prastą į smegenis nukreiptą efektyvumą ir atsparumą daugeliui vaistų (MDR), dėl kurių GBM ląstelės turi labai prastą monoterapijos atsaką net tada, kai atsinaujina iš pašalintos kraštinės ertmės 127. Tiesą sakant, veiksmingumas chemoterapinio vaisto temozolomido (TMZ) vartojimą dažnai riboja atsparumas vaistams ir vis stiprėjantis neigiamas poveikis [128, 129]. Todėl gydymas GBM išlieka sudėtingas, kai reikia skubiai pagerinti chemoterapijos rezultatus ir nustatyti naujus galimus GBM gydymo tikslus.
Naujausi tyrimai parodė, kad kurkuminas ne tik turi priešvėžinį poveikį sergant plaučių, tiesiosios žarnos ir krūties vėžiu, daugiausia dėl savo antioksidacinių ir priešuždegiminių savybių, bet ir dėl to, kad jis padidina spinduliuotės ir chemoterapijos veiksmingumą, todėl pagerėja išgyvenamumą, taip pat antimetastazinių baltymų ekspresiją[130] ir tuo pačiu sumažinant jų šalutinį poveikį[131-134]. Įdomu tai, kad kurkuminas sustiprina ir sukelia apoptotinį aktyvumą prieš naviko ląsteles, susijusias su vidiniais ir išoriniais būdais, kaip aprašyta anksčiau [10, 135]. Todėl kurkumino derinys su chemoterapija ar radioterapija gali padidinti vėžio ląstelių jautrumą chemoterapijai ar spindulinei terapijai ir pagerinti chemoterapinių vaistų veiksmingumą. Iš tiesų, kaspazės -3 ir Bax ekspresija padidėjo, tačiau Bcl-2 ir HIF1 ekspresija U251 ląstelėse sumažėjo po gydymo 20 ir 30 μM kurkuminu. Tiek HIF-1, tiek ENO1 ekspresija U251 ląstelėse sumažėjo. Hipoksinėmis sąlygomis HIF-1 gali veikti kaip pagrindinis transkripcijos faktorius, aktyvuojantis užkoduotus glikolitinius fermentus, įskaitant ENO1.
Gerai dokumentuota, kad padidėjusi glikolizė laikoma viena iš GBM metabolinių savybių [136]. Enolazė yra svarbus glikolitinis fermentas, o ENO1 yra pagrindinė jo izoforma, išreikšta GBM. Tame pačiame tyrime ENO1 buvo sumažintas, todėl buvo slopinamas gliomos ląstelių augimas, migracija ir invazinis progresavimas. Apibendrinant galima pasakyti, kad ENO1 gali būti potencialus tikslinis kurkumino genas, o jo priešvėžiniai mechanizmai gali būti susiję su glikolitiniais ir apoptotiniais keliais [137]. Šias išvadas patvirtino naujausi tyrimų duomenys, rodantys, kad ir nanomicelių kurkuminas, ir kurkuminas kartu su Erlotinibu sumažina žmogaus glioblastomos ląstelių U87 gyvybingumą, migraciją ir invaziją in vitro. Tiek invazija, tiek migracija atlieka svarbų vaidmenį vėžio metastazėse. Įdomu tai, kad U87 žmogaus glioblastomos ląstelėse su angiogeneze susijusių veiksnių, įskaitant VEGF, HIF-1, bFGF ir Cox-2, ekspresija buvo žymiai sumažinta. Kita vertus, kurkuminas vienas arba kartu su erlotinibu padidino su autofagija susijusių baltymų (LC3-I, LC3-I ir Beclin1) ekspresiją ir moduliavo proapoptotinių faktorių ekspresiją. Bax, kaspazė 8 ir Bcl-2 su priešuždegiminiu NF-kB (žr. 2 pav.) [138].
Be to, kurkuminas žymiai sumažino genų, susijusių su Wnt keliais, tokių kaip ciklinas D1, ZEB1, -kateninas ir Twist, ekspresiją [139]. Įrodyta, kad molekuliniu lygiu kurkuminas slopina GBM ląstelių proliferaciją per AKT / mTOR signalizacijos kelią ir padidina PTEN ekspresiją. Šio tyrimo in vitro eksperimentai nuosekliai patvirtino, kad kurkuminas slopina U251 ląstelių, gautų iš žmogaus piktybinės daugiaformės glioblastomos, migraciją ir invaziją ir stimuliuoja apoptozę [140].
Siekiant pagerinti BBB įsiskverbimą ir veiksmingą intracefalinį vaistų išsiskyrimą bei pateikti veiksmingus, tikslinius GBM terapinius agentus, buvo pasiūlyti įvairūs metodai. Taikant šiuos metodus, kurkuminas buvo kapsuliuotas į ketvirtos kartos paviršiaus modifikuotą poliamidoamino (PAMAM) dendrimerį. Pažymėtina, kad in vitro naudojant inkapsuliuotą kurkuminą terapinėmis dozėmis, labai sumažėjo įvairių glioblastomos ląstelių iš trijų skirtingų rūšių (U98, F98 ir GL261) gyvybingumas[141]. Yra žinoma, kad vėžinėms ląstelėms reikalinga didelė oksidacinė būsena, kad išlaikytų jų augimą ir dauginimąsi. Kaip aprašyta aukščiau, kurkuminas yra maistinis junginys, žinomas dėl savo priešuždegiminio ir antioksidacinio poveikio, todėl gali būti naujas alternatyvus potencialus kandidatas niokojančio GBM gydymui. Tačiau kurkumino potencialo GBM įvertinimas yra susijęs su kitais esamais gydymo būdais, tačiau ateityje reikia atlikti in vivo tyrimą su graužikų glioblastomos modeliais. Siekiant pagerinti BBB įsiskverbimą ir pasiekti efektyvų vaistų tiekimą į pelių glioblastomą, buvo panaudota pasiutligės viruso glikoproteino polipeptido darinio (RVG) peptidas, nukreiptas į doksorubiciną ir kurkuminu padedamas redukcijos jautrumo nanomicelės (DOX/RVG-CSC). Tinkamas kurkumino tiekimas skatina bendrą mikroglijos repoliarizaciją, o tai savo ruožtu stimuliuoja GBM ląstelių transformaciją iš imunosupresinės būsenos M2 į jautrų fenotipą M1[142]. Dėl unikalaus mikroaplinkos suderinamumo ir afiniteto intracerebrinėms gliomoms, chondroitino sulfatas (CHS) buvo naudojamas kaip hidrofilinis segmentas [143] ir disulfidiniais ryšiais konjuguotas su kurkuminu. Dėl to vandenyje spontaniškai susirinko šerdies ir apvalkalo polimerinės micelės. RVG tarpininkaujantis DOX / RVG-CSC prasiskverbia į BBB, pasiekia tikslines naviko ląstelės sritis ir po to, stimuliuojant didele glutationo koncentracija GBM, išskiria aktyvųjį vaistą [144]. Be to, naujausi rezultatai rodo, kad kurkuminas gali atlikti esminį vaidmenį pašalinant likusias GMB ląsteles stimuliuodamas imuninę sistemą [145,146].
Šis naujas kurkumino vaidmuo GBM kontekste buvo ištirtas atliekant daugybę mechaninių tyrimų, atliktų GBM pelių modeliuose. Visai neseniai Baidoo ir kt. ištyrė įgimtos imuninės sistemos panaudojimą terapiniam požiūriui į vėžio ląstelių pašalinimą. Jie išsiaiškino, kad navikai savo nišose turi makrofagų ir mikroglijų, bet dažniausiai auglį skatinančio M2 būsenoje, kontroliuojant naviko išskiriamus citokinus. Ryškiausias jų rezultatų atradimas yra tas, kad kurkuminas sukėlė su naviku susijusių makrofagų (TAM) repoliarizaciją į azoto oksidą (NO) gaminantį navikams naikinantį M1 fenotipą. Šis M2→M1 jungiklis apėmė kurkumino sukeltą STAT-3 slopinimą ir STAT-1 indukciją bei aktyvavimą. Tai įdarbina aktyvuotas natūralias žudikas ląsteles (NK) ir citotoksinį T (Tc) į naviką ir dėl to pašalina vėžio ląsteles ir vėžio kamienines ląsteles. Iš esmės šis metodas gali būti bendra kovos su GBM strategija, tačiau reikia atlikti daugiau tyrimų, kad būtų galima geriau suprasti įvairių susijusių veiksnių poveikį kurkumino ir priešvėžiniams keliams [147-150]. Be to, tai atvėrė galimybę atlikti I / II fazės klinikinį tyrimą su GBM pacientais, siekiant ištirti jų kurkumino terapijos veiksmingumą skatinant TAM repoliarizaciją.
Apibendrinant, kurkuminas gali moduliuoti su GBM susijusius kelius. Pavyzdžiui, kurkuminas slopina naviko augimą blokuodamas naviko augimą skatinančius kelius NF-kB, PI3k/Akt/žinduolių taikinį rapamicinu (PI3K/Akt/mTOR), Janus kinazės/signalų keitiklius ir transkripcijos aktyvatorius (JAK/STAT3) ir mitogeną. -aktyvuoti baltymų kinazės keliai, o pagrindiniai naviko slopinimo genai (ty p53 ir p21 ir kaspazė) buvo reguliuojami [151].
Remiantis visais in vitro kurkumino radiniais, buvo pranešta apie kitus naudingus kurkumino poveikius GBM in vivo (S1 lentelė), įskaitant nuo matricos metaloproteinazių (MMP) priklausomos ląstelių migracijos ir invazinės ląstelių proliferacijos slopinimą, dėl kurio vėliau atsirado sumažėjęs naviko tūris ir tuo pačiu ilgesnis išgyvenimo laikas[137].
Visi aptarti kurkumino efektai rodo, kad glioblastomos ląstelių funkcijos / veikla yra moduliuojamos, o jų progresavimas yra atidėtas (1 pav.). Tačiau glioblastomos navikų genomo profiliavimas ir specifinių kurkumino taikinių nustatymas GBM gydymui išlieka svarbūs norint suprasti jo farmakologinius mechanizmus ir, dar svarbiau, gali suteikti teorinį pagrindą racionaliam kurkumino naudojimui klinikinėje praktikoje. Reikėtų apsvarstyti tolesnius tyrimus, kad būtų parengta galutinė įtikinama ataskaita apie kurkumino gydomąjį poveikį klinikinėje praktikoje atskirai arba kartu su vaistiniais preparatais. Reikia tolesnio tyrimo dėl galimo netiesioginio poveikio smegenų sveikatai ir glioblastomos prevencijai per žarnyno ir smegenų ašį.
6. Kurkuminas ir epilepsija
CNS ligos šiuo metu yra didelė socialinė ir individuali problema. Visų pirma, naujausi epidemiologiniai duomenys rodo, kad epilepsija yra vis labiau paplitusi ligų grupė visame pasaulyje. Dėl šios priežasties bėgant metams buvo sukurta vis daugiau vaistų ir terapijos būdų, padedančių neutralizuoti epilepsijos priepuolių simptomus ir dažnumą; tačiau įrodyta, kad daugelis šių vaistų yra veiksmingi, tačiau jie taip pat sukelia rimtą ir dažną šalutinį poveikį. Tiesą sakant, pastaruoju metu buvo ištirta daug vaistinių augalų, o kurkuminas yra vienas iš jų. Atrodo, kad kurkuminas vaidina svarbų vaidmenį reguliuojant smegenų monoamino kiekį ir tai rodo galimą apsauginį poveikį priepuolių kontrolei ir pažinimo sutrikimams (ypač atminties sutrikimams). Nustatyta, kad kurkuminas turi 10 kartų stipresnį antioksidacinį poveikį nei vitaminas E ir yra tinkama alternatyva pačiam vitaminui E [152].
Kurkuminas iš tiesų gali slopinti NF-kB tarpininkaujamą transkripciją, uždegiminius citokinus, indukuojamus iNOS ir Cox{1}}, todėl pasižymi antioksidacinėmis ir priešuždegiminėmis savybėmis[153]. Šios savybės rodo jo vaidmenį neuroprotekcijoje ir neuromoduliacijoje aprašytuose epileptogenezės procesuose (S1 lentelė) (1 pav.).
Antiepilepsinis kurkumino poveikis taip pat gali būti pasiektas suaktyvinant priešuždegiminius genus, tokius kaip interleukino -10 receptorių subvieneto beta genas ir chemokino ligandas16 (CXCL16), CXCL17 ir NCSTN[154]. Naujausi ikiklinikiniai tyrimai parodė, kad kurkuminas gali atlikti naudingą vaidmenį gydant epilepsiją ir su ja susijusius sutrikimus, nesukeldamas šalutinio poveikio ar neigiamo poveikio [155, 156]. Kai kurie eksperimentiniai tyrimai, pagrįsti sukeltos epilepsijos modeliu, pranešė apie kurkumino veiksmingumą atitolinant arba visiškai slopinant priepuolių pradžią [157].
Taip pat buvo pasiūlyta, kad kurkuminas vaidina svarbų vaidmenį nustatant kai kurių kanalų baltymų (CACNA1A ir GABRD) sumažėjimą, dėl kurio vėliau slopinami FeClg sukelti traukuliai (2 pav.). Vartojant kurkuminą, atkuriami žmogaus potrauminės epilepsijos modeliai [158]. Mikronizuotas kurkuminas veiksmingumui, panašus į antiepilepsinio vaisto valproatą, slopina toninius-kloninius traukulius PTZ sukeltuose epilepsijos modeliuose tiek lervoms, tiek suaugusiems zebrafiniams žuvims [159]. Kito tyrimo metu buvo įvertintas kurkumino priešuždegiminis ir prieštraukulinis poveikis po didelių FeCl dozių; vartojamas kartu su dieta ir išmatuotas milijoninėmis dalimis (1500 ppm), buvo geresnis veiksmingumas slopinant generalizuotus priepuolius, palyginti su mažomis dozėmis (500 ppm)[160].
Didėjančios įtampos elektrošoko testo su pelėmis modelyje 100 mg/kg per burną vartojamas kurkuminas padidino priepuolių slenkstį tiek sergant ūmine, tiek su lėtine epilepsija (21 dienai) [161]. Šis poveikis panašus į fenitoino (25 mg/kg PO) vartojimą[161]. Šiame tyrime nustatytas mirtingumo sumažėjimas net ir chroniškai vartojant kurkuminą, paaiškinant šios medžiagos prieštraukulinį poveikį. Tolesni ikiklinikiniai tyrimai patvirtino jo prieštraukulinį ir priešuždegiminį poveikį. Be to, buvo nustatyta, kad kurkuminas atlieka apsauginį vaidmenį stabdant įvairius oksidacinio streso pokyčius, susijusius su pilokarpino stimuliacija [162]. Šiuos duomenis taip pat patvirtino kitas tyrimas, kurio metu buvo įvertintos 10–300 mg/kg kurkumino dozės, kurios buvo naudingos mažinant pilokarpino sukeltus traukulius [163].
Kurkuminas taip pat parodė savo poveikį sergant epilepsija. Iš tiesų, Gupta ir kt.[164] atliktas tyrimas numatė, kad kurkumino dozė yra 50-200mg/kg maždaug 30 minučių prieš stimuliavimą kaino rūgštimi. Šio tyrimo autoriai pastebėjo apsauginį kurkumino poveikį didinant priepuolių pradžios latentiškumą, kai buvo vartojama 100–200 mg/kg dozės. Toje pačioje grupėje statistiškai reikšmingai sumažėjo priepuolių dažnis [164]. Mažesnės dozės neparodė klinikinio veiksmingumo. Tada gyvūnų smegenų analizė parodė, kaip ilgai trunkantys priepuoliai padidino MDA ir sumažino glutationo kiekį. Šį poveikį galima pakeisti tik vartojant 100 ir 200 mg/kg kurkumino dozes. Mažesnės dozės nebuvo kliniškai naudingos [164].
Taip pat įrodyta, kad kurkuminas veiksmingai mažina pažinimo nuosmukį ir oksidacinį stresą, kurį sukelia nuolatinis vaistų nuo epilepsijos, tokių kaip fenobarbitalis ir karbamazepinas, kurie plačiai naudojami klinikinėje praktikoje, vartojimo [165].
Be to, kurkumino veiksmingumas gydant su epilepsija susijusius sutrikimus taip pat buvo patvirtintas tyrimais su Wistar žiurkių patinais PTZ sukeltu metodu. Šiame tyrime vartojant 300 mg/kg kurkumino, pagerėjo PTZ sukeltų traukulių atsiradimas, sumažėjo oksidacinis stresas ir sumažėjo pažinimo funkcijos [165].
Kaip žinoma, lėtinis kai kurių vaistų nuo epilepsijos, tokių kaip karbamazepinas ir fenobarbitalis, vartojimas gali sukelti pažinimo nuosmukį, kurį, kaip manoma, sukelia oksidacinis stresas. Nustatyta, kad kurkuminas, vartojamas kartu su šiais vaistais nuo epilepsijos, panaikina šį pažinimo pablogėjimą ir oksidacinio streso parametrus [165].
Kiti tyrimai, tiriantys kurkumino veiksmingumą gydant neurologinius ir psichikos sutrikimus, įskaitant pažinimo nuosmukį, parodė, kad pelėms, kurios vartojo kurkuminą, pažinimo funkcijos pablogėjimo nepastebėta, palyginti su pelių, kurios vartojo fenitoiną, pažinimo pablogėjimo [166]. Piperino injekcija kartu su kurkuminu gali pagerinti jo biologinį prieinamumą ir dar labiau sustiprinti jo antiepilepsinį poveikį [167].
Šie tyrimai yra labai vilčių teikiantys ir yra būsimų tyrimų pagrindas, nepaisant to, kad yra apribojimų, susijusių su sudėtingu žmogaus epileptogeninių tinklų atkuriamumu, pradedant nuo eksperimentiniais modeliais, ir su sunkumais paverčiant eksperimentiniuose modeliuose vartojamas dozes į dozes žmonėms.
7. Išvados
Natūralus junginys kurkuminas pasižymi antioksidacinėmis ir priešuždegiminėmis savybėmis bei apsauginiu poveikiu, veikdamas įvairiuose ląstelių keliuose. Šioje apžvalgoje mes sutelkėme dėmesį į terapinį kurkumino poveikį neurodegeneraciniams sutrikimams, tokiems kaip AD, PD, MS, glioblastoma ir epilepsija, moduliuodami įvairius molekulinius kelius smegenų ląstelėse (žr. S1 lentelę ir 2 paveikslą). Ekstraląstelinės pūslelės arba nanovezikulės gali pagerinti kurkumino tirpumą ir biologinį prieinamumą smegenyse, tačiau iki šiol šių naujų kurkumino pristatymo būdų taikymas neurodegeneracinėse ligose nebuvo iki galo ištirtas. Todėl daugiau tyrimų naudojant šias terapines biomolekules gali duoti teigiamą neuroprotekcijos rezultatą. Šie nauji tyrimai gali būti orientuoti į (1) vaistų tiekimo sistemų tobulinimą, siekiant padidinti kurkumino biologinį prieinamumą ir BBB pralaidumą; (2) tolesnius klinikinius tyrimus, siekiant nustatyti veiksmingesnę šių biomolekulių, pernešančių kurkuminą, dozę neurodegeneraciniams sutrikimams gydyti (3); ) tiriant signalizacijos kelius, kuriuos terapinės biomolekulės naudoja neuroprotekcijai sukelti. Šioje apžvalgoje aprašyti rezultatai teikia vilčių, tačiau reikalingi tolesni tyrimai, siekiant optimizuoti kurkumino naudojimą neurodegeneracinių ligų profilaktikai ir gydymui.
Šis straipsnis ištrauktas iš Molecules 2022, 27, 236. https://doi.org/10.3390/molecules27010236 https://www.mdpi.com/journal/molecules
