Nukleino rūgštimis pagrįstos vakcinų platformos nuo 19 koronavirusinės ligos (COVID-19)
Aug 11, 2023
Abstraktus
2019 m. koronaviruso ligos (COVID{1}}) pandemija iki šios dienos visame pasaulyje užkrėtė 673 010 496 pacientus ir sukėlė 6 854 959 atvejų mirtį. Didžiulės pastangos buvo dedamos kuriant iš esmės skirtingas COVID{8}} vakcinos platformas. Nukleino rūgščių pagrindu pagamintos vakcinos, sudarytos iš mRNR ir DNR vakcinų (trečiosios kartos vakcinos), buvo daug žadančios dėl greito ir patogios gamybos bei veiksmingo imuninio atsako prieš COVID išprovokavimo{11}}. Keletas DNR pagrįstų (ZyCoV-D, INO-4800, AG0302-COVID19 ir GX-19N) ir mRNR (BNT162b2, mRNR-1273 ir ARCoV) COVID{22}} prevencijai buvo naudojamos patvirtintos vakcinų platformos. mRNR vakcinos yra visų COVID-19 prevencijos platformų priešakyje. Tačiau šių vakcinų stabilumas yra mažesnis, o DNR vakcinos reikalingos didesnėmis dozėmis, kad paskatintų imuninį atsaką. Nukleino rūgščių pagrindu pagamintų vakcinų tiekimas į ląstelę ir jų nepageidaujami reiškiniai reikalauja tolesnių tyrimų. Atsižvelgiant į tai, kad vėl atsiranda susirūpinimą keliančių COVID{26}} variantų, vakcinų pakartotinis įvertinimas ir daugiavalenčių vakcinų arba pankoronaviruso strategijų kūrimas yra būtini veiksmingai infekcijų prevencijai.

cistanche papildo privalumai – kaip stiprinti imuninę sistemą
Spustelėkite čia norėdami pamatyti Cistanche Enhance Immunity produktus
【Klauskite daugiau】 El. paštas:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Raktažodžiai
Koronavirusinė liga 19 · Nukleino rūgščių bazės vakcinos · Imunitetas · Apsauga
Fonas
2019 m. pabaigoje Kinijoje, Uhane, atsirado naujas beta koronavirusas, kuris greitai išplito visame pasaulyje. 2019 m. koronavirusinė liga (COVID-19) turi didelį pandemijos potencialą dėl didelio užkrečiamumo lygio ir didelio mirtingumo visame pasaulyje (Sharma ir kt., 2020; Su ir kt., 2020; Wibawa, 2021). Todėl reikia dėti daug pastangų kuriant veiksmingas vakcinas ar gydymo būdus nuo šios ligos (Su ir kt., 2020). COVID-19 ligos simptomai skiriasi, įskaitant lengvus į fu panašius simptomus, pneumoniją, ūminį kvėpavimo distreso sindromą (ARDS) ir mirtiną baigtį. Pacientams, sergantiems vėžiu, diabetu, širdies ir kraujagyslių ligomis, vyresnio amžiaus žmonėms ir net genetiškai linkusiems asmenims, kyla didžiausia rizika susirgti COVID-19 sunkumu (Sharma ir kt., 2020; Su ir kt., 2020; Wibawa 2021; Vakil ir kt.). 2022). Remiantis Pasaulio sveikatos organizacijos (PSO) rekomendacijomis, kaukių dėvėjimas, antivirusinių vaistų vartojimas, socialinis atsiribojimas ir skiepijimo procedūrų laikymasis yra esminis elgesys siekiant kontroliuoti COVID{14}} pandemiją visame pasaulyje (Sharma ir kt., 2020). Mokslinės pastangos kuriant veiksmingas vakcinas nuo invazinių patogenų datuojamos jau daug metų (Deb ir kt., 2020; Zhang ir kt., 2020; Wibawa 2021). Šios vakcinos platformos taip pat buvo sukurtos nuo patogeninių bakterijų (Farhani ir kt., 2019; Jafari ir Mahmoodi, 2021). Šiuo atžvilgiu veiksmingos, apsauginės ir saugios vakcinos sukūrimas laikomas pagrindiniu prevenciniu metodu, siekiant užkirsti kelią sunkaus ūminio kvėpavimo sindromo koronaviruso 2 (SARS-CoV-2) plitimui (Moore ir Klasse 2020). Todėl įvairios farmacijos įmonės ir tyrimų komandos visame pasaulyje varžėsi, siekdamos pristatyti saugią ir veiksmingą vakciną nuo COVID-19, skirtą naudoti tarptautinėje bendruomenėje. Šios pastangos sukūrė kitas vakcinų platformas, skirtas ikiklinikiniams ir klinikiniams tyrimams pradėti, o kai kurios iš jų buvo patvirtintos (Chen ir kt., 2021), įskaitant tradicines vakcinas, tokias kaip gyvos arba inaktyvuotos, subvieneto ir nukleorūgščių pagrindu pagamintos vakcinos kaip naujos kartos vakcinos. (Moore ir Klasse 2020). Remiantis moksliniais įrodymais, gyvos susilpnintos vakcinos stimuliuoja įgimtą, ląstelinį ir humoralinį imuninį atsaką, sukeldamos į rinkliavą panašius receptorius (TLR), sukeldamos ilgalaikį imunitetą ir gali sukelti padidėjusį jautrumą. Pagrindinis šių vakcinų trūkumas yra brangus jų saugumo ir veiksmingumo vertinimas. Inaktyvuotos virusinės vakcinos silpnai išprovokuoja ląstelinį imuninį atsaką, o tai sumažina jų veiksmingumą. 2020 m. balandžio mėn. Sinovac ir Wuhan biologinių produktų institutas (Sinopharm) pagamino inaktyvuotą COVID-19 vakciną (Moore ir Klasse 2020; Su ir kt., 2020). Subvienetinės vakcinos yra saugios, turi tam tikrų trūkumų, įskaitant mažą imunogeniškumą, revakcinacijos ar adjuvanto poreikį ir didelę kainą (Koirala ir kt., 2020; Su ir kt., 2020). Nukleino rūgšties pagrindu pagamintos vakcinos buvo sukurtos remiantis sekų informacija. Jie apima antigenų DNR arba mRNR sekas, kurios įvairiomis dozėmis stipriai stimuliuoja ląstelinį ir humoralinį imuninį atsaką. Dėl savo pranašumų, pvz., greitos gamybos ir ankstyviausių COVID{40}} vakcinų klinikiniuose tyrimuose, pastebimas DNR pagrįstų vakcinų pranašumas yra jų stabilumas įvairiomis laikymo sąlygomis (Silveira ir kt., 2020 m.; van Riel ir de. 2020 m.). RNR pagrindu pagamintos vakcinos sulaukė daugiau farmacijos kompanijų, tokių kaip Pfizer/Biotech ir Moderna, dėmesio. Priešingai nei DNR vakcinos, jos stimuliuoja veiksmingą humoralinį imuninį atsaką kaip TLR ligandai be adjuvanto, o jų seka modifikuojama, kad būtų išvengta mRNR degradacijos (Moore ir Klasse 2020; van Riel ir de Wit 2020; Soiza ir kt., 2021). Šios apžvalgos tikslas – įvertinti naujausius nukleino rūgščių pagrindu pagamintų vakcinų, įskaitant mRNR ir DNR vakcinas nuo COVID, pokyčius-19.
Pagrindinis tekstas
Koronaviruso molekulinis infekcijos mechanizmas ir imuninis atsakas

cistanche augalą stiprinanti imuninė sistema
COVID{0}} genomas yra teigiama vienos grandinės RNR, koduojanti keturis pagrindinius struktūrinius baltymus, susidedančius iš apvalkalo (E), smaigalio (S), membranos (M) ir nukleokapsidės (N) (Stadler ir Rappuoli 2005), kaip parodyta 1a pav. Žmogaus SARS-CoV kaip apvalkalo dalį apima smaigalys (S) glikoproteinas. Virusą į ląsteles-šeimininkus įtraukia smaigalio baltymas, kurį sudaro S1 ir S2 subvienetai. Jie vaidina esminį vaidmenį prisijungiant prie ląstelės šeimininkės receptorių, žinomų kaip angiotenziną konvertuojantis fermentas II (ACE2), kad sukeltų infekciją (1b pav.). Centrinis S1 domeno regionas, jungiantis su ACE2 dideliu afinitetu, yra receptorius surišantis domenas (RBD). Šiuo atžvilgiu UBR ir ACE2 sąveika reikalinga žmogaus ląstelių infekcijai inicijuoti (He ir kt., 2020). Be to, S baltymo sutrumpinimas yra būtinas viruso patekimui į šeimininko ląsteles; po UBR regiono prijungimo prie ACE2, šeimininko proteazė, žinoma kaip TM proteazės serinas 2 (TMPRSS2), suskaido S baltymą į S1 ir S2 domenus, dėl kurių S2 domenas susilieja su ląstele šeimininke (Huang ir kt., 2020). Nors stiprus imuninis atsakas yra veiksmingas prieš COVID-19, padidėjusį jautrumą ir citokinų audrą (daugiausia interleukiną-6-, IL-1b, GM-CSF-, interferoną-/IFN-, nekrozės faktorių / TNF -, IL-10-, IL-2- ir IL- 7-pagrįsti atsakymai) turi būti uždrausti (Chowdhury ir kt., 2020). Po viruso prisitvirtinimo (smaigalio ir ACE2 sąveikos) ir patekimo į kvėpavimo ląsteles, fagocitiniai alveolių makrofagai ir dendritinės ląstelės (DC) pateikia viruso antigenus T ląstelėms ir suaktyvina T CD4+(pagalbinę T ląstelę) ir T CD{{37 }}(citotoksinė T ląstelė). Vėliau, norint susidurti su virusu, išsiskiria priešuždegiminiai citokinai, tokie kaip IL6, IL12, TNF ir IFN ir kt. Tačiau didelis citokinų gamybos lygis, sukeliantis citokinų audrą, sukelia plaučių pažeidimus (Hosseini ir kt., 2020). Remiantis moksliniais įrodymais, pagalbinės T ląstelės yra būtinos virusinei infekcijai pašalinti, B ląstelėms skatinti gaminti antikūnus ir stimuliuoti citotoksines T ląsteles (Sharma ir kt., 2020). COVID-19 antigeniniai taikiniai Kuriant saugią ir apsauginę vakciną nuo patogeninio organizmo, labai svarbu nustatyti geriausius imunogeninius taikinius (Lu et al. 2020b). Galimų antigeninių taikinių priėmimas yra labai svarbus norint išprovokuoti T ląstelių ir B ląstelių epitopus, kad jie tinkamai sukeltų ląstelinį ir humoralinį imunitetą (Rueckert ir Guzmán 2012). Viruso S baltymas sąveikauja su šeimininko ląstelėmis per UBR domeną kaip esminis ligandas. UBR domenas gali sukelti neutralizuojančių antikūnų gamybą ir T ląstelių imuninį atsaką prieš COVID-19. Taip pat patvirtintas S baltymo imunogeniškumas (Pushparajah ir kt., 2021). N baltymas turi mažą ir labai konservuotą seką, palyginti su kitais viruso baltymais. N baltymas yra labai išreikštas virusinės infekcijos metu, o pacientų humoralinis imuninis atsakas prieš COVID{48}} yra labai didelis. Be to, atsižvelgiant į ląstelių atsaką į N baltymą, jis gali būti laikomas tinkamu kandidatu į vakcinos antigeną (Dutta ir kt., 2020). Be to, M baltymas ir E baltymas stimuliuoja T CD{50}}epitopus (Wang ir kt., 2005; Abdelmageed ir kt., 2020; Dong ir kt., 2020). Stipraus imuninio atsako prieš S baltymą sukėlimas yra lemiamas ir būtinas (Buchholz ir kt., 2004). S baltymas apima imunogeniškiausius T ląstelių ir B ląstelių epitopus, žinomus kaip pageidaujami taikiniai kuriant vakciną nuo COVID{55}}. Jis buvo pritaikytas visose sukurtose mRNR platformos vakcinose, tokiose kaip Pfizer/BioNtech ir Moderna vakcinos.

1a pav. SARS-CoV-2 viriono struktūra; pagrindiniai COVID-19 viruso paviršiaus baltymai yra Spike (S) glikoproteinas, Membran (M) ir Envelope (E) baltymai. S baltymas yra pagrindinė vakcina ir terapinis taikinys, kuris sąveikauja su angiotenziną konvertuojančio fermento II (ACE2) receptoriumi, kad sukeltų infekciją. b Smailių baltymų domenai; S baltymas apima S1 (NTD arba netransliuojamą domeną ir RBD arba receptorių surišantį domeną) ir S2 subvienetus
Nukleino rūgšties pagrindu pagamintų vaistų istorija
Oligonukleotidai buvo įtraukti į klinikinius tyrimus daugiau nei prieš 30 metų. Nukleino rūgštimis pagrįstų terapinių metodų naudojimo istorija siekia 1977 m., kai Paterson ir kt. naudojo nukleino rūgštis genų ekspresijai suderinti (Paterson ir kt., 1977). Šiuo metu jie susilaukė daugiau dėmesio. Nukleino rūgšties pagrindu pagaminti vaistai skirstomi į skirtingas kategorijas, įskaitant antisensines formas, ribozimus, mRNR ir DNR pagrindu sukurtas vakcinas (Sharma ir kt., 2014). Sintetinis oligodeoksinukleotidas slopino Rouso sarkomos viruso (RSV), kuris buvo papildomas RSV mRNR ir buvo žinomas kaip antisensas, replikaciją (Zamecnik ir Stephenson 1978). Pirmasis antisensas buvo įvestas į kliniką prieš citomegalovirusą (CMV) (Mulamba ir kt., 1998). Maža trukdanti RNR (siRNR) gali slopinti genų ekspresiją ir pirmą kartą apie ją pranešta 1998 m. Kita mažų nekoduojančių RNR grupė apima mikroRNR (miRNR), kurios atlieka nepakeičiamą vaidmenį reguliuojant genų ekspresiją. funkcijos panašios į siRNR ir terapinis potencialas (Usman ir Blatt 2000; Sharma ir kt. 2014). Kaip minėta, RNR molekulių ribozimų klasė veikia kaip fermentai, nukreipti į transkripciją. Ribozimai dalyvavo klinikiniuose tyrimuose prieš vėžį ir kai kurias virusines infekcijas, tokias kaip žmogaus imunodeficito virusas (ŽIV) (Usman ir Blatt 2000; Abera ir kt., 2012). Be mRNR ir DNR pagrįstų vakcinų, jos priskiriamos nukleino rūgščių pagrindu pagamintiems vaistams, pristatytiems 1990 m. ir jiems buvo skiriama daugiau dėmesio kuriant vakcinas, skirtas kovai su COVID{19}} (Le et al. 2020; Zhang ir kt. . 2020). Pagrindiniai šių vakcinų grupių pranašumai yra greita jų gamyba ir didelis specifiškumas atitinkamiems tiksliniams antigenams (Le et al. 2020).

cistanche tubulosa - stiprina imuninę sistemą
mRNR pagrindu pagamintos vakcinos
Pradinis mRNR molekulių pristatymas į šeimininko ląsteles apėmė mRNR transfekciją į fibroblastų ląsteles naudojant katijoninį lipidą (Park ir kt., 2021). mRNR vakcinos apima patogenų antigenus mRNR, kurie žmogaus ląstelėse gamina antigeninius baltymus. Keletas mRNR vakcinų pranašumų yra paprastas gamybos procesas, efektyvus ir apsauginis imunitetas, patogus manipuliavimas ir industrializacija bei lankstumas reaguojant į COVID-19 variantus (Kaufman ir kt., 2016; Fang ir kt., 2022). Kai kurie metodai, pvz., 5ʹ-cap ir Kozak sekų pridėjimas, yra taikomi naudojant 3ʹ-poli-A sekas ir modifikuojant mRNR nukleozidus (Borah ir kt., 2021). MRNR vakcinos yra verčiamos į šeimininko citozolį. Todėl nėra jokios rizikos įterpti šeimininko genomus, o tai yra žinoma kaip pagrindinis jų pranašumas. Šiuo atžvilgiu pastaruoju metu daugiau dėmesio buvo skiriama mRNR pagrįstoms vakcinoms kaip saugiai profilaktikai nuo vėžio ir infekcinių ligų (Kaur ir Gupta 2020). Pirminis mRNR vakcinų veikimo mechanizmas pavaizduotas 2 pav.
DNR pagrįstos vakcinos
DNR vakcinos apima keletą genų, koduojančių virusinius antigeninius peptidus, ekspresuojamus plazmidiniais vektoriais ir perduodamus ląstelėms elektroporacijos (EP) būdu. Palyginti su kitomis vakcinų platformomis, DNR vakcinos siūlo lanksčią ir greitą vakcinų kūrimo platformą, todėl tai yra patraukli technologija kovojant su besivystančiomis epidemijomis, tokiomis kaip COVID{0}}. Be to, DNR vakcinos antigeno gamyba vyksta tikslinėse ląstelėse, o tai padeda apibendrinti natūralią viruso antigeno konformaciją ir potransliacinę modifikaciją. Pagrindinis DNR vakcinų trūkumas yra ribotas jų imunogeniškumas. Todėl svarbu apsvarstyti tokias strategijas kaip adjuvantas arba pirminio padidinimo režimo naudojimas, kuris galėtų padidinti DNR vakcinos potencialą. Be to, nukleino rūgšties integravimas į šeimininko DNR yra dar vienas susirūpinimas dėl biologinės saugos, sukeliantis onkogenezę ir mutagenezę (Rauch ir kt., 2018). Nors remiantis ankstesniais tyrimais, DNR vakcinos įterpimo rizika yra nereikšminga, PSO ir FDA rekomenduoja įdiegti DNR vakcinos saugumą integruojant (Wang ir kt., 2004; Schalk ir kt., 2006). DNR vakcinos perkelia koronaviruso genus į žmogaus ląsteles. Vakcinacijos principas priklauso nuo DNR patekimo į ląstelės branduolį taip, kad pradedama antigeno transkripcija, o po to - transliacija. DNR vakcinose kaip vektoriai dažniausiai naudojamos plazmidės. Atsižvelgiant į vakcinos įvedimo būdą, sprendžiami ir miocitai, ir keratinocitai. Tačiau antigeną pristatančios ląstelės netoli injekcijos vietos taip pat gali būti tiesiogiai transfekuotos naudojant DNR vakcinas. Tokiais atvejais kryžminio pradėjimo procesas atspindi antigenus, naudojant abi pagrindines histokompatibilumo komplekso (MHC-I/II) molekules (Hobernik ir Bros 2018). Sukurti antigenai išskiriami naudojant apoptotinius kūnus arba egzosomas, dėl kurių juos atpažįsta antigeną pateikiančios ląstelės, kurios savo ruožtu išprovokuoja ląstelinį ir humoralinį imuninį atsaką. Siekiant sukurti stiprų imuninį atsaką, naudojamos įvairios pristatymo strategijos (Donnelly ir kt., 2005; Li ir Petrovsky, 2016; Strizova ir kt., 2021). Kalbant apie imuninį reguliavimą COVID{14}} infekcijos metu, buvo atskleista, kad pacientams, kuriems gresia perikardo efuzija ir klaidinga prognozė, yra padidėjęs CD3+CD8+ T ląstelių kiekis ir sumažėjęs CD{{ 18}}HLA-DR ir T reguliuojančios (Treg) ląstelės (Duerr ir kt., 2020). Šie rezultatai rodo, kad sunki infekcija atsiranda dėl nesubalansuoto imuninio atsako, kuris pablogina ligos sąlygas (Tay ir kt., 2020). COVID-19 vakcinos pažangos tikslas buvo sukurti veiksmingą ir tinkamą imuninį atsaką (įskaitant abi rankas), nesukeliant pažangos iki tokio disbalanso (Hobernik ir Bros, 2018). Nors klinikiniai DNR vakcinų tyrimai su žmonėmis sukėlė bendrą atsaką, šie atsakai dažnai yra nepakankami, kad būtų galima gauti priimtinus klinikinius pranašumus. Be to, pagrindiniai plazmidinės DNR komponentai, pavyzdžiui, nemetilintos CpG sekos, gali sukelti įgimtų imuninių atsakų aktyvavimą, padidindami adaptyvų imuninį atsaką prieš išreikštus antigenus. Taigi, DNR vakcinos labiau pritaikomos veterinarijoje (Coban ir kt. 2013; Silveira ir kt. 2017; Hobernik ir Bros 2018). Dėl šio trūkumo kai kurios tyrimų kryptys daugiausia dėmesio skiria DNR vakcinų optimizavimui ir pristatymui, įskaitant kodonų optimizavimą, promotoriaus dizainą, molekulinius adjuvantus, EP taikymą, pirminę vakcinaciją arba pažangių vakcinų projektavimo „omikos“ metodus (Li ir kt. 2012; Silveira ir kt., 2020). 3 paveiksle pavaizduoti pagrindiniai DNR vakcinos mechanizmų veiksmingo imuninio atsako etapai.

2 pav. mRNR vakcinos formuluotė, skyrimas ir imuninės provokacijos mechanizmai: mRNR kompozicija su lipidų nanodalelėmis (LNP) palaiko ir padidina sekos stabilumą. b MRNR-LNP vakcinos druskos tirpalas suleidžiamas į raumenis. c LNP turinti mRNR endocitozės būdu transfekuojama į antigeną pateikiančias ląsteles (APC). MRNR išskiriama citoplazmoje ir paverčiama virusiniais baltymais, po to juos lizuoja proteasoma ir prisijungia prie pagrindinio histokompatibilumo komplekso I (MHC-I) ant endoplazminio tinklo paviršiaus ir pateikia T citotoksinėms (Tc) ląstelėms.
MRNR ir DNR pagrįstų vakcinų potencialas
MRNR lygio vakcinos struktūroje yra elementų, skirtų stabilumui ir baltymų ekspresijai atkurti, įskaitant 3′ UTR, kodavimo seką, 5′UTR, 5′ dangtelį ir poli (A) uodegą (Liu 2019). 5′ ir 3′ UTR elementai, besiribojantys su koduojančia seka, gauta iš virusinių arba eukariotinių genų, padidina struktūrinį stabilumą ir pagerina mRNR transliaciją, o tai yra esminiai veiksniai vakcinoms (Ross ir Sullivan 1985; Holtkamp ir kt., 2006). Norint efektyviai perkelti baltymus iš mRNR, reikalinga 5′ dangtelio struktūra (Martin ir kt., 1975; Ross ir Sullivan 1985). MRNR poli (A) uodega taip pat turi reguliuojantį vaidmenį mRNR stabilumui ir transliacijai (Holtkamp ir kt., 2006). Be to, kodono naudojimas turi gyvybiškai svarbų vaidmenį baltymų vertime. Šiuo atžvilgiu, siekiant padidinti baltymų transliaciją iš mRNR, reti kodonai pakeičiami naudojamais sinoniminiais kodonais, kurių citozolyje yra daug giminingų tRNR (Stepinski ir kt., 2001). Kitas sekos optimizavimo būdas yra G: C turinio praturtinimas. Pastaraisiais metais keli metodai sukūrė veiksmingas ir saugias kandidatines DNR vakcinas. DNR pagrindu sukurtoje vakcinų platformoje bakterijų kilmės plazmidiniai vektoriai naudojami norimiems antigenams ekspresuoti ląstelėse-šeimininkėse. Bakterijų plazmidės turi būti įvestos į eukariotų ląsteles ir perkeltos į branduolį. Tada DNR transkripuojama ir verčiama iš svetimų genų atitinkamai ląstelės šeimininkės branduolyje ir citoplazmoje. Todėl norint sukurti stiprią DNR vakciną, būtina sukurti tinkamą plazmidę su dideliu transfekcijos efektyvumu ir baltymų ekspresija (Malone ir kt., 1989). Eukariotinės srities seka (DNR vakcinų plazmidėse), esanti prieš įterptą geną, susideda iš promotoriaus ir poli A signalo (poliA) (AAU AAA), esančio 3′ antigeninės sekos galuose (Shan ir kt. . 2011). Promotoriai yra esminiai elementai, reikalingi DNR vakcinos plazmidėse, kad išprovokuotų aukštą norimų antigenų ekspresijos lygį šeimininko ląstelėse (Becker ir kt., 2008) ir lemtų mRNR transkripciją iš įterpto geno. Dažniausiai DNR vakcinose naudojamas promotorius yra žmogaus citomegaloviruso (CMV) promotorius. PoliA sekos signalas efektyviai sukelia mRNR stabilumą ir pernešimą bei eukariotų genų ekspresiją. Kitas svarbus elementas yra Kozako seka (ACCATGG), kuri atlieka gyvybiškai svarbų vaidmenį eukariotinės ribosomos transliacijoje. Be to, norint išvengti neteisingo įterpto geno vertimo į šeimininko ląstelę, būtina pridėti vieną ar dvi stopkodono sekas (Becker ir kt., 2008; Williams, 2013). DNR ir mRNR vakcinų platformų palyginimas Nors DNR ir mRNR vakcinos buvo kuriamos nuo 1990 m. ir neseniai buvo kuriamos bei licencijuojamos įvairios veterinarinės DNR vakcinos, didelis entuziazmas nukrypo į mRNR. Abiem reikia stengtis padidinti savo antigeniškumą, stabilumą ir veiksmingumą manipuliuojant plazmidės DNR ir mRNR tiesiogiai arba pridedant imunomoduliatorių ar adjuvantų ir formulių bei tiekimo sistemų (Liu 2019). MRNR stabilumo trukmė yra mažesnė nei plazmidinės DNR. Buvo išaiškinta, kad DNR vakcinos greitai generuoja užkoduotą baltymą, o jų kiekis yra didesnis nei mRNR vakcinos dėl didesnio vidinio plazmidės DNR stabilumo. Nustatyta, kad plazmidinė DNR raumenyse išlieka iki 6 mėnesių neintegruotu režimu (Ledwith ir kt., 2000). Nors DNR ir mRNR vakcinos turėtų būti mėgstamo baltymo ekspresijos sistema, nė viena iš jų nėra imunologiškai inertiška. Be to, DNR plazmidės ir mRNR stimuliuoja įgimtą imunitetą (Campbell 2017). DNR ir mRNR pagrįsta vakcinų technologija gali būti ne visai bendra. mRNR yra sudėtingesnė nei plazmidinė DNR dėl modifikuotų nukleozidų ir formulių, reikalingų tiekimui, stabilumui ir būtinybei kontroliuoti vidinį mRNR imunostimuliacinį aktyvumą. Nepaisant to, tai naudinga gamybai, kuri vengia kiekvieno ląstelinio ar gyvūninio produkto paklausos. Žadama, kad klinikiniai pasiekimai bus įmanomi po to, kai bus išspręstos plazmidinės DNR ir mRNR vakcinos problemos, ypač taikant pažangias technologijas ligų prevencijai ir gydymui (Liu 2019).

3 pav. COVID-19 DNR vakcinos ekspresijos procesas į antigeną pateikiančias ląsteles (dendritines ląsteles arba DC). Plazmidinė DNR patenka į DC branduolį ir išreiškia antigenus in vivo (1) Tada antigenai pateikiami T ląstelėms (T ląstelių receptoriams arba TCR) per MHC-I ir MHC-II molekules. Antigeno pateikimas vyksta per DC CD80/86 molekules ir CD8+T ląstelių CD28 molekules kartu su MHC-I-TCR, taip pat per DC CD40 ir CD4+T ląstelių CD40L kartu su MHC-II ir TCR sąveika (2a, 3 ir 4) CD8+T ląstelių ir citokinų išsiskyrimo aktyvinimas ir proliferacija sukelia veiksmingą imuninį atsaką, pvz., makrofagų aktyvavimą (2b). Be to, suaktyvėja CD 4+T ląstelės po prisijungimo prie DC ir citokinų poveikio iš jų yra susijusios su B ląstelių aktyvacija, proliferacija ir antikūnų sekrecija (5)
DNR ir mRNR vakcinos pristatymo pažanga
Svetimos DNR ir RNR įsisavinimas eukariotinėse ląstelėse nėra efektyvus, palyginti su virusiniais vektoriais. Buvo sukurta daug fizinio pristatymo būdų, siekiant padidinti ląstelių įsisavinimo pajėgumą (Mellott ir kt., 2013). Fiziniai genų transfekcijos metodai apima tiekimo sistemas, perduodančias genetinę medžiagą mechaninėmis procedūromis, įskaitant EP ir projektoriaus įrenginius (Gulce-Iz ir Saglam-Metiner 2019). Biojektoriaus prietaisai naudoja CO2 slėgį terapiniams preparatams transportuoti per IM (intramuskulinį), ID (intraderminį), o taip pat SC (poodinį) švirkštimą be adatos (Jorritsma ir kt., 2016), o tai suteikia didelių pranašumų, palyginti su įprastine adatine injekcija, įskaitant sušvelninimą. neigiamas poveikis, adatos kryžminė tarša ir adatos dūrio pažeidimai (Zhang ir kt., 2015). Atitinkamai, dvi DNR vakcinos buvo įvertintos nuo Zikos viruso I fazės tyrime, o tai rodo, kad po injekcijos be adatų padidėja ląstelių atsakas, palyginti su adata (Gaudinski ir kt., 2018). Be to, mRNR vakcinos nuo pasiutligės pristatymo platforma naudojant projektorių atskleidė sustiprintus antikūnų atsakus (Alberer ir kt., 2017). Padidėjęs vakcinos veiksmingumas naudojant reaktyvinę injekciją gali būti siejamas su platesniu vakcinų pasiskirstymu, todėl naudojant APC yra didesnis įsisavinimas (Williams ir kt., 2000; Alberer ir kt., 2017). Šiuo metu klinikiniuose tyrimuose DNR vakcinos įvedimui paprastai naudojamos ID arba IM injekcijos, o po to EP (Sardesai ir Weiner 2011). EP apima porų formavimąsi odos ląstelėse, kad padidintų genetinės medžiagos įsisavinimą ląstelėse naudojant elektros impulsus (Pushparajah ir kt., 2021). IM EP metodas pirmiausia buvo pritaikytas 1998 m. (Aihara 1998), padidinant raumenų ląstelių įsiskverbimą į DNR vakcinas (Rizzuto ir kt., 1999; Dupuis ir kt., 2000; Sokołowska ir Błachnio-Zabielska, 2019). Daugybė pranešimų atskleidė geresnę antigeno ekspresiją ir padidino specifinį antigenui imuninį atsaką in vivo naudojant EP (Yan ir kt., 2008; Yan ir kt., 2009). Buvo pranešta, kad ŽIV DNR vakcina ADVAX padidino imunogeniškumą po perkėlimo per EP (Vasan ir kt., 2011), palyginti su IM vartojimu (Vasan ir kt., 2010). Nepaisant to, EP metodas kenčia nuo ląstelių mirties rizikos dėl aukštos įtampos naudojimo (Gulce-Iz ir Saglam-Metiner 2019). Nauji pristatymo metodai, tokie kaip EP, vis dar tiriami RNR vakcinos pristatymui.

cistanche nauda vyrams - stiprina imuninę sistemą
EP efektyvumas savaime amplifikuojančiai vakcinai buvo panašus į plazmidinių DNR vakcinų veiksmingumą pagal genų ekspresiją ir imuninį atsaką pelėms (Cu ir kt., 2013). Tačiau EP nepadidino tradicinių nereplikuojančių RNR vakcinų pristatymo veiksmingumo (Johansson ir kt., 2012), todėl galbūt sumažėjo jų veiksmingumas dubliuojant RNR vektorius. Atitinkamai, EP ir biologiniai injektoriai yra naudingi parenteraliniam COVID-19 DNR/RNR vakcinų sušvirkštimui. Šie metodai prisideda prie didesnės DNR vakcinos kandidatų gamybos ir pristatymo bei žymiai pagerina rezultatus (Pushparajah ir kt., 2021).
Nukleino rūgščių pagrindu pagamintų vakcinų privalumai ir apribojimai
Kaip nauji ir daug žadantys imunizacijos metodai, nukleino rūgščių pagrindu pagamintos vakcinos suteikia įžvalgų apie saugios ir apsauginės vakcinacijos kūrimą (Choi ir Chang, 2013), kaip įrodė milijonai žmonių COVID-19 pandemijos metu. Nukleino rūgščių pagrindu pagamintos vakcinos turi trumpus vystymosi ciklus, todėl pandemijos metu jie greitai pasklinda. Norint panaudoti rekombinantines DNR vakcinas, reikia efektyviai perkelti DNR vektorių į branduolį, transkripciją ir tada transliuoti į norimą antigeną (Leitner ir kt., 1999). Dėl patogaus manipuliavimo ir nebrangios gamybos, plika plazmidinė DNR yra patrauklus antigenų pateikimo vektorius (Williams 2013). Paprastai plazmidinę DNR sudaro pagrindiniai genetiniai elementai, įskaitant antigeną koduojantį geną, promotorių, stiprintuvus ir transkripcijos nutraukimo/poliadenilinimo sekas (Vogel ir Sarver 1995). Plazmidinės DNR platforma yra perspektyvi biofarmacinė konstrukcija, daug kartų replikuojama nebrangiose prokariotinėse ląstelėse, tačiau ją reikia išvalyti (Prazeres ir kt., 1999; Ferreira ir kt., 2000; Suschak ir kt., 2017). RNR vakcinos yra sudarytos iš mRNR molekulių, turinčių antigeno RNR, apsuptą 3′, poli-A uodegos ir 5′ galais, ir joms trūksta transkripcijos reikalavimų. (Zhang ir kt. 2019). Kai kurios RNR vakcinos savaime amplifikuojamos, žinomos kaip nauja kuriama technologija. Atitinkamai, RNR molekulė gali būti replikuojama ir transliuojama šeimininke po gimdymo, nepaisant atviros RNR nestabilumo galimybės, taip padidinant imunogeninių peptidų ekspresiją (Pardi ir kt., 2018; Zhang ir kt., 2019; Wadhwa ir kt., 2020) . MRNR skaido visur esantys ribonukleazės fermentai (Wadhwa ir kt., 2020; Xu ir kt., 2020). 3′ poli-A uodegos ir 5′–7-metilguanozino dangtelio pridėjimas yra labai svarbus siekiant padidinti mRNR stabilumą ir transliaciją citozolyje (Gallie 1991; Schlake ir kt., 2012). Vakcinos įsisavinimo ir ekspresijos didinimo strategijos daugiausia buvo vertinamos DNR vakcinoms, o ne RNR vakcinoms, nes norint pasiekti branduolį, DNR reikia kirsti dvi ląstelių membranas. Priešingai, RNR prasiskverbia į citoplazmą per vieną membraną (Rauch ir kt., 2018). DNR struktūra yra palyginti stabilesnė. Per 7 metus buvo nustatyta, kad plazmidinė DNR išliko nepažeista ir nesiskyrė nuo naujai pateiktos DNR, laikomos –20 laipsnių temperatūroje (Walther ir kt., 2013; Pushparajah ir kt., 2021). Žemas pH ir temperatūra yra labai svarbūs norint išlaikyti DNR vientisumą ilgą laiką. Ir atvirkščiai, RNR yra labai jautri temperatūrai ir turi būti laikoma –70 laipsnių temperatūroje terpėje be fermentų, kad pailgėtų jos pusinės eliminacijos laikas (Jones ir kt., 2007).
Nukleino rūgščių pagrindu pagamintų vakcinų kūrimo iššūkiai
Gerai žinoma, kad vakcinos nuo COVID{0}} turi būti veiksmingos ir pakankamai apsaugotos (Grahamas, 2020 m.) ir sukelti ilgalaikį imunitetą. Tačiau metinė vakcinacija gali būti įmanoma remiantis kasmetine gripo vakcinos patirtimi (Randolph ir Barreiro 2020; van Riel ir de Wit 2020). COVID{5}} vakcinos kūrimas kelia iššūkių net naudojant naujas platformas. Nepaisant didelio koronaviruso smaigalio baltymo vakcinos imunogeniškumo ir apsaugos, mutacijų atsiradimas kelia susirūpinimą ir viruso atsiradimą iš naujo. Taigi ligos atsiradimo laiko ir vietos prognozė bei tikslus tikslinės baltymų sekos nustatymas yra svarbiausias vystymosi proceso etapas, kuriam reikia tinkamai atlikti klinikinius tyrimus (Lurie ir kt., 2020). Pagrindinis DNR vakcinų iššūkis yra sukelti santykinai mažesnį imuninį atsaką žmonėms ir dideliems gyvūnams nei mažų gyvūnų sistemose (Grunwald ir Ulbert 2015; Suschak ir kt., 2017). Pastebėtina, kad dar reikia spręsti su COVID{10}} vakcinomis susijusius tolesnius iššūkius, pvz., apsaugos patvarumą, veiksmingumą tam tikruose pogrupiuose, virusų perdavimo prevenciją ir visuomenės pripažinimą (Pushparajah ir kt., 2021). Uždelsta antigeno ekspresija savaime amplifikuojančiose mRNR vakcinose gali apriboti šių vakcinų veiksmingumą. Tačiau ši platforma suteikia didesnį derlių ir taip užtikrina lygiavertę apsaugą naudojant žymiai mažesnes dozes (Vogel ir kt., 2018; Strizova ir kt., 2021).
Naujausi COVID-19 DNR ir mRNR vakcinų pažanga
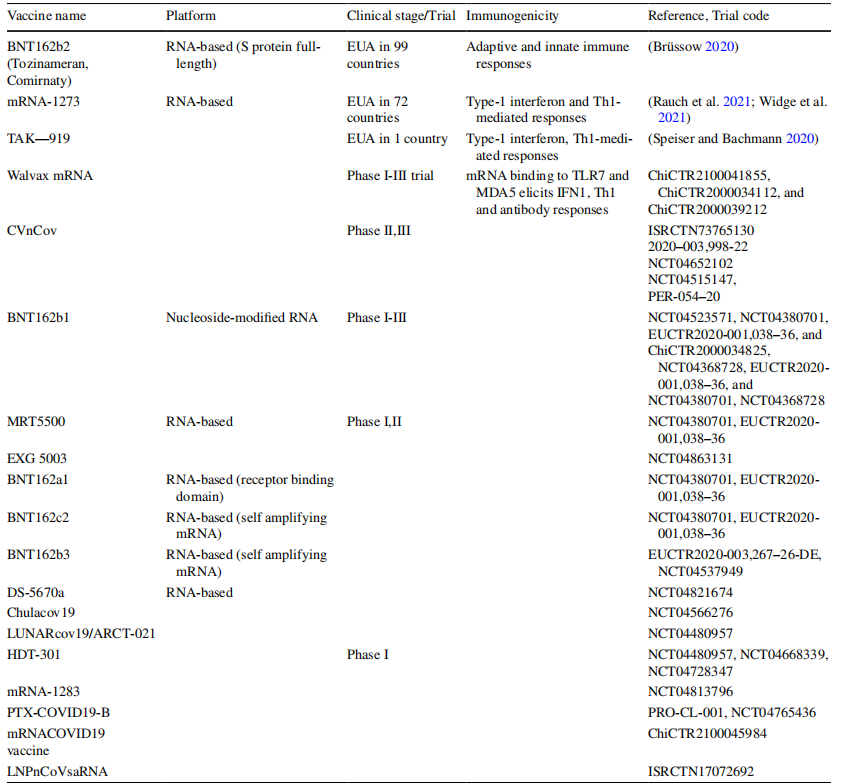
Kuriant vakciną nuo COVID{{0}}, daugybė tyrimų buvo sutelkti į mRNR vakcinų platformas (Verbeke ir kt. 2021), todėl buvo patvirtintos kelios vakcinos (Vitiello ir Ferrara 2{{ 94}}21), pvz., „Moderna“ ir „Pfizer / BioNtech“ įmonių. Moderna vakcina apima visą COVID-19 spike glikoproteino mRNR kodavimą, o Pfizer/BioNtech turi RBD mRNR seką (Brüssow 2020). Pfizer/BioNTech ir Moderna vakcinų veiksmingumo lygiai yra atitinkamai 95 % ir 94,5 % (Rauch ir kt., 2021; Widge ir kt., 2021). Moderna vakcinos laikymo temperatūra yra nuo –25 laipsnių iki –15 laipsnių, o Pfzer vakcinos – nuo –80 laipsnių iki –60 laipsnių (Meo ir kt., 2021; Rauch ir kt., 2021). Palyginti su Moderna vakcina, Pfizer/BioNTech vakcina turi mažesnes sąnaudas ir šalutinį poveikį (Rauch ir kt., 2021). Kitą mRNR vakciną nuo COVID{17}} sukūrė Kinijos mokslininkai ir naudojo termostabilią (mažiausiai vieną savaitę 25 laipsnių temperatūroje) UBR koduojančią mRNR (Brüssow 2020). Kitoje apklausoje CureVac buvo naudojama kaip sukurta viso ilgio S baltymo mRNR platforma COVID-19 vakcinos kūrimui su pakaitalais dviejose prolino liekanose, siekiant pagerinti baltymų stabilumą (Rauch ir kt., 2021). Ruklanthi de Alwis ir kt. (2021) sukūrė savaime transkribuojančią ir replikuojančią mRNR vakciną nuo COVID-19, naudodama viso ilgio S baltymą ir replikoną (de Alwis ir kt., 2021), kurią galima pritaikyti kaip veiksmingą ir saugią vienos dozės vakciną. kovoti su COVID{30}} (de Alwis ir kt., 2021). Panašiai buvo panaudota savaime amplifikuojanti RNR, koduojanti COVID-19 S baltymą, inkapsuliuotą lipidų nanodalelėje (LNP), kuri išryškino aukštus antikūnų ir ląstelinio imuninio atsako titrus (McKay ir kt., 2020). Kai kurios DNR vakcinos kandidatės, tokios kaip S, N ir M baltymų pagrindu pagamintos vakcinos, buvo sukurtos nuo SARS-CoV. Be to, S baltymo DNR vakcina veiksmingai sukėlė apsauginį poveikį nuo COVID-19 infekcijos, galbūt dėl to, kad S baltymas atlieka gyvybiškai svarbų vaidmenį jungiantis receptoriams (Zhao ir kt., 2020). INO-4800 yra COVID-19 DNR vakcinos kandidatas, koduojantis COVID-19 S baltymą (Sarwar ir kt., 2020; Smith ir kt., 2020). Ikiklinikiniai pelių ir jūrų kiaulyčių rezultatai parodė humoralinį ir ląstelinį imuninį atsaką. I fazės klinikinių tyrimų metu dvi INO-4800 dozės buvo sušvirkštos per ID, papildytos EP per CELLECTRA®2000 Inovio Pharmaceutical (Diehl ir kt., 2013; Amante ir kt., 2015). Visiškas imuninis atsakas buvo paaiškintas remiantis antikūnų ir ląstelių atsakais 34 iš 36 I fazės klinikinio tyrimo dalyvių. Dešimt praneštų nepageidaujamų poveikių (AE) buvo pastebėti be jokių rimtų nepageidaujamų reiškinių (SAE) (fazė). I/II fazės klinikinis tyrimas buvo pradėtas siekiant įvertinti INO- 4800 imunogeniškumą, saugumą ir toleravimą (Tebas ir kt., 2019). INO-4800 laikymo sąlygos panašios (Smith ir kt., 2020), tikimasi paprastesnio vakcinos platinimo. Be to, kai kurios kitos COVID{56}} DNR vakcinų grupės pradėjo bandymus. 2020 m. birželio mėn. pradėtas GX{58}} I ir IIa fazės klinikinis tyrimas. DNR vakcina AG0301-COVID-19, pagaminta bendradarbiaujant Osakos universitetui (Japonija), Takaro Bio ir AnGes, 2020 m. liepos mėn. pradėtas įdarbinti I ir II fazės klinikiniams tyrimams, siekiant įvertinti jo imunogeniškumas ir saugumas (Speiser ir Bachmann 2020). Buvo atlikti I ir II fazės klinikiniai tyrimai, siekiant įvertinti trijų ZyCoV-D dozių imunogeniškumą ir saugumą (Kumar ir kt., 2021). Ši geriamoji vakcina plazmidinėje DNR užkodavo smaigalio baltymą, dinamiškai amplifikuotą gyvoje Bifidobacterium longum, gerai atpažįstamoje žarnyno probiotinėje bakterijoje. Buvo pradėtas kitas I fazės klinikinis tyrimas, skirtas įvertinti CORVax12, DNR vakciną, koduojančią smaigalio baltymą. Ištirtas elektroporuoto CORVax12 efektyvumas atskirai arba kartu su kita plazmide, koduojančia interleukiną 12 (IL-12). Įvairios COVID-19 mRNR vakcinos yra kuriamos ir davė daug žadančių rezultatų (Leitner ir kt., 1999; Croyle ir kt., 2001). Įvairus požiūris į RQ3013-VLP (koduojančių S, E ir M baltymus) kūrimą buvo veiksmingas in vivo naudojant mRNR kokteilį. Ši mRNR vakcina buvo integruota su pakeistais nukleozidais, o po to supakuota į LNP ir atskleidė gebėjimą sukelti pelių stiprų ląstelinį ir humoralinį imuninį atsaką (Le ir kt., 2020; Lu ir kt., 2020a). Sukurta arginil-glicil-asparto rūgšties (RGD) domeno DNR vakcina dviem dozėmis po 60 µg, naudojant elektroporaciją, pagerino poveikį BALB/cJ pelėms (Guo ir kt., 2021). Vienos dozės (0,2 mg) DNR vakcinos IM + reaktyvinė injekcija gali imunizuoti Sirijos žiurkėnus (Brocato ir kt., 2021). Kita DNR vakcina, naudojanti S baltymą trimis dozėmis, apsaugojo Rhesus makakas (Yadav ir kt., 2021). UBR suliejimas su hepatito B viruso preS1 aminogaline ir IM injekcija trimis dozėmis (0, 2 ir 4 savaitės) C57BL/6 pelėms sukėlė humoralinį ir ląstelinį imuninį atsaką (Jeong ir kt., 2021). Be to, S baltymo plazmidės DNR ir S1 subvieneto (rekombinantinio baltymo) IM injekcija trimis dozėmis 0, 2 ir 8 savaites rezus makakose stimuliavo neutralizuojančius antikūnus (Prompetchara ir kt., 2021). S baltymo IM+EP injekcija trimis dozėmis (0, 2 ir 4 savaitės) ICR pelėms paskatino humoralinį ir ląstelių atsaką (Li ir kt., 2021). Į kitas klinikinių tyrimų DNR vakcinas buvo įtrauktas S baltymas I/II fazėse 2022 m. birželį (NCT04445389, IM būdas 18–50 metų suaugusiems), 2021 m. liepos mėn. (NCT04463472, IM būdas 20–60 metų suaugusiems), 2021 m. rugsėjis (NCT04527081, IM maršrutas 20–65 metų suaugusiems) ir I fazė (NCT04336410, ID maršrutas 18 metų ir vyresniems), 2022 m. vasario mėn. (NCT04334980, oralinis 18 metų ir vyresniems) ir 2021 m. birželio mėn. NCT04591184, IM maršrutas 18–84 metų suaugusiems). Be to, mRNR vakcinos klinikiniuose tyrimuose apėmė II fazės vakcinas 2021 m. lapkritį (NCT04515147, IM, 18–60 metų), II–III fazės 2022 m. gruodžio mėn. (NCT04368728, IM 18–85 metų suaugusiems) ir I fazę. 2021 m. birželio mėn. (NCT04566276, IM 18–75 metų suaugusiems). COVID-eVax buvo UBR pagrindu sukurta vakcina, kuri po 38 dienų sukėlė pakankamą imuninį atsaką pelėms, šeškams ir žiurkėms (Conforti ir kt., 2022). Dvi (X-19 ir GX-19N) DNR vakcinos, koduojančios smaigalio ir nukleokapsidės baltymus, buvo įvertintos I fazės tyrimuose tarp 19–49 metų suaugusiųjų, o surišantys antikūnai buvo aptikti po antrosios vakcinacijos dozės. Šių vakcinų saugumas ir toleravimas buvo patvirtintas, nes GX-19N sukėlė didesnį T ląstelių kiekį ir antikūnų atsaką (Ahn ir kt., 2022). Xcl1-SARS-CoV{-2 smaigalių suliejimo DNR vakcina sukėlė didesnį antikūnų ir T ląstelių sukeltų atsakų dažnį, palyginti su plazmidės turinčiu smaigalio genu atskirai in vitro ir in vivo (Qi ir kt. 2022). Neseniai panaudota bakulovirusinė COVID{153}} Delta DNR vakcina gali apsaugoti 100 % pelių nuo COVID{155}} (Jang ir kt., 2023). Linijinė DNR (linDNR), koduojanti SARS-CoV{158}} UBR (Lin-COVIDeVax), sugebėjo sukelti antikūnų ir T ląstelių atsaką ir užtikrinti saugumą bei neturėjo neigiamo poveikio (Conforti ir kt., 2023). 1 lentelėje pateikti klinikiniai tyrimai ir patvirtintos nukleorūgščių pagrindu pagamintos vakcinos nuo COVID{163}}. Atnaujintais duomenimis, 229 820 324 asmenys visame pasaulyje buvo paskiepyti COVID{167}} vakcinomis, tarp kurių iš Afrikos šalių pasiskiepijo mažiau (https://www.usnews.com/news/coronavirus-and -vaccine-news, https://www.bloomberg.com/graph ics/covid-vaccine-tracker-global-distribution/). Atitinkamai, vakcinacijos rodiklis yra susijęs su įvairių regionų / vietovių ekonominėmis sąlygomis.
Galimos COVID-19 vakcinų saugos problemos
Kiekvienos sukurtos profilaktinės ar profilaktinės vakcinos saugos stebėjimas yra vienas iš esminių aspektų. MRNR vakcinos gamybos procesuose nebūtina naudoti toksiškų cheminių medžiagų ar ląstelių kultūros, todėl ji vadinama saugia platforma. Trumpas gamybos laikas taip pat sumažina užteršimo mikroorganizmais riziką (Wang ir kt., 2020). Dažniausiai pranešta apie galvos skausmą, nuovargį ir kitus sisteminius sunkius reiškinius, tokius kaip karščiavimas, šaltkrėtis, mialgija, vėmimas, pilvo skausmas ir reti viduriavimo pranešimai. Tačiau mRNR vakcinos recipientų mirtis nepastebėta (Chapin-Bardales ir kt., 2021; Skowronski ir De Serres, 2021). Kai kurie sisteminiai šalutiniai poveikiai, tokie kaip anafilaksija, dažniausiai pasireiškia alergiškiems asmenims ir yra 2,5–11,1 atvejo milijonui dozių (Shimabukuro ir kt., 2021). Stiprus imuninis atsakas jaunesniems nei kiti žmonėms gali sukelti didelius sisteminius reiškinius ir pranešama apie daugiau šalutinių poveikių po antrosios vakcinos dozės suleidimo, palyginti su pirmąja doze (Male 2021; Skowronski ir De Serres 2021). Be to, skausmas injekcijos vietoje, paraudimas ir patinimas yra labiausiai lokalūs šalutiniai poveikiai (Anand ir Stahel 2021). Remiantis pakankamais patvirtintų mRNR vakcinų, įskaitant „Pfizer/BioNTech“ ir „Moderna“, įrodymų, nebuvo įrodyta, kad nėštumo metu gali atsirasti persileidimų (dažnis =0%) (2021 m. vyras). Pastebėtina, kad DNR vakcinos yra pakankamai saugios, bet ne visada imunogeniškos; todėl pakankamam imuniniam atsakui reikia papildomų dozių. Humoralinis imuninis atsakas nebuvo nuoseklus atliekant tyrimus su žmonėmis, o ląstelinis imunitetas atrodo labiau paplitęs. Atitinkamai DNR vakcinų saugumas vyresnio ir jaunesnio amžiaus žmonėms yra palankesnis (Ledgerwood ir kt., 2011; Houser ir kt., 2018; Carter ir kt., 2019). Susirūpinimas dėl saugumo rodo galimą transfekuotos DNR integraciją į gemalo linijas ir šeimininko somatines ląsteles. Tokiais atvejais genų ekspresijos reguliavimas gali atsirasti kartu su daugybe reikšmingų mutacijų. Nepaisant to, kuriant DNR vakciną, paprastai naudojamos tik ekstrachromosominės ir nepakankamos chromosomų integracijos plazmidės. Be to, dauguma plazmidžių lieka vartojimo vietoje (Schalk ir kt., 2006). Neseniai atlikta sisteminė apžvalga ir metaanalizė parodė, kad mRNR vakcinos yra susijusios su didesniais nepageidaujamais reiškiniais, palyginti su kitomis platformomis (Kouhpayeh ir Ansari 2022). Neseniai 34-metų moteriai buvo pastebėtas retas su BNT162b2 mRNR vakcina susijusio miozito atvejis (Magen ir kt., 2022). DNR metilinimas ir atitinkami epigenetiniai pakitimai taip pat trikdo DNR ir mRNR vakcinų veiksmingumą (Pang ir kt., 2022). Pastebėtina, kad kelios patvirtintos nukleorūgščių vakcinos (ZyCoV-D, DNR plazmidinė vakcina, naudojama intradermiškai, Indija), BNT162b2 (mRNR, 2 dozės, Vokietija), mRNR- 1273 (Moderna, JAV, 2 dozės), ARCoV (WALVAX, Kinija) ir klinikiniai tyrimai, įskaitant 302-COVID19 (DNR plazmidinė vakcina, II/III fazės į raumenis, Japonija), INO-4800 (DNR plazmidė, II/III fazė, intraderminė, Kinija), GX{{36 }}N (DNR vakcina, Genexine, II/III fazė), Covigenix VAX-001 (DNR vakcina, Entos Pharmaceuticals, I/II fazė, į raumenis), COVID-eVax (DNR vakcina, I/II fazė, į raumenis , Roma) ir bacTRL-Spike (DNR vakcina, I fazė, geriamoji, Symvivo) (Sheridan 2021; Liu ir Ye 2022a). Šios vakcinos paskatino humoralinį ir ląstelinį imunitetą, išskyrus GX-19N ir AG0302- COVID-19. Kai kurie neigiami COVID-19 nukleorūgščių pagrindu pagamintų vakcinų poveikiai yra skausmas, limfadenopatija, eritema, paraudimas, patinimas, pykinimas, nuovargis, artralgija, mialgija, karščiavimas, širdies ir kvėpavimo sustojimas, insultas, padidėjusio jautrumo reakcija, alkoholinė kepenų liga, Belo paralyžius. , paroksizminė skilvelių aritmija ir mirtis (Norquist ir kt., 2012; McNeil ir DeStefano, 2018; Baden ir kt., 2021; Momin ir kt., 2021; Liu ir Ye, 2022b, 2022a).
Feniletanolio glikozidas yra pagrindinis aktyvus Cistanche deserticola komponentas
Išvada
Dėl greitos COVID{0}} pandemijos nepatenkintas poreikis sukurti veiksmingas vakcinas, kad būtų išvengta šios ligos. Nors DNR vakcinų imunogeniškumas gyvūnams yra priimtinas, žmonėms reikalingas klinikinis patvirtinimas. RNR vakcinos gali suteikti tinkamų imunologinių savybių ir didelių pranašumų, palyginti su DNR vakcinomis. Problemos, susijusios su nestabilia RNR prigimtimi, buvo išspręstos naudojant tinkamus saugojimo metodus ir formules, kad būtų sustabdytas jos skilimas. Vakcinos sauga taip pat yra svarbi ir negali būti pažeista siekiant didesnio veiksmingumo. Yra patvirtintų nukleino rūgščių pagrindu sukurtų vakcinų, skirtų COVID-19 plitimui kontroliuoti. Dalyvių stebėjimas turi būti tęsiamas. Reikia mokytis apie nukleorūgščių pagrindu pagamintos COVID{5}} vakcinos šalutinį poveikį. Be to, vakcinų pakartotinis įvertinimas ir polivalentinių vakcinų kūrimas arba pan-koronaviruso strategijos yra daug žadančios, atsižvelgiant į naujų susirūpinimą keliančių variantų atsiradimą.
1 lentelė Klinikiniai tyrimai ir patvirtintos COVID-19 vakcinos bei jų savybės

Nuorodos
Abdelmageed MI ir kt. (2020) Daugiaepitopinės peptidinės vakcinos nuo žmogaus COVID -19 E baltymo kūrimas: imunoinformatikos metodas. Int J Biomed Clin Anal. https://doi.org/ 10.1155/2020/2683286
Abera G, Berhanu G, Tekewe A (2012) Ribozimai: nukleorūgščių fermentai, galintys pritaikyti farmacijoje: apžvalga. Pharmacophore 3:164–178
Ahn JY ir kt. (2022) Dviejų rekombinantinės DNR COVID-19 vakcinų, kuriose yra spygliuočių arba smaigalių ir nukleokapsidės baltymų koduojančių sričių, saugumas ir imunogeniškumas: tarpinė dviejų atvirų, neatsitiktinių imčių, 1 fazės tyrimų analizė. sveikiems suaugusiems. Lancet Microbe 3:e173–e183. https://doi.org/10.1016/ S2666-5247(21)00358-X
Aihara H (1998) Miyazaki J. genų perkėlimas į raumenis elektroporacija in vivo. Nat Biotechnol 16:867–870. https://doi.org/10. 1038/nbt0998-867
Alberer M et al (2017) mRNR vakcinos nuo pasiutligės saugumas ir imunogeniškumas sveikiems suaugusiems: atviras, neatsitiktinių imčių, perspektyvus, pirmasis 1 fazės klinikinis tyrimas su žmogumi. Lancetas 390: 1511–1520.https://doi.org/10.1016/s0140-6736(17)31665-3
Amante DH ir kt. (2015) Odos transfekcijos modeliai ir elektroporacijos sustiprintos plazmidės tiekimo ekspresijos kinetika naudojant nešiojamąjį naujos kartos odos elektroporacijos įrenginį CELLECTRA-3P. Žmogaus genų terapijos metodai 26:134–146. https:// doi.org/10.1089/hgtb.2015.020
Anand P, Stahel VP (2021 m.) Apsvarstykite Covid-19 mRNR vakcinų saugumą: apžvalga. Pacientas Saf Surg 15:20. https://doi.org/10.1186/ s13037-021-00291-9
Baden LR ir kt. (2021) mRNR-1273 SARS CoV-2 vakcinos veiksmingumas ir saugumas. N Engl J Med 384:403–416. https://doi.org/10. 1056/NEJMoa2035389
Becker PD, Noerder M, Guzmán CA (2008) Genetinė imunizacija: bakterijos kaip DNR vakcinos pristatymo priemonės. Hum Vaccin 4:189–202.https://doi.org/10.4161/hv.4.3.6314
Borah P ir kt. (2021) RNR vakcinos kandidatų nuo COVID perspektyvos-19. Priekyje Mol Biosci. https://doi.org/10.3389/fmolb. 2021.635245
Brocato RL ir kt. (2021) Apsauginis SARS-CoV-2 DNR vakcinos veiksmingumas laukinio tipo ir imunosupresuotų Sirijos žiurkėnų organizme. Npj Vakcinos 6:1–7.https://doi.org/10.1038/s41541-020-00279-z
Brüssow H (2020) Pastangos kuriant COVID-19 vakciną. Environ Microbiol 22:4071-4084. https://doi.org/10.1111/1462-2920. 15225
Buchholz UJ ir kt. (2004) Sunkaus ūminio kvėpavimo sindromo koronaviruso struktūrinių baltymų indėlis į apsauginį imunitetą. Proc Natl Acad Sci 101:9804-9809. https://doi.org/ 10.1073/pnas.0403492101
Campbell JD (2017) CpG adjuvanto 1018 kūrimas: atvejo tyrimas. Vakcina Adjuv. https://doi.org/10.1007/ 978-1-4939-6445-1-2
Carter C ir kt. (2019) Tiriamos sezoninės gripo hemagliutinino DNR vakcinos ir po to trivalentės inaktyvuotos vakcinos, švirkščiamos į odą arba į raumenis sveikiems suaugusiems žmonėms, saugumas ir imunogeniškumas: atviras atsitiktinių imčių 1 fazės klinikinis tyrimas. PLoS One 14:e0222178. https://doi.org/10.1371/ journal.pone.0222178
Chapin-Bardales J, Gee J, Myers T (2021) Reaktogeniškumas gavus mRNR pagrindu pagamintas COVID-19 vakcinas. JAMA. https://doi. org/10.1001/jama.2021.5374
Chen Y, Cheng L, Lian R, Song Z, Tian J (2021) COVID{1}} vakcinos tyrimai daugiausia dėmesio skiria saugai, veiksmingumui, imunoinformatikai ir vakcinos gamybai bei pristatymui: bibliometrinė analizė, pagrįsta VOSviewer. Biosci tendencijos. https://doi.org/10.5582/bst.2021. 01061
Choi Y, Chang J (2013) Virusiniai vektoriai, skirti vakcinoms. Clin Exp Vaccine Res 2:97.https://doi.org/10.7774/cevr.2013.2.2.97
Chowdhury MA, Hossain N, Kashem MA, Shahid MA, Alam A (2020) Imuninis atsakas sergant COVID-19: apžvalga. J užkrėsti visuomenės sveikatą. https://doi.org/10.1016/j.jiph.2020.07.001
Coban C, Kobiyama K, Jounai N, Tozuka M, Ishii KJ (2013) DNR vakcinos: paprasta DNR jutimo medžiaga? Hum Vaccin Immunother 9:2216–2221.https://doi.org/10.4161/hv.25893
Conforti A et al (2022) COVID-eVax, kandidatas į elektroporuotą DNR vakciną, koduojančią SARS-CoV-2 UBR, sukelia apsaugines reakcijas gyvūnų modeliuose. Mol Ther 30:311–326. https://doi. org/10.1016/j.ymthe.2021.09.011
Conforti A, Sanchez E, Salvatori E, Lione L, Compagnone M, Pinto E ir kt. (2023) Kandidatas į linijinę DNR vakciną, koduojantis SARS CoV-2 receptorių surišimo domeną, sukelia stiprų imuninį atsaką ir neutralizuojančius antikūnus naminėms katėms. Mol Ther-Metho Clinic Dev 28:238-248. https://doi.org/10.1016/j.omtm.2022. 12.015 val
Croyle M, Cheng X, Wilson J (2001) Formulių, gerinančių fizinį virusinių vektorių stabilumą genų terapijai, kūrimas. Gene Ther 8:1281–1290.https://doi.org/10.1038/sj.gt.3301527
Cu Y ir kt. (2013) Padidėjęs savaime amplifikuojančių mRNR vakcinų pristatymas ir stiprumas elektroporacijos būdu in situ. Vakcinos 1:367–383. https://doi.org/10.3390/vaccines1030367
