Antikūnų neutralizavimo aktyvumo prieš SARS-CoV-2 variantus ir sezoninius žmogaus koronavirusus NL63, HKU1 ir 229E, sukeltų trijų skirtingų COVID-19 vakcinų platformų, analizė
Oct 26, 2023
Abstraktus: Koronavirusinės infekcijos, pasibaigusios neseniai 2019 m. prasidėjusia sunkia ūminio respiracinio sindromo koronaviruso 2 (SARS-CoV-2) pandemija, pabrėžė veiksmingų vakcinų svarbą skatinant antikūnų atsaką kryžmiškai neutralizuojančiu aktyvumu. COVID-19 vakcinos buvo greitai sukurtos siekiant sumažinti SARS-CoV-2 infekcijų naštą ir ligos sunkumą. Buvo iškelta hipotezė apie kryžminę apsaugą nuo sezoninių žmogaus koronaviruso (hCoV) infekcijų, tačiau tai vis dar prieštaringa. Čia mes ištyrėme neutralizuojantį aktyvumą prieš protėvių SARS-CoV{10}} ir susirūpinimą keliančius variantus (LOJ) asmenims, paskiepytiems dviem BNT162b2, mRNR-1273 arba AZD1222 dozėmis, su arba be istorijos. SARS-CoV{16}} infekcijos. Antikūnus neutralizuojantis aktyvumas prieš SARS-CoV-2 ir LOJ buvo didesnis BNT162b{20}}vakcinuotų asmenų, kurie anksčiau buvo užsikrėtę SARS-CoV-2 ir suteikė plataus spektro apsaugą. Omicron BA.1 variantas buvo atspariausias tarp LOJ. COVID-19 vakcinacija nesuteikė apsaugos nuo hCoV-HKU1. Atvirkščiai, antikūnai, kuriuos sukelia vakcinacija mRNR-1273, padidino jų neutralizuojantį aktyvumą prieš hCoV-NL63, o vakcinacija AZD1222 padidino antikūnų neutralizavimą prieš hCoV-229E, o tai rodo galimus skirtingų spuogų antigeniškumo ir imunogeniškumo skirtumus. konstrukcijos, naudojamos tarp įvairių skiepijimo platformų. Šie duomenys rodo, kad tarp HCoV ir SARS-CoV-2 smaigalių baltymų gali būti bendrų epitopų.
Raktiniai žodžiai: SARS-CoV-2; sezoninis; HKU1; 229E; NL63; neutralizavimas

cistanche tubulosa - stiprina imuninę sistemą
1. Įvadas
2019 m. gruodį visame pasaulyje greitai išplito naujojo koronaviruso, pavadinto sunkaus ūminio kvėpavimo sindromo koronavirusu 2 (SARS-CoV-2), protrūkis, dėl kurio kilo pasaulinė pandemija [1]. Nuo tada tarptautinės pastangos sukurti tinkamą gydymą paskatino kelių vakcinacijos platformų ir kitų antivirusinių vaistų kūrimą. Laipsniškas variantų augimas sumažino neutralizuojančių antikūnų, kuriuos sukėlė ankstesnė SARS-CoV infekcija-2 arba vakcinacija, veiksmingumą [2,3]. Pasaulio sveikatos organizacija (PSO) nerimą keliančius variantus priskyrė susirūpinimą keliantiems variantams (VOC), o kiti variantai, neatitinkantys tų pačių kriterijų, patenka į dominančius variantus (VOI) arba tiriamus variantus (VUI). Didelis dėmesys buvo skiriamas variantams ir jų savybėms, tokioms kaip antikūnų vengimas ir replikacijos greitis, o daugelyje tyrimų lyginami variantai ir jų gebėjimas neutralizuoti [4–8], pandemijai toliau progresuojant.

cistanche tubulosa - stiprina imuninę sistemą
SARS-CoV-2 priklauso Coronaviridae šeimai, kuriai priklauso SARS-CoV-1 [9], Vidurio Rytų kvėpavimo takų virusas (MERS) [10] ir keturi žmogaus koronavirusai 229E, HKU-1 , NL63 ir OC43 [11] (1A pav.). Nors SARS-CoV-1 ir MERS protrūkiai sukėlė sunkias žmonių ligas [12], kiti keturi koronavirusai, paprastai vadinami sezoniniais arba žmogaus koronavirusais (HCoV), paprastai sukelia lengvą ligą, panašią į peršalimą. [11,13]. Tačiau retais atvejais HCV gali sukelti sunkias ligas [14–16]. SARS-CoV-2 kartu su NL63 naudoja angiotenziną konvertuojantį fermentą 2 (ACE2) kaip pagrindinį receptorių, patenkantį į ląsteles [17,18]. Nepaisant to, kad HKU1 ir OC43 yra glaudžiau susiję su SARS-CoV-2, jie jungiasi su sialo rūgštimis kaip patekimo būdas [19], o tolimesni 229E naudoja žmogaus aminopeptidazę (hAPN) [20]. (1B pav.).
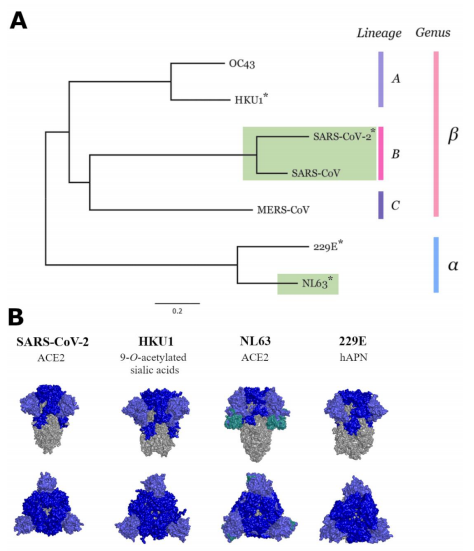
1 pav. Coronaviridae šeimos narių filogenetinis medis. * žymi smaigalio baltymus, kurie buvo naudojami šiame tyrime (A). SARS-CoV-2 ir trijų sezoninių HCV smailių baltymų struktūros; HKU1, NL63 ir 229E, kurie buvo naudojami šiame tyrime (B). (PBP kodai: 6VXX, 60HW, 6U7H, 5I08 ir 5SZS). Pilka spalva reiškia S2 domeną, o šviesiai mėlyna yra S1 subvieneto N-galinė sritis, o tamsiai mėlyna reiškia likusį S1 subvienetą. NL63 turi papildomą žalsvai melsvos spalvos sekciją, vaizduojančią unikalų regioną S1 domene, kurio nepastebėta kituose koronavirusuose [21].
Pandemijos pradžioje buvo diskutuojama dėl galimybės, kad antikūnai, sukurti prieš HCOV, turėjo kokį nors vaidmenį apsaugant nuo SARS-CoV-2 [22–25]. Nuo tada didėjantis susidomėjimas HCoV leido geriau suprasti jų sukeliamą imuninį atsaką. Keletas publikacijų, kuriose buvo tiriamas HCoV poveikis, rėmėsi surišimo tyrimų, pvz., su fermentu susijusių imunosorbentų tyrimų (ELISA), kurie matuoja antikūnų surišimą, bet neišaiškino jų neutralizavimo galimybių. Be to, sėkmingai sukurtos įvairios vakcinos platformos buvo naudojamos siekiant apsaugoti asmenis nuo infekcijų ir sunkių ligų [26], nors jų veiksmingumas mažėja, nes atsiranda naujesni ir labiau imuninę sistemą vengiantys variantai [27]. Čia naudojame lentivirusinius pseudotipinius SARS-CoV-2, LOJ/VOI ir HCoV virusus, kad išmatuotume neutralizuojančių antikūnų, kuriuos sukelia dvi BNT162b2 (Pfizer), AZD1222 (Astrazeneca) dozės, stiprumą. arba mRNR-1273 (Moderna) prieš SARS-CoV-2 ir variantus B.1.1.7 (Alfa), B.1.351 (Beta), P.1 (gama), B.1.617.2 ( Delta), B.1.525 (Eta) ir B.1.1.529 (Omicron BA.1) (2 pav.), ir ar kuri nors iš šių vakcinų gali padidinti neutralizuojančių antikūnų prieš HCoV 229E, HKU1 arba NL63.

2 pav. Šiame tyrime naudotos SARS-CoV-2 variantų mutacijos.
2. Medžiagos ir metodai
2.1. Paciento serumo rinkimo / etikos informacija
Serumo mėginiai buvo paimti iš 36 sveikų vakcinuotų asmenų. Tyrimą patvirtino San Raffaele mokslinės ligoninės etikos komitetas (protokolo numeris 68/INT/2020). Visi įtraukti pacientai davė raštišką informuotą sutikimą.
2.2. Filogenetinio medžio ir panašumo sklypas
Didžiausios tikimybės filogenetinė rekonstrukcija, pagrįsta smaigalio geno kodonų išlygiavimu, buvo sukurta naudojant medį (1.6.12 versija) [28] su 10,000 itin greitų įkrovos pakartojimų [29] ir TVM+F+I. +G4 pakeitimo modelis, pasirinktas naudojant ModelFinder [30]. Sekos panašumo grafikas buvo sudarytas lygiuojant SARS CoV-2 (QHD43416.1), HKU1 (YP_173238.1) 229E (NP_073551.1) ir NL63 ( YP_003767.1), naudojant mat (7.453 versija) [31] (genų poros parinktis) ir vizualizuota naudojant D3 JavaScript paketą, įdiegtą stebimame (https://observablehq.com/@spyros-lytras/seasonal cov -smaigalys pasiektas 2022 m. lapkričio 3 d.).
2.3. Audinių kultūra
Žmogaus embriono inksto 293T/17 (HEK293T/17) ląstelės ir žmogaus hepatocitų Huh- 7 ląstelės buvo palaikomos DMEM, papildytu 10 % galvijų vaisiaus serumo ir 1 % penicilino/streptomicino. Kininio kiaušidžių žiurkėno (CHO) ląstelės buvo laikomos Ham's F12, papildytu 10% galvijų vaisiaus serumo ir 1% penicilino / streptomicino. Ląstelės buvo reguliariai paskirstomos, kad būtų išvengta susiliejimo, plaunant fosfatu buferiniu druskos tirpalu ir atskiriant tripsinu-EDTA. Visos ląstelės buvo inkubuojamos 37 ◦C temperatūroje ir 5 % CO2.

cistanche augalą stiprinanti imuninė sistema
2.4. Pseudotipo viruso gamyba
Visi pseudotipai (PV) buvo sukurti, kaip aprašyta anksčiau [32]. Trumpai tariant, 1000 ng pc-DNR 3.1+ plazmidės, turinčios protėvių SARS-CoV-2, Alfa, Beta, Delta, Gamma, Eta, Omicron Ba variantų smaigalį. 1, arba HCoVs 229E, HKU1 ir NL63 buvo sumaišyti su 1000 ng p8.91 plazmidės, koduojančios ŽIV Gag-pol, ir 1500 ng pCSFLW plazmidės, turinčios Renilla ugniagesių luciferazės reporterio geną, ir kartu transfekuoti į HEK293% susiliejimo ląsteles. T-75 kolbose naudojant FuGENE-HD. HKU-1 prireikė papildomo veiksmo – 1,5 U egzogeninės neuraminidazės (Sigma) į 10 ml papildyto DMEM praėjus 24 valandoms po transfekcijos. Norint surinkti pseudotipinius virusus, terpė buvo išsiurbta praėjus 48 valandoms po transfekcijos dienos ir filtruojama naudojant 0, 45 µm celiuliozės acetato filtrą. Visi PV buvo padalyti į alikvotas ir laikyti –80 ◦ C temperatūroje. Po pakartotinių bandymų mums nepavyko nustatyti HCoV OC43 pseudotipo.
2.5. Pseudotipo viruso titravimas
Visi PV buvo titruoti, kaip aprašyta anksčiau [32]. Tikslinės SARS-CoV-2, variantų ir HCoV NL63 ląstelės buvo paruoštos dieną prieš titravimą, transfekuojant ACE-2 ir TRSSMP2. CHO ląstelės buvo naudojamos kaip tikslinės ląstelės HKU-1, o Huh-7 ląstelės buvo naudojamos kaip tikslinės ląstelės 229E. Trumpai tariant, 50 µL surinkto PV buvo įdėta į baltos F formos dugno 96-šulinėlių plokštelės (Nunc) viršutinę eilutę ir serijiniu būdu skiedžiama naudojant DMEM arba Ham's F-12, skirta HKU-1 PV per pusę žingsnių iki apatinės plokštelės eilės, prieš įdedant 10, 000 tikslinių ląstelių į kiekvieną šulinėlį. Plokštelės buvo grąžintos į inkubatorių 48 valandoms prieš lizuojant Bright-Glo reagentu ir tiriant luciferazės reporterio geno aktyvumą santykiniuose linijos vienetuose (RLU), naudojant Glo-Max luminometrą. PV titrai pateikiami RLU/ml.

cistanche tubulosa - stiprina imuninę sistemą
Spustelėkite čia norėdami pamatyti Cistanche Enhance Immunity produktus
【Klauskite daugiau】 El. paštas:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
2.6. Pseudotipo mikroneutralizacijos (pMN) tyrimai
pMN tyrimas buvo atliktas taip, kaip aprašyta anksčiau. Trumpai tariant, sveikstantys serumai buvo sumaišyti su DMEM arba Ham's F{0}} pradiniu praskiedimu santykiu 1:40, o po to serijiniu būdu skiedžiami 2- kartus baltoje plokščiadugėje 96-šulinėlių plokštelėje iki galutinio. praskiedimas santykiu 1:5120. Visi mėginiai buvo pakartoti dviem egzemplioriais. Tada į kiekvieną šulinėlį buvo pridėta PV, esant 1 × 106 RLU / ml įėjimui. Plokštelės buvo grąžinamos į audinių kultūros inkubatorių 1 valandai, prieš pridedant iš anksto transfekuotų ACE-2/TRSSMP2 HEK293T tikslinių ląstelių arba CHO ląstelių, skirtų HKU-1 ir Huh-7 ląstelėms. 229E, esant 1 × 104 ląstelių tankiui vienoje duobutėje. Plokštelės buvo grąžintos į inkubatorių 48 valandoms prieš lizuojant Bright-Glo reagentu ir tiriant luciferazės reporterio geno aktyvumą santykiniuose linijos vienetuose (RLU), naudojant Glo-Max luminometrą. IC50 buvo apskaičiuoti naudojant GraphPad Prism 8 programinę įrangą, naudojant nelinijinę regresijos kreivę, kaip aprašyta [33].
2.7. Statistinė analizė
Wilcoxon suderintų porų reitinguoti testai buvo naudojami suderintų tiriamųjų reikšmingumui įvertinti. Kruskal-Wallis ANOVA testas buvo naudojamas reikšmingumui įvertinti lyginant IC50 titrus tarp trijų vakcinų platformų. Visi testai buvo naudojami GraphPad Prism 8 programinėje įrangoje.
3. Rezultatai
3.1. Grupės charakteristikos
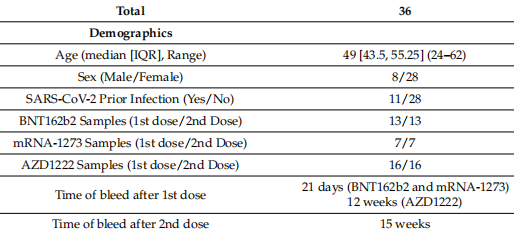
Siekiant įvertinti SARS-CoV-2 specifinių antikūnų prieš SARS CoV-2 LOJ ir hCoV neutralizavimo potencialą, serumai, gauti iš dvigubos dozės BNT162b2-vakcinuoto (n=13), Buvo tikrinami AZD1222-vakcinuoti (n=16) ir mRNR-1273-vakcinuoti (n=7) asmenys, sirgę SARS-CoV-2 infekcija ir jos neturintys ( 1 lentelė).
1 lentelė. Grupės demografinės ir klinikinės charakteristikos.
3.2. SARS-CoV-2 variantų neutralizavimas
Pirmiausia atlikome pMN tyrimus, siekdami išanalizuoti neutralizuojančių antikūnų atsakų prieš protėvių SARS-CoV-2 ir variantus mastą, neatsižvelgiant į vakcinos tipą (3A pav.). Mūsų rezultatai parodė, kad Omicron BA.1 buvo mažiausiai neutralizuotas LOJ (24-karto sumažėjimas, p =< 0.0001). As expected, we observed the samples from individuals with prior infection had higher neutralisation titers compared with immunologically naïve subjects. The serum from previously infected individuals (Figure 3B), neutralized the Alpha variant more effectively compared with the ancestral strain, as it showed a 1.3-fold decrease in median IC50 titre, followed by Eta and Delta variants, (3.4- and 4.5-fold decrease, respectively). Beta and Gamma variants were more resistant to neutralization (10.9- and 9.7-fold decrease, respectively), and Omicron BA.1 reached a 16.1-fold decrease compared with ancestral SARS-CoV-2. Notably, the majority of these subjects had received the BNT162b2 vaccine. Taken together, these results suggested that in vaccinated subjects the pre-existing immunity raised by natural infection with SARS-CoV-2, or a VOC is more effective in protecting against the spectrum of variants that emerged later over time, compared with immunity triggered by vaccination only. However, the recently emerged variants evolved mechanisms to evade the neutralizing antibody response.

3 pav. Serumo antikūnų gebėjimas neutralizuoti SARS-CoV-2 ir LOJ iš asmenų, vakcinuotų dviem BNT162b2, AZD1222 arba mRNR-1273 dozėmis. Neutralizuojantis antikūnų atsakas prieš protėvių SARS-CoV-2 ir jo variantus anksčiau užsikrėtusiems asmenims (mėlyna spalva) ir neužkrėstiems asmenims (raudonos spalvos), gaunantiems dvi BNT162b2, AZD1222 arba mRNR{12}} vakcinų dozes (A) . Wilcoxon suderintų porų ženklų rango testų statistinė analizė buvo naudojama siekiant palyginti protėvių SARS-CoV{15}} su kiekvienu variantu (A). BNT162b{17}}vakcinuotų asmenų, anksčiau sirgusių infekcija, serumų neutralizavimo profiliai. C skydelyje BNT162b2 statistinis testas nebuvo naudojamas dėl mažo imties dydžio ir didelių skirtumų. (B). Trijų tipų vakcinų neutralizavimo profiliai prieš variantus (C) ir vakcinų platformų palyginimas. (D) Wilcoxon suderintų porų ženklų rango testų statistinė analizė buvo naudojama siekiant palyginti protėvių SARS-CoV-2 su kiekvienu C skydelio variantu. Kruskal-Wallis ANOVA buvo naudojama statistinei analizei D skydelyje. ns {{23} } nereikšmingas, * p < 0.05, ** p < 0.01, *** p < 0,001, **** p Mažiau kaip arba lygus 0,0001.
Tada išanalizavome tiriamuosius, kurie prieš vakcinos skyrimą nebuvo užsikrėtę SARS-CoV{1}} (3C pav.). Kiekvienos vakcinos platformos veiksmingumas buvo analizuojamas atsižvelgiant į gebėjimą neutralizuoti tiek protėvių štamą, tiek jo variantus. Pastebėjome, kad BNT162b2-vakcinuotų asmenų serumo IC50 titrai buvo dideli, palyginti su serumais, gautais iš mRNR-1273- ir AZD1222-vakcinuotų asmenų. Nors Alfa variantas neparodė imuninio pabėgimo nė vienam iš vakcinuotų asmenų, visi LOJ buvo atsparūs antikūnų neutralizavimui skirtingais laipsniais (3C pav.). Mums nepavyko gauti reikšmingų reikšmingumo balų iš BNT162b2 mėginių dėl kelių mėginių (n=5) su labai dideliu IC50 titrų skirtumu. Nepastebėjome jokio statistiškai reikšmingo skirtumo tarp trijų vakcinų platformų, atsižvelgiant į jų gebėjimą neutralizuoti Alfa, Eta, Beta, Gamma ir BA.1 variantus. Ir atvirkščiai, didžiausias skirtumas tarp trijų vakcinų tipų buvo pastebėtas naudojant protėvių ir delta variantus, nes mRNR-1273 atitinkamai 16- ir 14-sumažėjo vidutiniai IC50 titrai. , palyginti su BNT162b2, o AZD1222 sumažėjo 38- ir 41- kartus (3D pav.).
3.3. Sezoninių HCoV neutralizavimas
Norėdami nustatyti, ar vakcinacija nuo SARS-CoV-2 gali apsaugoti nuo sezoninių HCV, paklausėme, ar ankstesnė SARS-CoV-2 infekcija turėjo įtakos antikūnų sukeltam HCV neutralizavimui (4A pav. ). Nepastebėjome statistiškai reikšmingo neutralizuojančių titrų prieš 229E arba HKU-1 padidėjimo tarp anksčiau SARS-CoV-2 užsikrėtusių ir negyvų asmenų. Priešingai, statistiškai reikšmingas neutralizuojančių titrų prieš NL63 sumažėjimas po antrosios dozės skyrimo buvo nustatytas paskiepytiems asmenims, kurie patyrė SARS-CoV-2 infekciją (p=0,033), lyginant su anksčiau negydytais (p {{). 16}}.063). Tada įvertinome, ar viena ar kelios vakcinos platformos padidins titrus prieš HCoV visiems tiriamiesiems, neatsižvelgiant į jų ankstesnę infekcijos būklę (4B pav.). Apskritai, vakcinuotų asmenų antikūnų neutralizavimo titrai prieš NL63 buvo didesni, palyginti su 229E ir HKU1, nepriklausomai nuo vakcinos platformos (4B pav.). Pažymėtina, kad NL63 naudoja ACE2 kaip įėjimo receptorių į tikslines ląsteles, kaip ir SARS-CoV-2. Vakcinos tipas neturėjo įtakos neutralizuojančiai veiklai prieš tris sezoninius koronavirusus, kuriuos tyrėme po antrosios dozės skyrimo, išskyrus NL63 ir HKU1. IC50 titrai prieš NL63 padidėjo po antrosios dozės naudojant mRNR-1273 (p=0.03), o 229E parodė statistiškai reikšmingą IC50 titro padidėjimą tik AZD1222-vakcinuotiems asmenims (p { {37}}< 0.001). Conversely, after the second boost of the BNT162b2 vaccine, neutralization titers against HCoV HKU-1 decreased, probably due to the selection of antigen-specific plasma cells with lower affinity for the HKU1 spike. To better understand the impact of COVID-19 vaccination on the protection from seasonal HCoVs in subjects with or without a history of SARS-CoV-2 infection, we analysed the spike protein similarity of HCoVs HKU1, NL63, 229E, and SARS-CoV-2 to investigate whether a particular region could explain the neutralization differences (Figure 4C). The similarity plot generated by comparing pairwise similarity showed HKU1 had higher similarity in all spike regions to the SARS-CoV-2 spike compared with 229E and NL63, consistent with the viruses' taxonomy. However, HKU1 seems to have extra insertions at the C-terminal end of the RBD compared with the other two seasonals and SARS-CoV-2. Furthermore, the S2 region shows much higher similarity to SARS-CoV-2 in all three HCoVs compared with the S1 region (Figure 4C).
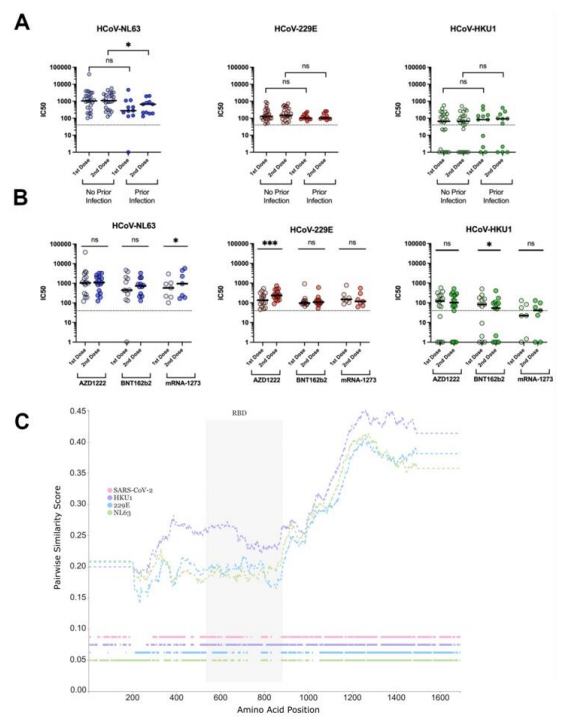
4 pav. Neutralizavimo atsakų palyginimas su HCoV NL63, 229E ir HKU1 tarp pirmosios ir antrosios vakcinacijos nuo SARS-CoV dozės-2. Neutralizacijos profilis prieš HCoV NL63, 229E ir HKU1 dviguba BNT162b2, mRNR-1273 arba AZD1222 doze – vakcinuotiems asmenims, sirgusiems SARS-CoV-2 infekcija arba be jo. (A). Neutralizuojantys antikūnų titrus prieš pirmiau minėtus HCoV po pirmosios ir antrosios BNT162b2, mRNR{{20}} arba AZD1222 vakcinos dozių. (B). A ir B buvo panaudota Wilcoxon suderintų porų rango testų statistinė analizė. Panašumo diagramos (C) rodo, kad HKU-1 smailė turi panašesnę aminorūgščių seką į SARS-CoV-2, palyginti su abiem. NL63 ir 229E visuose smaigalio baltymo regionuose. Brūkšninės linijos viršuje rodo aminorūgščių porų panašumą tarp SARS-CoV-2 ir 3 HCoV Spike baltymų, pavaizduotų naudojant 400 aminorūgščių lango dydį ir 1 žingsnį. Padėtys su tarpais buvo pašalintas iš langų. Horizontalios linijos apačioje rodo kiekvieno iš 4 išlygiuotų koronavirusų likučių buvimą per visą išlyginimo ilgį (spalvos buvimas=aminorūgščių buvimas; spalvos nebuvimas=tarpas). ns=nereikšminga, * p < 0,05, *** p < 0,001.
4. Diskusija
Šiame tyrime galėjome tiesiogiai palyginti antikūnų neutralizavimo titrus, sukeltus dviejų m-RNR pagrindu sukurtų vakcinų – BNT162b2 ir mRNR-1273 bei adenovirusinės vakcinos AZD1222 nuo SARS-CoV{{8}. }, atsiradę jo variantai ir trys sezoniniai HCoV. Mūsų duomenys apie antikūnų neutralizavimą prieš SARS-CoV{10}} ir jo variantus vakcinuotiems asmenims, kuriems anksčiau buvo užsikrėtę arba be jo, sutampa su tuo, kas aprašyta literatūroje [2,4,5,7,34–38 ]. Patvirtinome, kad vakcinacija dviem vakcinų dozėmis sukėlė antikūnus, galinčius neutralizuoti SARS-CoV-2 ir LOJ, o BNT162b2 sukėlė didžiausius neutralizavimo titrus, o po to seka mRNR-1273 ir AZD1222. Nepaisant neutralizavimo titrų skirtumų, buvo pranešta, kad visos trys vakcinos yra labai veiksmingos užkertant kelią sunkiam COVID -19 [39–41]. Omicron BA.1 variantas buvo labiausiai vengiantis iš visų šiame tyrime analizuotų LOJ (3 pav.). Iš tiesų, stipriai mutavęs BA.1 varianto baltymas kėlė problemų dabartinių vakcinų veiksmingumui apsaugoti nuo COVID-19 ir atkreipė dėmesį į būtinybę stebėti suteiktą apsaugą nuo šio ir naujai atsiradusio SARS-CoV{ {31}} variantai, būtent Omicron BA.4 ir BA.5. Dvivalentės mRNR vakcinų formulės, turinčios ir protėvių SARS-CoV-2 smaigalio mRNR, ir tą, kuri yra bendra tarp BA.4 ir BA.5 linijų, buvo sukurtos ir patvirtintos siekiant neutralizuoti. imuninio atsako, sukelto pradinio vakcinos dizaino, vengimas.
HCoV yra paplitę visame pasaulyje ir manoma, kad jie sukelia trumpalaikius apsauginius antikūnus [42]. Todėl yra didelė pakartotinio užsikrėtimo tikimybė, ypač žiemos laikotarpiais [13,43–45], nepaisant didelio serologinio paplitimo [43,45,46]. Šiuo metu diskutuojama, ar ankstesnė infekcija sezoniniais HCoV sukelia kryžmiškai reaktyvius antikūnus prieš SARS-CoV{10}} ir, dar svarbiau, ar tai reiškia apsaugą nuo SARS-CoV{12}}. Kryžmiškai reaguojantys antikūnai [47–54] ir T-ląstelių atsakai [55–61] buvo aptikti serumuose prieš pandemiją ir sveikuose donoruose; tačiau kiti tyrėjai panašius eksperimentinius metodus parodė priešingai [62]. Be to, daugelyje pirmiau minėtų straipsnių, kuriuose buvo atskleisti kryžmiškai reaguojantys antikūnai priešpandeminiuose mėginiuose, kryžmiškai reaguojančių mėginių skaičius sudarė mažą visų ištirtų serumų dalį, o tai rodo, kad kryžminis reaktyvumas, nors ir egzistuoja, yra mažas. . Tas pats klausimas buvo iškeltas dėl antikūnų, kuriuos sukelia COVID{25}} vakcinos, o tyrimai rodo kryžmiškai reaguojančius antikūnus prieš kai kuriuos, bet ne visus sezoninius HCV [63–65]. Įrodyta, kad vakcinacija nuo SARS-CoV-2 smaigalio baltymo makakose sukelia kryžmiškai reaktyvius antikūnus tiek prieš alfa, tiek prieš betakoronavirusus [66]. Svarbu išsiaiškinti, ar kryžmiškai reaguojantys antikūnai virsta apsauginiais, neutralizuojančiais antikūnais prieš SARS-CoV-2. Kai kuriose ataskaitose teigiama, kad nors SARS-CoV{38}} infekcijos metu šiek tiek padaugėja antikūnų prieš HCoV, jie nėra susiję su apsauga [67]. Panašiai tyrimai parodė, kad ankstesnė HCoV infekcija neapsaugo nuo SARS-CoV-2 infekcijos ir ligos [68, 69].

cistanche tubulosa - stiprina imuninę sistemą
Mes neradome jokio neutralizuojančių antikūnų prieš HKU1 titrų padidėjimo mūsų SARS-CoV-2-vakcinuotų asmenų grupėje, neatsižvelgiant į jų SARS-CoV-2 ikiinfekcinę būklę, išskyrus asmenis, kuriems buvo paskirta BNT162b2. Tai prieštarauja dviem pranešimams, kuriuose buvo pastebėtas HKU-1 titrų padidėjimas po vakcinacijos nuo SARS-CoV-2 BNT162b2 [63,64]. Hicks ir kt. parodė, kad antikūnai, reaguojantys į HCoV-OC43 ir HCoVHKU1, turėjo minimalų kryžminį reaktyvumą su SARS-CoV-2, atsižvelgiant į šių baltymų sekos homologiją [54]. Be to, ankstesnė SARS-CoV-2 infekcija nepadidino kryžminės neutralizacijos nei prieš HKU1, nei su filogenetiškai labiau susijusiu HCoV-229E (4A pav.). Vienoje ataskaitoje teigiama, kad HKU1 gali turėti kitą receptorių kandidatą, kuris dar turi būti identifikuotas, nes yra numanomas UBR, nutolęs nuo sialo rūgštį surišančių regionų [70, 71]. Taip pat reikėtų pažymėti, kad neutralizuojantis gebėjimas gali priklausyti ne tik nuo baltymo aminorūgščių porinio panašumo, bet ir nuo trumpų įterpimų bei ištrynimų, kurie gali pakeisti baltymo struktūrinę konformaciją. Pavyzdžiui, specifinis HKU{32}}įterpimas UBR C terminalo gale (4C pav.) gali iš dalies paaiškinti mūsų neutralizavimo rezultatus. Ir atvirkščiai, mes nustatėme, kad antrojo dozės skyrimas anksčiau negydytiems asmenims padidino apsauginį antikūnų atsaką prieš NL63, palyginti su gautu anksčiau užsikrėtusių asmenų, vartojusių tą pačią dozę. Tikriausiai taip atsitiko dėl to, kad papildomas smailės antigeno poveikis neturėjo įtakos antikūnų neutralizavimui prieš NL63.
Antikūnų neutralizavimo skirtumai tarp HCoV gali atsirasti dėl skiepijimo platformų naudojamų smailių skirtumų. BNT162b27 koduoja viso ilgio smaigalį su K986P ir V987P mutacijų vietomis, kad stabilizuotų baltymo konformaciją prieš suliejimą [72]. Vakcinoje mRNR-1273 yra smailaus glikoproteino kodavimo seka, stabilizuota tais pačiais prolino pakaitalais, kurie naudojami BNT162b2 vakcinoje, su transmembraniniu inkaru ir nepažeista S1-S2 skilimo vieta. Išankstinę suliejimo konformaciją stabilizuoja nuoseklūs prolino pakaitalai, esantys S2 subvienete centrinės spiralės viršuje [73]. Ir atvirkščiai, AZD1222 vakcina išreiškia vietinį smaigalį. Kadangi mūsų anksčiau negydytiems tiriamiesiems buvo skirta vakcina AZD1222, galime spėti, kad natūrali spygliuočių baltymo forma paskatino didesnių neutralizuojančių antikūnų titrų susidarymą, palyginti su tuo, kurį sukėlė iš anksto suliejus stabilizuotas baltymas. Ir atvirkščiai, antrasis imunogeninis SARS-CoV-2 poveikis padidino neutralizuojantį atsaką prieš NL63 arba 229E (4B pav.), kaip buvo pranešta anksčiau [67], priklausomai nuo vakcinos platformos, neatsižvelgiant į infekcijos būklė. Įdomu tai, kad kitoje ataskaitoje buvo pastebėtas tas pats kryžminio neutralizavimo aktyvumas, nors tai buvo neatsižvelgiama į vakcinos platformą [74]. Spėjame, kad kryžminis reaktyvumas gali atsirasti dėl NL63 receptorių surišimo motyvo (RBM) epitopų panašumo į SARS-CoV-2, nes abu virusai dalijasi AKF-2 kaip įėjimo receptoriumi [75] ]. Panašiai buvo pranešta, kad epitopas, persidengiantis su S2 sulietą peptidą 229E, sukelia kryžminį reaktyvumą prieš SARS-CoV-2 [48]. Song ir kt. aprašė apsauginius neutralizuojančius antikūnus, nukreiptus į S2 subdomeną [53]. Be to, ataskaitoje per pradinį SARS-CoV-1 protrūkį taip pat buvo rasta kryžmiškai reaguojančių antikūnų prieš NL63 ir 229E [76], o tai sustiprina hipotezę apie bendrus alfakoronavirusų ir betakoronavirusų epitopus. NL63 S baltyme nėra furino atpažinimo vietos ir jis nėra suskaidomas biogenezės metu [77]. Panašiai mRNR1273 vakcinos ekspresuojamam smaigalio baltymui trūksta skilimo vietos; todėl baltymo konformacija gali būti panaši ir gali sukelti neutralizuojančius antikūnus prieš bendrus epitopus, kurie sustiprėja po antrojo to paties antigeno poveikio.
Skirtingų vakcinų išreikšto smaigalio baltymo antigeninis pobūdis kartu su daugybe konformacijų, kurias jos gali įgyti, gali turėti įtakos neutralizuojančių antikūnų, turinčių skirtingą giminingumą keliems smaigalio baltymo epitopams, vystymuisi. Kadangi AZD-1222 smaigalyje nėra dviejų prolino mutacijų, kurios stabilizuotų jo smailę į trimerinę iki suliejimo struktūrą [78,79], po suliejimo atsiradęs smaigalys gali sukelti didesnį imuninį atsaką į epitopus. S2 domene. Tai gali paaiškinti, kodėl nepastebėjome jokio neutralizuojančių titrų prieš 229E padidėjimo nei mRNR pagrindu, nei sintezės stabilizuotuose imunogenuose, nei vakcinuotuose mėginiuose. Galiausiai, nepaisant stebimų titrų padidėjimo, negalime pasakyti, ar tai virsta apsauginiais titrais, nes apsaugos nuo SARS-CoV{11}} koreliacijos dar turi būti apibrėžtos. Mūsų tyrime yra keletas apribojimų, į kuriuos reikia atsižvelgti. Mūsų duomenims būtų buvę naudinga gauti daugiau mėginių iš visų tipų vakcinų platformų ir kontrolinius neskiepytų asmenų, užsikrėtusių SARS-CoV-2 arba ne, mėginius. Be to, mes neanalizavome pradinio kryžminio reaktyvumo neutralizuojančių antikūnų prieš sezoninius koronavirusus lygių mūsų vakcinuotų asmenų grupėje. Pankoronaviruso vakcina sukeltų antikūnus, kurie atpažįsta ir neutralizuoja daugybę koronavirusų. Tai sudėtinga dėl šių RNR virusų, kurie dažnai mutuoja ir sukelia imunitetą, kuris laikui bėgant silpnėja, genetinės prigimties, todėl padidėja pakartotinio užsikrėtimo tikimybė. Todėl pagrindinių epitopų, esančių labiausiai konservuotuose smaigalio baltymo regionuose, ypač S2 subvienete, nustatymas yra svarbus siekiant potencialiai sukelti neutralizuojančius antikūnus, turinčius platesnį afinitetą ląstelių receptoriams, kurie tarpininkauja viruso patekimui. Buvo suformuluoti keli vakcinos kandidatai, o kai kurie yra pagrįsti dvigubais antigenais, įskaitant ir smaigalius, ir nukleokapsidės (N) komponentus [80]. Šios kompozicijos yra ikiklinikinėje stadijoje, nes gali suteikti platesnį ir patvaresnį humoralinį ir ląstelinį imuninį atsaką prieš koronavirusus [80].
Nuorodos
1. Zhu, N.; Zhang, D.; Wang, W.; Li, X.; Yang, B.; Daina, J.; Zhao, X; Huangas, B.; Ši, W.; Lu, R.; ir kt. Naujas koronavirusas iš pacientų, sergančių pneumonija Kinijoje, 2019. N. Engl. J. Med. 2020, 382, 727–733. [CrossRef] [PubMed]
2. Altmann, DM; Boitonas, RJ; Beale, R. Imunitetas SARS-CoV-2 Susirūpinimo variantai. Mokslas 2021, 371, 1103–1104. [CrossRef] [PubMed]
3. Burki, T. SARS-CoV variantų supratimas-2. Lancet 2021, 397, 462. [CrossRef] [PubMed]
4. Garcia-Beltran, WF; Lamas, EK; St Denisas, K.; Nitido, AD; Garcia, ZH; Hauseris, BM; Feldmanas, J.; Pavlovičius, MN; Gregory, didžėjus; Poznansky, MC; ir kt. Keli SARS-CoV-2 variantai išvengia neutralizavimo dėl vakcinos sukelto humoralinio imuniteto. Cell 2021, 184, 2372–2383. [CrossRef] [PubMed]
5. Hoffmann, M.; Arora, P.; Groß, R.; Seidel, A.; Hörnichas, BF; Hahn, AS; Krüger, N.; Graichen, L.; Hofmann-Winkler, H.; Kempfas, A.; ir kt. SARS-CoV-2 B.1.351 ir P.1 variantai pabėga nuo neutralizuojančių antikūnų. Cell 2021, 184, 2384–2393. [CrossRef]
6. Cantoni, D.; Mayora-Neto, M.; Nadesalingamas, A.; Wells, DA; Carnell, GW; Ohlendorfas, L.; Ferrari, M.; Palmeris, P.; Chanas, ACY; Smith, P.; ir kt. SARS-CoV neutralizavimo hierarchija-2 Susirūpinimą keliantys variantai, naudojant standartizuotus, kiekybinius neutralizavimo tyrimus, atskleidžia ryšį su ligos sunkumu; Apsauginių antikūnų slenksčių iššifravimo link. Priekyje. Immunol. 2022, 13, 773982. [CrossRef]
7. Planas, D.; Bruelis, T.; Grzelak, L.; Guivel-Benhassine, F.; Staropolis, I.; Porrot, F.; Planchais, C.; Buchrieser, J.; Rajah, MM; Vyskupas, E.; ir kt. Infekcinio SARS-CoV-2 B.1.1.7 ir B.1.351 variantų jautrumas neutralizuojantiems antikūnams. Nat. Med. 2021, 27, 917–924. [CrossRef]
8. Lustig, Y.; Cukermanas, N.; Nemetas, I.; Atari, N.; Klikeris, L.; Regev-Yochay, G.; Sapiras, E.; Mor, O.; Alroy-Preis, S.; Mendelsonas, E.; ir kt. Neutralizuojamas pajėgumas prieš Delta (B.1.617.2) ir kitus susirūpinimą keliančius variantus po bendros vakcinacijos (BNT162b2, BioNTech / Pfizer) sveikatos priežiūros darbuotojų vakcinacijos, Izraelis. Eurosurveillance 2021, 26, 2100557. [CrossRef]
9. Ksiazekas, TG; Erdmanas, D.; Goldsmith, CS; Zaki, SR; Peretas, T.; Emery, S.; Tong, S.; Urbani, C.; Comer, JA; Limas, W.; ir kt. Naujas koronavirusas, susijęs su sunkiu ūminiu kvėpavimo sindromu. N. Engl. J. Med. 2003, 348, 1953–1966. [CrossRef]
10. Zaki, AM; van Boheemen, S.; Bestebroer, TM; Osterhauzas, ADME; Fouchier, RAM naujojo koronaviruso išskyrimas iš žmogaus, sergančio plaučių uždegimu, Saudo Arabijoje. N. Engl. J. Med. 2012, 367, 1814–1820. [CrossRef]
11. Liu, DX; Liang, JQ; Fung, TS žmogaus koronavirusas-229E, -OC43, -NL63 ir -HKU1 (Coronaviridae). In Encyclopedia of Virology, 4th ed.; Bamford, DH, Zuckerman, M., red.; Academic Press: Oksfordas, JK, 2021 m.; 428–440 p. ISBN 978-0-12-814516-6.
12. de Wit, E.; van Doremalen, N.; Falzarano, D.; Munsteris, VJ SARS ir MERS: naujausios įžvalgos apie naujus koronavirusus. Nat. Rev. Microbiol. 2016, 14, 523–534. [CrossRef]
13. Gaunt, ER; Hardie, A.; Claas, ETT; Simmonds, P.; Templeton, KE Keturių žmogaus koronavirusų 229E, HKU1, NL63 ir OC43 epidemiologija ir klinikiniai pristatymai, aptikti per 3 metus, naudojant naują daugialypį realaus laiko PGR metodą. J. Clin. Microbiol. 2010, 48, 2940–2947. [CrossRef]
14. Da Veiga, ABG; Martins, LG; Riedigeris, I.; Mazetto, A.; Deburas, MdC; Gregianini, TS Daugiau nei paprastas peršalimas: endeminiai koronavirusai OC43, HKU1, NL63 ir 229E, susiję su sunkia ūmine kvėpavimo takų infekcija ir mirtimi sveikų suaugusiųjų tarpe. J. Med. Virol. 2021, 93, 1002–1007. [CrossRef]
15. Ardenas, KE; Nissenas, MD; Slots, TP; Mackay, IM Naujasis žmogaus koronavirusas, HCoV-NL63, susijęs su sunkia apatinių kvėpavimo takų liga Australijoje. J. Med. Virol. 2005, 75, 455–462. [CrossRef]
16. Ranka, J.; Rožė, EB; Salinas, A.; Lu, X.; Sakthivel, SK; Schneider, E.; Watson, JT Sunkios kvėpavimo takų ligos protrūkis, susijęs su žmogaus koronavirusu NL63, ilgalaikės priežiūros įstaigoje. Atsiras. Užkrėsti. Dis. 2018, 24, 1964–1966. [CrossRef]
17. Hoffmann, M.; Kleine-Weber, H.; Schroederis, S.; Krüger, N.; Herrler, T.; Erichsenas, S.; Schiergens, TS; Herrler, G.; Wu, N.-H.; Nitsche, A.; ir kt. SARS-CoV-2 ląstelių patekimas priklauso nuo ACE2 ir TMPRSS2 ir yra blokuojamas kliniškai įrodyto proteazės inhibitoriaus. Ląstelė 2020, 181, 271–280.e8. [CrossRef]
18. Hofmann, H.; Pyrc, K.; van der Hoek, L.; Geier, M.; Berkhoutas, B.; Pöhlmann, S. Žmogaus koronavirusas NL63 naudoja sunkaus ūminio kvėpavimo sindromo koronaviruso receptorių, skirtą patekti į ląsteles. Proc. Natl. Akad. Sci. JAV, 2005, 102, 7988–7993. [CrossRef]
19. Hulswit, RJG; Lang, Y.; Bakkers, MJG; Li, W.; Li, Z.; Schouten, A.; Ophorst, B.; van Kuppeveldas, FJM; Boons, G.-J.; Bosch, B.-J.; ir kt. Žmogaus koronavirusai OC43 ir HKU1 jungiasi prie 9-O-acetilintų sialo rūgščių per konservuotą receptorių surišimo vietą smaigalio baltymo domene A. Proc. Natl. Akad. Sci. JAV, 2019, 116, 2681–2690. [CrossRef]
20. Yeager, CL; Ašmunas, RA; Williams, RK; Cardellichio, CB; Šapiro, LH; Žiūrėti į; Holmes, KV Žmogaus aminopeptidazė N yra žmogaus koronaviruso 229E receptorius. Gamta 1992, 357, 420–422. [CrossRef]
21. Wu, K.; Li, W.; Pengas, G.; Li, F. NL63 kvėpavimo takų koronaviruso receptorius jungiančio domeno kristalinė struktūra, susieta su žmogaus receptoriumi. Proc. Natl. Akad. Sci. JAV 2009, 106, 19970–19974. [CrossRef]
22. Meyerholz, DK; Perlman, S. Ar peršalimo koronaviruso infekcija apsaugo nuo sunkios SARS-CoV{2}} ligos? J. Clin. Ištirti. 2021, 131. [CrossRef] [PubMed]
23. Ringlanderis, J.; Martneris, A.; Nilsson, S.; Westinas, J.; Lindas, M.; Hellstrand, K. Covid sergamumas ir sunkumas{1}} pacientams, sergantiems ir nesergančiais anksčiau patvirtintomis peršalimo koronaviruso infekcijomis. J. Užkrėsti. Dis. 2021, 223, 1831–1832. [CrossRef]
24. Schnierle, BS Atsakymas Ringlander ir kt. J. Užkrėsti. Dis. 2021, 223, 1833. [CrossRef] [PubMed]
25. Bereta, A.; Cranage, M.; Zipeto, D. Ar kryžminis reaktyvus imunitetas sukelia COVID{2}} imunopatogenezę? Priekyje. Immunol. 2020, 11, 2695. [CrossRef] [PubMed]
26. Creech, CB; Walkeris, SC; Samuels, RJ SARS-CoV{2}} Vakcinos. JAMA 2021, 325, 1318–1320. [CrossRef]
27. Tao, K.; Tzou, PL; Nouhin, J.; Gupta, RK; de Oliveira, T.; Kosakovsky Pond, SL; Fera, D.; Shafer, RW. Naujų SARS-CoV-2 variantų biologinė ir klinikinė reikšmė. Nat. Kunigas Genet. 2021, 22, 757–773. [CrossRef]
28. Nguyen, L.-T.; Schmidt, HA; von Haeseris, A.; Minh, BQ IQ-TREE: greitas ir efektyvus stochastinis algoritmas didžiausios tikimybės filogenezėms įvertinti. Mol. Biol. Evol. 2015, 32, 268–274. [CrossRef]
29. Hoangas, DT; Černomoras, O.; von Haeseris, A.; Minh, BQ; Vinh, LS UFBoot2: Ultrafast Bootstrap aproksimacijos tobulinimas. Mol. Biol. Evol. 2018, 35, 518–522. [CrossRef]
30. Kalyaanamoorthy, S.; Minh, BQ; Wongas, TKF; von Haeseris, A.; Jermiin, LS ModelFinder: Greitas modelio pasirinkimas tiksliam filogenetiniam įvertinimui. Nat. Metodai 2017, 14, 587–589. [CrossRef]
31. Katoh, K.; Standley, DM MAFFT kelių sekų derinimo programinės įrangos 7 versija: našumo ir naudojimo patobulinimai. Mol. Biol. Evol. 2013, 30, 772–780. [CrossRef]
32. Genova, CD; Sampsonas, A.; Skotas, S.; Cantoni, D.; Mayora-Neto, M.; Bentley, E.; Mattiuzzo, G.; Wright, E.; Derveni, M.; Auld, B.; ir kt. Sunkaus ūminio kvėpavimo sindromo koronaviruso 2 (SARS-CoV-2) lentivirusinių pseudotipų gamyba, titravimas, neutralizavimas, saugojimas ir liofilizavimas. Bio-Protocol 2021, 11, e4236. [CrossRef]
33. Ferrara, F.; Temperton, N. Pseudotipo neutralizavimo tyrimai: nuo laboratorinio stendo iki duomenų analizės. Metodai Protok. 2018, 1, 8. [CrossRef]
35. Liu, C.; Ginn, HM; Dejnirattisai, W.; Supasa, P.; Wang, B.; Tuekprakhon, A.; Nutalai, R.; Džou, D.; Mentzer, AJ; Zhao, Y.; ir kt. Sumažėjęs SARS-CoV-2 B.1.617 neutralizavimas vakcina ir sveikstančiu serumu. Ląstelė 2021, 184, 4220–4236.e13. [CrossRef]
35. Shen, X.; Tangas, H.; Pajonas, R.; Smithas, G.; Glennas, GM; Ši, W.; Korberis, B.; Montefiori, DC SARS-CoV-2 variantų B.1.429 ir B.1.351 neutralizavimas. N. Engl. J. Med. 2021, 384, 2352–2354. [CrossRef]
36. Shen, X.; Tangas, H.; McDanal, C.; Vagas, K.; Fišeris, W.; Theiler, J.; Yoon, H.; Li, D.; Haynes, BF; Sandersas, KO; ir kt. SARS-CoV-2 B.1.1.7 variantas yra jautrus neutralizuojantiems antikūnams, kuriuos sukelia protėvių spygliuočių vakcinos. Ląstelių šeimininko mikrobas, 2021, 29, 529–539. [CrossRef]
37. Willett, BJ; Grove, J.; MacLean, OA; Wilkie, C.; De Lorenzo, G.; Furnon, W.; Cantoni, D.; Skotas, S.; Loganas, N.; Ašrafas, S.; ir kt. SARS-CoV-2 Omicron yra imuninio pabėgimo variantas su pakeistu ląstelių patekimo keliu. Nat. Microbiol. 2022, 7, 1161–1179. [CrossRef]
38. Siracusano, G.; Ruggiero, A.; Bisoffi, Z.; Piubeli, C.; Carbonare, LD; Valenti, MT; Mayora-Neto, M.; Tempertonas, N.; Lopalco, L.; Zipeto, D. Skirtingas antikūnų atsako ir LOJ jautrumo mažėjimas naiviems ir anksčiau infekuotiems subjektams 15 savaičių po vakcinacijos BNT162b2. J. Vertimas Med. 2022 m., 20, 22. [CrossRef]
39. Polackas, FP; Tomas, SJ; Kičinas, N.; Absalonas, J.; Gurtmanas, A.; Lockhart, S.; Perezas, JL; Pérez Marc, G.; Moreira, ED; Zerbini, C.; ir kt. BNT162b2 MRNA Covid-19 vakcinos saugumas ir veiksmingumas. N. Engl. J. Med. 2020, 383, 2603–2615. [CrossRef]
40. Badenas, LR; El Sahly, HM; Essink, B.; Kotloffas, K.; Frey, S.; Novakas, R.; Diemertas, D.; Spector, SA; Rouphael, N.; Creech, CB; ir kt. MRNA{1}} SARS-CoV-2 vakcinos veiksmingumas ir saugumas. N. Engl. J. Med. 2021, 384, 403–416. [CrossRef]
41. Emary, KRW; Golubčikas, T.; Aley, PK; Ariani, CV; Angusas, B.; Bibi, S.; Blane, B.; Bonsall, D.; Cicconi, P.; Charlton, S.; ir kt. ChAdOx1 NCoV-19 (AZD1222) vakcinos nuo SARS-CoV-2 veiksmingumas Variantas susirūpinimą 202012/01 (B.1.1.7): atsitiktinių imčių kontroliuojamo tyrimo tiriamoji analizė. Lancet 2021, 397, 1351–1362. [CrossRef]
42. Edridge, AWD; Kaczorowska, J.; Šeimininkas, ACR; Bakker, M.; Kleinas, M.; Loensas, K.; Džebinkas, MF; Matser, A.; Kinsella, CM; Rueda, P.; ir kt. Sezoninis koronaviruso apsauginis imunitetas yra trumpalaikis. Nat. Med. 2020, 26, 1691–1693. [CrossRef] [PubMed]
43. Aldridžas, RW; Lewer, D.; Beale, S.; Johnsonas, AM; Zambonas, M.; Hayward, AC; Fragaszy, EB sezoniškumas ir imunitetas laboratorijoje patvirtintiems sezoniniams koronavirusams (HCoV-NL63, HCoV-OC43 ir HCoV-229E): gripo stebėjimo kohortos tyrimo rezultatai. Wellcome Open Res 2020, 5, 52. [CrossRef] [PubMed]
44. Zhang, S.-F.; Tuo, J.-L.; Huangas, X.-B.; Zhu, X.; Zhang, D.-M.; Džou, K.; Yuan, L.; Luo, H.-J.; Zheng, B.-J.; Yuen, K.-Y.; ir kt. Žmogaus koronavirusų epidemiologinės charakteristikos pacientams, turintiems kvėpavimo takų infekcijos simptomų, ir HCoV-OC43 filogenetinė analizė per 2010-2015 Guangdžou. PLoS ONE 2018, 13, e0191789. [CrossRef] [PubMed]
45. Byington, CL; Ampofo, K.; Stockmann, C.; Adleris, FR; Herbeneris, A.; Mileris, T.; Sheng, X.; Blaschke, AJ; Traškus, R.; Pavia, AT bendruomenės kvėpavimo takų virusų stebėjimas tarp šeimų Jutoje geresnio mikrobų identifikavimo ir išilginės virusinės epidemiologijos (BIG-LoVE) tyrimas. Clin. Užkrėsti. Dis. 2015, 61, 1217–1224. [CrossRef] [PubMed]
46. Wells, DA; Cantoni, D.; Mayora-Neto, M.; Genova, CD; Sampsonas, A.; Ferrari, M.; Carnell, G.; Nadesalingamas, A.; Smith, P.; Chanas, A.; ir kt. Žmogaus sezoninio koronaviruso neutralizavimas ir COVID{2}} sunkumas. J. Med. Virol. 2022, 94, 4820–4829. [CrossRef]
47. Shrwani, K.; Šarma, R.; Krišnanas, M.; Jonesas, T.; Mayora-Neto, M.; Cantoni, D.; Tempertonas, NJ; Dobsonas, SL; Subramaniam, K.; McNamara, PS; ir kt. Kryžmiškai reaktyvių antikūnų serume aptikimas ir atminties atsakas į SARS-CoV-2 priešpandeminiuose ir po COVID{6}} sveikimo mėginiuose. J. Užkrėsti. Dis. 2021, 224, 1305–1315. [CrossRef]
48. Ng, KW; Faulkner, N.; Kornvalio, GH; Rosa, A.; Harvey, R.; Hussain, S.; Ulfertas, R.; Earl, C.; Wrobel, AG; Bentonas, didžėjus; ir kt. Jau egzistuojantis ir de Novo humoralinis imunitetas SARS-CoV-2 žmonėms. Mokslas 2020, 370, 1339–1343. [CrossRef]
49. Woudenberg, T.; Pelleau, S.; Ana, F.; Atija, M.; Donnadieu, F.; Gravet, A.; Lohmann, C.; Seraphin, H.; Guiheneufas, R.; Delamare, C.; ir kt. Vaikų ir suaugusiųjų humoralinis imunitetas SARS-CoV-2 ir sezoniniams koronavirusams Šiaurės Rytų Prancūzijoje. EBioMedicine 2021, 70, 103495. [CrossRef]
50. Tso, FY; Lidenge, SJ; Penja, PB; Clegg, AA; Ngowi, JR; Mvaiselage, J.; Ngalamika, O.; Julius, P.; Vakarai, JT; Wood, C. Didelis jau esamo serologinio kryžminio reaktyvumo prieš sunkų ūminį kvėpavimo sindromo koronavirusą-2 (SARS-CoV-2) paplitimas Afrikoje į pietus nuo Sacharos. Tarpt. J. Užkrėsti. Dis. 2021, 102, 577–583. [CrossRef]
51. Laingas, ED; sterlingų, SL; Ričardas, SA; Phogat, S.; Samuelsas, EK; Epsi, NJ; Janas, L.; Moreno, N.; Coles, C.; Mehalko, J.; ir kt. Betakoronaviruso daugialypės mikrosferos imunologinis tyrimas aptinka ankstyvą SARS-CoV-2 serokonversiją ir jau egzistuojančio sezoninio žmogaus koronaviruso antikūnų kryžminio reaktyvumo kontrolę. medRxiv 2020. [CrossRef]
52. Ladneris, JT; Hensonas, SN; Boyle, AS; Engelbrektson, AL; Finkas, ZW; Rahee, F.; D'ambrozio, J.; Schaecher, KE; Akmuo, M.; Dongas, W.; ir kt. Pagal epitopą išspręstas SARS-CoV-2 antikūnų atsako profilis identifikuoja kryžminį reakciją su endeminiais žmogaus koronavirusais. Cell Rep. Med. 2021, 2, 100189. [CrossRef]
53. Daina, G.; Jis, W.; Callaghan, S.; Anzanello, F.; Huangas, D.; Ricketts, J.; Torresas, JL; Beutleris, N.; Pengas, L.; Vargas, S.; ir kt. Kryžminis reaktyvus serumas ir atminties B ląstelių atsakas į smaigalio baltymą sergant SARS-CoV-2 ir endemine koronaviruso infekcija. Nat. Komun. 2021, 12, 2938. [CrossRef]
54. Hicks, J.; Klumpp-Thomas, C.; Kalish, H.; Šunmugavelis, A.; Mehalko, J.; Densonas, J.-P.; Snead, KR; Drew, M.; Corbett, KS; Graham, BS; ir kt. Serologinis kryžminis SARS-CoV{5}} reaktyvumas su endeminiais ir sezoniniais betakoronavirusais. J. Clin. Immunol. 2021, 41, 906–913. [CrossRef]
55. Grifoni, A.; Weiskopfas, D.; Ramirezas, SI; Mateusas, J.; Danas, JM; Moderbacheris, CR; Rawlings, SA; Sutherlandas, A.; Premkumaras, L.; Jadi, RS; ir kt. T-ląstelių atsako į SARS-CoV-2 koronavirusą tikslai žmonėms, sergantiems COVID-19 liga, ir neveikiantiems asmenims. Ląstelė 2020, 181, 1489–1501.e15. [CrossRef]
56. Mateusas, J.; Grifoni, A.; Tarke, A.; Sidney, J.; Ramirezas, SI; Danas, JM; Mėsainiai, ZC; Rawlings, SA; Smithas, DM; Phillips, E.; ir kt. Selektyvūs ir kryžmiškai reaktyvūs SARS-CoV-2 T ląstelių epitopai neeksponuotiems žmonėms. Mokslas 2020, 370, 89–94. [CrossRef]
57. Sekinė, T.; Perez-Potti, A.; Rivera-Ballesteros, O.; Strålin, K.; Gorin, J.-B.; Olsson, A.; Llewellyn-Lacey, S.; Kamal, H.; Bogdanovičius, G.; Muschiol, S.; ir kt. Tvirtas T-ląstelių imunitetas sveikstantiems asmenims, sergantiems besimptomiu arba lengvu COVID{5}}. Ląstelė 2020, 183, 158–168.e14. [CrossRef]
58. Šulienė, I.; Kemingas, J.; Oberhardtas, V.; Laukinis, K.; Seidel, LM; Killmer, S.; Sagar; Daulas, F.; Salvat Lago, M.; Deckeris, A.; ir kt. Jau esamų ir sukeltų SARS-CoV-2-specifinių CD8+ T ląstelių apibūdinimas. Nat Med 2021, 27, 78–85. [CrossRef]
59. Reynolds, CJ; Swadling, L.; Gibbons, JM; Pade, C.; Jensen, MP; Dinizas, MO; Schmidt, NM; Butleris, DK; Aminas, OE; Bailey, SNL; ir kt. Nesuderinami neutralizuojančių antikūnų ir T ląstelių atsakai besimptomės ir lengvos SARS-CoV-2 infekcijos atveju. Sci. Immunol. 2020, 5, eabf3698. [CrossRef]
60. Žemas, JS; Vaqueirinho, D.; Melė, F.; Foglierinis, M.; Jerak, J.; Perotti, M.; Jarrossay, D.; Jovičius, S.; Perezas, L.; Cacciatore, R.; ir kt. CD4 T ląstelių atsako į SARS-CoV imunodominavimo ir kryžminio reaktyvumo kloninė analizė-2. Mokslas 2021, 372, 1336–1341. [CrossRef]
61. Echeverría, G.; Guevara, Á.; Coloma, J.; Ruizas, AM; Vasquez, MM; Tejera, E.; de Waard, JH. Ankstesnis T-ląstelių imunitetas SARS-CoV-2 neeksponuotose sveikose kontrolinėse grupėse Ekvadore, nustatytas atliekant COVID{5}} interferono-gama išsiskyrimo tyrimą. Tarpt. J. Užkrėsti. Dis. 2021, 105, 21–25. [CrossRef]
62. Postonas, D.; Weisblum, Y.; Išmintingas, H.; Templtonas, K.; Jenksas, S.; Hatziioannou, T.; Bieniasz, P. Sunkaus ūminio kvėpavimo sindromo koronavirusas 2 neutralizuojantis aktyvumas prepandeminiuose serumuose iš asmenų, sergančių neseniai sezonine koronaviruso infekcija. Clin. Užkrėsti. Dis. 2020, 73, e1208–e1211. [CrossRef] [PubMed]
63. Amanat, F.; Thapa, M.; Lei, T.; Ahmedas, SMS; Adelsbergas, Kolumbija; Carreño, JM; Strohmeier, S.; Schmitz, AJ; Zafaras, S.; Džou, JQ; ir kt. SARS-CoV-2 MRNR vakcinacija sukelia funkciškai skirtingus antikūnus prieš NTD, UBR ir S2. Ląstelė 2021, 184, 3936–3948.e10. [CrossRef]
64. Angyal, A.; Longet, S.; Moore, SC; Payne, RP; Hardingas, A.; Tiptonas, T.; Rongkardas, P.; Ali, M.; Heringas, LM; Meardonas, N.; ir kt. T-ląstelių ir antikūnų atsakas į pirmąją BNT162b2 vakcinos dozę anksčiau užsikrėtusiems ir SARS-CoV-2-naiviems JK sveikatos priežiūros darbuotojams: daugiacentris perspektyvus kohortos tyrimas. Lancet Microbe 2022, 3, e21–e31. [CrossRef] [PubMed]
65. Skelly, DT; Harding, AC; Gilbert-Jaramillo, J.; Riteris, ML; Longet, S.; Brownas, A.; Adelė, S.; Adlandas, E.; Brownas, H.; Tiptonas, T.; ir kt. Dvi SARS-CoV-2 vakcinacijos dozės sukelia stiprų imuninį atsaką į naujus SARS-CoV-2 susirūpinimą keliančius variantus. Nat. Komun. 2021, 12, 5061. [CrossRef] [PubMed]
66. Grobenas, M.; van der Stratenas, K.; Brouwer, PJ; Brinkkemperis, M.; Maisonnasse, P.; Dereuddre-Bosquet, N.; Apelmanas, B.; Lavell, AA; van Vught, LA; Mėsainiai, JA; ir kt. Kryžmiškai reaktyvūs antikūnai po SARS-CoV-2 infekcijos ir vakcinacijos. eLife 2021, 10, e70330. [CrossRef]
67. Andersonas, EM; Goodwin, EK; Verma, A.; Arevalo, CP; Boltonas, MJ; Weirick, ME; Gouma, S.; McAllister, CM; Christensen, SR; Weaver, J.; ir kt. Sezoniniai žmogaus koronaviruso antikūnai padidėja užsikrėtus SARS-CoV{2}}, bet nesusiję su apsauga. Ląstelė 2021, 184, 1858–1864.e10. [CrossRef]
68. Sermet-Gaudelus, I.; Temamas, S.; Huonas, C.; Behillil, S.; Gajdos, V.; Bigotas, T.; Lurier, T.; Chrétien, D.; Backovičius, M.; Delaunay Moisan, A.; ir kt. Ankstesnė sezoninių koronavirusų infekcija, įvertinus serologiją, neapsaugo nuo SARS-CoV-2 vaikų infekcijos ir ligų, Prancūzija, 2020 m. balandžio–birželio mėn. Eurosurveillance 2021, 26, 2001782. [CrossRef]
69. Gombaras, S.; Bergkvistas, T.; Pejaveris, V.; Hammarlund, NE; Murugesanas, K.; Mooney, S.; Shah, N.; Pinsky, BA; Banaei, N. SARS CoV-2 infekcija ir COVID-19 sunkumas asmenims, anksčiau užsikrėtusiems sezonine koronaviruso infekcija. Diagn. Microbiol. Užkrėsti. Dis. 2021, 100, 115338. [CrossRef]
70. Qian, Z.; O, X; Góes, LGB; Osborne, C.; Castano, A.; Holmsas, KV; Dominguez, SR Žmogaus betakoronaviruso HKU1 spike glikoproteino receptorius surišančio domeno identifikavimas. J. Virolis. 2015, 89, 8816–8827. [CrossRef]
71. Ou, X.; Guanas, H.; Qin, B.; Mu, Z.; Wojdyla, JA; Wang, M.; Dominguezas, SR; Qian, Z.; Cui, S. Žmogaus betakoronaviruso HKU1 smaigalio glikoproteino receptorių surišimo domeno kristalinė struktūra. Nat Commun 2017, 8, 15216. [CrossRef]
72. „Vogel“, AB; Kanevskis, I.; Che, Y.; Swanson, KA; Muikas, A.; Vormehr, M.; Kranz, LM; Walzeris, KC; Heinas, S.; Güleris, A.; ir kt. BNT162b vakcinos apsaugo rezus makakas nuo SARS-CoV-2. Gamta 2021, 592, 283–289. [CrossRef]
73. Džeksonas, Los Andželas; Anderson, EJ; Rouphael, NG; Robertsas, kompiuteris; Makhene, M.; Coler, RN; McCullough, MP; Chappell, JD; Denisonas, MR; Stevensas, LJ; ir kt. MRNR vakcina nuo SARS-CoV-2 – preliminari ataskaita. N. Engl. J. Med. 2020, 383, 1920–1931. [CrossRef]
74. Lawrenz, J.; Xie, Q.; Zechas, F.; Weil, T.; Seidel, A.; Krnavek, D.; van der Hoek, L.; Miunchas, J.; Miuleris, JA; Kirchhoff, F. Sunkaus ūminio kvėpavimo sindromo koronaviruso 2 vakcinacija padidina neutralizuojančią veiklą prieš sezoninius žmogaus koronavirusus. Clin. Užkrėsti. Dis. 2022, 75, e653–e661. [CrossRef]
75. Simulė, ER; Manca, MA; Jasemi, S.; Uzzau, S.; Rubino, S.; Manchia, P.; Bitti, A.; Palermas, M.; Sechi, LA HCoV-NL63 ir SARS-CoV-2 dalijasi pripažintais epitopais pagal humoralinį atsaką žmonių serumuose, surinktuose prieš CoV-2 pandemiją ir jos metu. Mikroorganizmai, 2020, 8, 1993. [CrossRef]
76. Chan, KH; Cheng, VCC; Woo, PCY; Lau, SKP; Poon, LLM; Guanas, Y.; Seto, WH; Yuen, KY; Peiris, JSM Serologiniai atsakai pacientams, sergantiems sunkia ūminio kvėpavimo sindromo koronaviruso infekcija ir kryžminė reakcija su žmogaus koronavirusais 229E, OC43 ir NL63. Clin. Vakcina Imunol. 2005, 12, 1317–1321. [CrossRef]
77. Linas, H.-X.; Feng, Y.; Tu, X.; Zhao, X; Hsieh, C.-H.; Griffin, L.; Junop, M.; Zhang, C. Žmogaus koronaviruso NL63 smaigalio baltymo apibūdinimas surišant receptorius ir viruso pseudotipo patekimą. Virus Res. 2011, 160, 283–293. [CrossRef]
78. Heinzas, FX; Stiasny, K. Skiriamieji dabartinių COVID{1}} vakcinų bruožai: žinomi ir nežinomi antigenų pateikimo ir veikimo būdai. npj Vakcinos 2021, 6, 1–13. [CrossRef]
79. Martínez-Flores, D.; Zepeda-Cervantes, J.; Cruz-Reséndiz, A.; Aguirre-Sampieri, S.; Sampieri, A.; Vaca, L. SARS-CoV-2 Vakcinos, pagrįstos spike glikoproteinu ir naujų virusų variantų pasekmėmis. Priekyje. Immunol. 2021, 12. [CrossRef]
80. Dolgin, E. Pan-Coronavirus Vaccine Pipeline įgauna formą. Nat. Drug Discov. 2022, 21, 324–326. [CrossRef]
