Interleukinas{0}} susieja autoimuninę ir autouždegiminę patofiziologiją mišrioje psoriazėje, 2 dalis
Jun 28, 2023
3.1. Autoimuniniai procesai sergant psoriaze. Autoimuninė
Autoimuniniai procesai sergant psoriaze. Atrodo, kad psoriazės autoimuninį požymį lemia vietiniai ir sisteminiai Th17 modeliai, išreiškiantys IL-17A, IL-22 ir IFN- [10] (3 pav.). Lėtinio stimuliavimo dendritinės ląstelės palaiko pažeistų Th17 ląstelių aktyvaciją ir diferenciaciją, visų pirma išskirdamos IL-23 [15].
Tiek ŽLA restrikcijos, tiek T ląstelių peptidų specifiškumą lemia T ląstelių receptorių repertuaras. Antigeninė stimuliacija sukelia T ląstelių aktyvaciją ir klonų išsiplėtimą. Nesant svetimų antigenų, kloninis T ląstelių išsiplėtimas greičiausiai rodo uždegiminių ligų autoimunitetą [16].
Atrodo, kad psoriazę sukelia lokaliai vyraujantys antigenai [17]. Dažniausiai vertinami aplinkos veiksniai, įskaitant stresą, rūkymą, narkotikus ir infekcijas [18]. Aktyvuotos kloninės T ląstelės sukelia ligos uždegiminį procesą kartu su lokaliai uždegiminiais leukocitais. Pastaraisiais metais sergant psoriaze buvo nustatyti galimi autoantigenai, tokie kaip katelicidinas LL-37, melanocitinis ADAMTSL5, lipidinis antigenas PLA2G4D ir keratinas 17 [19–22].
Psoriazė yra imuninės sistemos sukelta odos liga, kuri turi tam tikrą ryšį su imunitetu.
1. Per didelė imuninės sistemos reakcija
Pacientų, sergančių psoriaze, imuninė sistema gali pernelyg reaguoti, o tai gali sukelti nenormalią citokinų sekreciją ir odos ląstelių metabolizmo disbalansą, dėl ko gali prasidėti liga. Tai rodo, kad normalus imuninės sistemos reguliavimas yra būtinas psoriazės pacientų sveikatai.
2. Sumažėjusi imuninės reguliavimo funkcija
Žvyneline sergančių pacientų imunoreguliacinė funkcija paprastai sumažėja, įskaitant imuninių ląstelių, tokių kaip bendrosios T ląstelės, CD4 plius T ląstelės, CD8 plius T ląstelės ir NK ląstelės, skaičiaus ir aktyvumo sumažėjimą. Tai gali būti susiję su tam tikrais autoantikūnais, imuniniais kompleksais ir kitais veiksniais paciento serume.
3. Susijęs su uždegiminiu atsaku
Psoriazė atsiranda ant odos paviršiaus, o pažeidimas dažnai pasireiškia uždegiminėmis reakcijomis, tokiomis kaip eritema, žvyneliai ir papulės. Todėl jis yra glaudžiai susijęs su su uždegimu susijusiais organizmo veiksniais (pvz., IL-6, TNF-, IL-1 ir kt.). Imuninės sistemos poveikis gali būti glaudžiai susijęs su uždegiminiu atsaku.
Paprastai tariant, imunitetas yra neatsiejamai susijęs su psoriazės atsiradimu ir vystymusi. Gydant žvynelinę svarbiausia yra sureguliuoti imuninės sistemos veiklą, sumažinti uždegiminį atsaką ir užkirsti kelią tolesniam ligos plitimui. Matyti, kad turime gerokai pagerinti imunitetą, kad galėtume atsispirti virusams. Cistanche gali sustiprinti imunitetą. Cistanche taip pat turi antivirusinį ir priešvėžinį poveikį, kuris gali sustiprinti imuninės sistemos gebėjimą kovoti ir pagerinti organizmo imunitetą.

Click cistanche tubulosa privalumai
3.2. Prisitaikančio ir įgimto imuniteto psoriazei susikirtimas.
Sudėtingas įgimtos ir adaptyvios imuninės sistemos susikirtimas su psoriaze prisideda prie antigenui būdingo psoriazės uždegimo paūmėjimo. Besikaupę netiesioginiai įrodymai rodo, kad pacientams, sergantiems stabilia ir lengva psoriaze, adaptyvus imunitetas gali būti labiau paplitęs, o įgimtas imunitetas gali labiau prisidėti prie aktyvios ir sunkios ligos, sisteminio įsitraukimo ir gretutinių ligų [23] (3 pav.). Gretutinių ligų, tokių kaip aterosklerozė, kartu egzistavimas sergant sunkia psoriaze buvo aiškinama kaip sisteminė uždegiminė reakcija į įgimtą vietinį pažeistų audinių uždegimą [24]. Šie veiksniai nėra specifiniai psoriazei, nors jie padidina bendrą uždegiminę naštą pacientams, sergantiems sunkia psoriaze.
Tyrimai, nagrinėjantys IL{0}} ir IL-36-sukeliamo uždegimo sąveiką, gali padėti suprasti, kaip tam tikri mediatoriai įtakoja psoriazės spektrą, pakeisdami įgimtą ar adaptyvų imunitetą [25]. Visos IL-36 izoformos (IL-36, , ir ) priklauso IL-1 šeimai ir yra išreikštos psoriazinėje odoje [26]. Jie jungiasi prie specifinio receptoriaus (IL-1RL2), suaktyvindami NF-κB aktyvindami kelių uždegiminių mediatorių transkripciją.
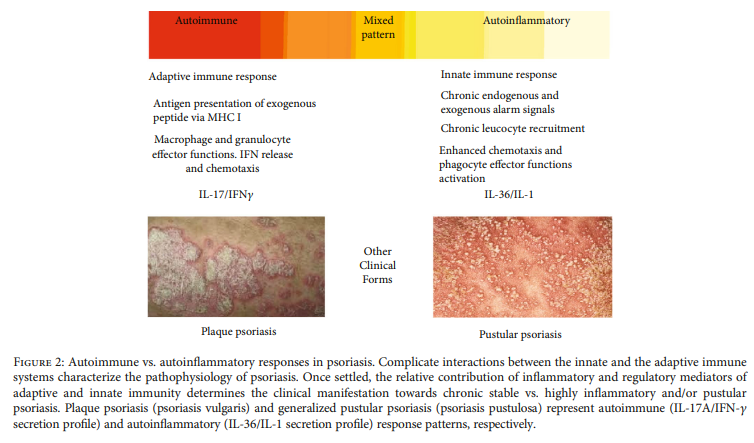
Atrodo, kad IL{0}} yra susijęs su specifinių psoriazės fenotipų klinikiniais pasireiškimais. Oda sergant psoriaze vulgaris labai skiriasi nuo pustulinės psoriazės odos, kuri yra priešingi psoriazės spektro galai. Pusiausvyra tarp IL-36 ir IL-17 gali prisidėti prie skirtingų klinikinių simptomų tarp vulgaris ir pustulosos formų, atsižvelgiant į atsaką į tam tikrą gydymą [27].
IL-23/IL-17 ašis yra labai svarbi, nes ji apima įgimtą imunitetą (IL-23-gaminančias mieloidines ląsteles) ir adaptyvųjį imunitetą (Th17- ir IL-17- ekspresuojančios CD8 plius T ląsteles). Psoriazės supratimas gali padėti išsiaiškinti tokius santykius.
3.3. Apie tai, kaip IL-1 ir IL-8 dalyvauja IL-12/23 suaktyvinant Th1 ir Th17.
Kai kurie citokinai, įskaitant IL-1, skatina IL-17 išsiskyrimą žmogaus T limfocituose. Jų gebėjimas skatinti Th17 ląsteles priklauso ne tik nuo dendritinių ląstelių IL-23, IL-6 ir TGF- indukcijos, bet ir nuo tiesioginio ar netiesioginio uždegimo aktyvavimo ir IL-1 .
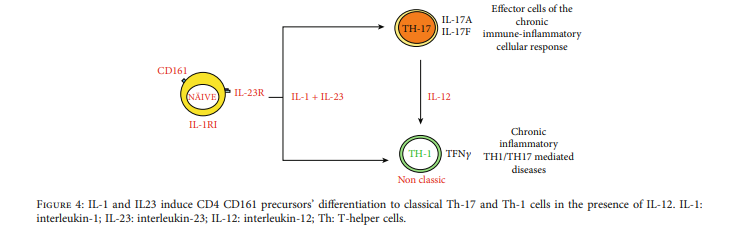
IL-12 ir IL-23 yra nepaprastai svarbūs atitinkamai Th1 ir Th17 indukcijai, o jų gamyba, kurią sukelia antigeną pateikiančios ląstelės, yra aiškiai reguliuojama. Įgimti imuniteto dirgikliai reguliuoja IL-12 ir IL-23 gamybą, darydami įtaką sukeltam T limfocitų fenotipui. IL23 skatina IL-23R ekspresiją mieloidinėse ląstelėse ir skatina priešuždegiminį TNF ir IL-1 citokinų gamybą. Be to, IL-23 skatina CD4 ir pirmtakų diferenciaciją iki Th17 efektoriaus, kai nėra IFN ir IL-4 [28].
IL-1 skatina limfocitų augimą ir diferenciaciją. Skirtinga IL1R1 ekspresija CD4 T limfocitų potipiuose suteikia skirtingas efektorines funkcijas.
Th17 ląstelių atsakas į IL-12 ir ilgalaikis IL-23 poveikis skatina Th17 pasikeitimą į Th1 fenotipą [29], o tai rodo stiprų poveikį aplinkai [30]. Th17- gautos Th1 ląstelės vadinamos „neklasikine Th1“ ir išreiškia CD161 ir IL1R1 [31]. IL-1 ir IL-23 derinys skatina T ląstelių gamybą su Th17 ir Th1 fenotipu CD4 plius CD161 plius ir CD4 plius CD161- ląstelių frakcijose. Tai rodo, kad Th1 ląstelės reaguoja į IL-1 ir kad CD4 ir CD161 plius klonai uždegiminiame audinyje gali gaminti IFNgamma ir ekspresuoti IL1R1 mRNR [32].
IL-8 (CXCL8) dalyvauja psoriazės patofiziologijoje, pritraukiant neutrofilus ir kitus uždegiminius leukocitus. IL-8 labai pasireiškia plokšteline psoriaze ir iki dešimt kartų – pustuline psoriaze [25].
IL-36, labai išreikštas plokšteline psoriaze, veikia keratinocitus ir mieloidines dendritines ląsteles [33] ir yra stiprus neutrofilų CXCL1 ir IL-8 chemotaktinių citokinų induktorius. Infiltruojantys neutrofilai vaidina pagrindinį vaidmenį psoriazės apnašose, sustiprindami IL-36-sukeliamą autouždegiminę kilpą sergant psoriaze [13].

4. Inflammasomų asociacija su įgimtu ir adaptyviu imunitetu
Inflammasomos yra trišaliai kompleksai, susidedantys iš citoplazminio jutiklio, adapterio, žinomo kaip ASC, ir procaspase1. Uždegimas apibrėžiamas pagal jų citoplazminį jutiklį, kuris apima AIM2, Pyrin, NLRP1, NLRP3 ir NLRC4 ir priklauso NOD2- panašių receptorių šeimai. Jutiklių įvairovė ir specifiškumas leidžia uždegiminėms medžiagoms reaguoti į įvairius išorinius (mikrobinės molekulės) arba vidinius (pavojaus signalus) dirgiklius.
NLRP3 uždegimas yra prototipinis ir geriausiai apibūdinamas uždegimas, o jo aktyvacija buvo sekvenuota [34]. Pirmasis signalas, pradinis, kurį teikia mikrobų molekulės, tokios kaip lipopolisacharidas, sukelia NLRP3 ir pro-IL1 ekspresiją priklausomai nuo NF-κB. Mikrobų molekulės, pvz., toksinai, arba pavojaus signalai, tokie kaip mononatrio uratas, suteikia antrąjį signalą ir sukelia multimerizaciją, kad susidarytų uždegimas (4 pav.).
NLRP3 susijungia į ASC, todėl suaktyvinama kaspazė-1, o tai sukelia proteolitinį IL-1 ir IL-18 brendimą ir Gasdermin D skilimą. Kitas Gasdermin D porų susidarymas ląstelės membranoje sukelia piroptozę, greitą priešuždegiminę ląstelių mirtį [35]. Piroptozė, susijusi su IL-1, IL-18 ir alarminų išsiskyrimu, prisideda prie pavojaus signalo sklidimo už pažeistos ar užkrėstos ląstelės ribų, įdarbindama mono- ir polimorfonuklearinius fagocitus (3 pav.). Iš uždegimo gali išsiskirti oligomerinės dalelės, kurios dar labiau sustiprintų uždegiminį atsaką po aplinkinių makrofagų fagocitozės.
Nepažeistuose fagocituose IL-1 sekrecija gali vykti nepriklausomai nuo piroptozės. Autofagija reguliuoja uždegimo apdorotus citokinus, kurie sukelia IL-17. Autofagija įvairiuose etapuose susikerta su nuo uždegimo priklausančia IL-1 ir IL-18 karta. Autofagosomos gali pašalinti endogeninius uždegimą aktyvinančius dirgiklius, įskaitant mitochondrijų DNR, ROS, pažeistas lizosomas, pro-IL-1 ir uždegiminius komponentus. Autofagija slopina IL-23 sekreciją dėl jos poveikio IL-1 [36].
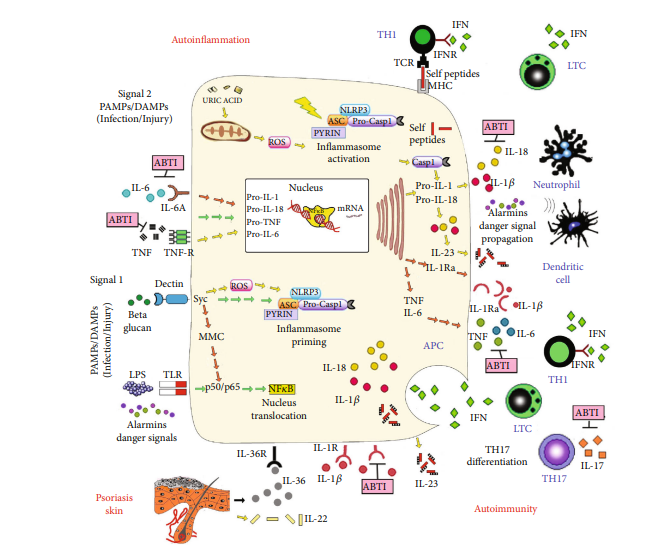
3 paveikslas. Scheminis uždegiminių signalų perdavimo mechanizmų vaizdas sergant mišriomis uždegiminėmis ligomis. Uždegiminės medžiagos ir patogenai sukelia kanoninį uždegimo kelią. PAMP ir DAMP aptinka specifiniai įgimti imuniniai jutikliai, dėl kurių atsiranda oligomerizacija ir uždegimas. Autouždegiminių ligų terapiniai taikiniai yra tokie: 1 signalo uždegiminis aktyvinimas: paviršiaus modelio atpažinimo receptoriai, tokie kaip Toll tipo receptoriai (TLR) ir su patogenais susiję molekuliniai modeliai, skatina molekulių, tokių kaip NF-κB, gamybą ir aktyvina uždegiminių procesų susidarymą per paskesnius imunologinius procesus. ; 2 signalo uždegiminis aktyvinimas: kristalai podagra, karščio šoko baltymai ir pažeisti audiniai, kaip ir nudegimų atveju, kitas su patogenu ir pažeidimu susijęs molekulinis modelis, aktyvina uždegiminį susikaupimą per reaktyviųjų deguonies rūšių (ROS) gamybą ir paskesnius imunologinius procesus. Tam tikri mediatoriai įtakoja psoriazės spektrą, pereina į įgimtus arba adaptacinius imuninius procesus.
Atrodo, kad IL-17- ir IL-36-sukeltas uždegimas yra susijęs su įgimta adaptyvia imunine pusiausvyra. Uždegimo sukeltos hiperaktyvios dendritinės ląstelės (DC) sukelia sustiprintus T ląstelių atsakus, išsaugodamos antigeno ir autoantigeno pateikimą bei kontekstualizdamos T pagalbinių ląstelių atsaką per IL-1, IL-18 ir IL-23 sekreciją. Šie citokinai sukelia Th1/Th17 atsaką. IL-18 sustiprina Th1 ląstelių IFN gamybą ir sustiprina Th1 diferenciaciją, o IL-1 skatina Th17 poliarizaciją ir IL-17 sekreciją, sukeldamas mišrią autouždegiminę-autoimuninę patologiją.
Paveikslėlyje parodytos galimos antikūnais pagrįstos terapinės intervencijos (ABTI) vietos. ASC: su apoptoze susijęs dėmių baltymas; ER: endoplazminis tinklas; IFNAR: su interferonu susijęs receptorius; IFN: interferonas; IL-1: interleukinas1; IL-1 R: IL-1 receptorius; IL-1Ra: IL-1 receptorių antagonistas; IL-6: interleukinas 6; IL-6R: IL-6 receptorius; IL-18: interleukinas-18; JAK: Janus kinazė; NLRP3: į NOD panašus receptorius P3; ROS: reaktyviosios deguonies rūšys; TLR: į rinkliavą panašus receptorius; TNF: naviko nekrozės faktorius; TNF-R: TNF receptorius; ASC: su apoptoze susijęs taškelių pavidalo baltymas, turintis CARD; KORTELĖ: caspase recruitment domenas; DAMP: su pažeidimu susijęs molekulinis modelis; LPS: lipopolisacharidas; NLR: į NOD panašus receptorius; NOD: nukleotidus surišantis oligomerizacijos domenas; PAMP: su patogenu susijęs molekulinis modelis; PYD: pirino domenas; MMC: daugiamolekulinis kompleksas; HMGB1: didelio mobilumo grupės 1 dėžutė; TCR: T ląstelių receptorius.
Dalyvavimas įvairiose patofiziologinėse sąlygose sukelia uždegimus kaip įdomius antikūnais pagrįstos terapinės intervencijos taikinius (3 pav.). Žvelgiant iš patogenetinės perspektyvos, jiems būdingas lėtinis imuninės sistemos aktyvinimas, sukeliantis audinių uždegimą genetiškai linkusiems asmenims. Tačiau žalai būdingi efektoriai yra skirtingi. Sergant autouždegiminėmis ligomis, įgimta imuninė sistema tiesiogiai sukelia audinių uždegimą, o esant autoimuniniams sutrikimams, įgimta imuninė sistema aktyvina adaptyviąją imuninę sistemą, galiausiai atsakingą už uždegiminį procesą [37].
Kai kurios ligos turi mišrią autoimuninę-autouždegiminę šaknį [38]. Uždegiminis reguliavimas yra susijęs su autouždegiminėmis ir autoimuninėmis ligomis, tokiomis kaip šeiminė Viduržemio jūros karštligė, reumatoidinis artritas, psoriazė ir sisteminė raudonoji vilkligė [4, 39]. Kai kurios imuninės-uždegiminės ligos gali atspindėti kintamą patogenetinių autouždegiminių ir autoimuninių veiksnių išraišką [40].
Bandydama paaiškinti, Polly Matzinger pateikė pavojaus signalo teoriją. Tai rodo, kad imuninė sistema ne tiek atskirtų endogeninius ir egzogeninius signalus, bet padidintų atsaką į pavojaus signalus, nepaisant to, ar tai egzogeninės patogeninės bakterijos, ar endogeniniai pažeisti audiniai [41]. Tačiau pavojaus modelis nepakankamai paaiškina išskirtinį adaptyvaus imuninio atsako specifiškumą sergant autoimuninėmis ligomis. Naujausi genetinių ir molekulinių tyrimų pažanga leidžia suartėti su vieninga visų imunologinių ligų klasifikacija teorinėje sistemoje. Psoriazė, ankilozuojantis spondilitas, Behceto sindromas, uveitas ir kitos ligos pasireiškia įvairiais būdais.
Uždegiminės hiperaktyvuotos dendritinės ląstelės sukelia sustiprintą T-ląstelių atsaką. Jie išsaugo savo antigeno pateikimo funkciją ir kontekstualizuoja T pagalbinių ląstelių atsaką per IL-1 ir IL-18 sekreciją. Šie citokinai ypač skatina Th1/Th17 atsaką. IL-18 sustiprina Th1 ląstelių IFN gamybą, o IL-1 skatina Th17 poliarizaciją ir IL-17 sekreciją [42] (3 pav.).
Nuo uždegimo priklausomi IL{1}} Th17 atsakai yra būtini šeimininko gynybai nuo grybelių, tokių kaip Candida albicans, infekcijų. C tipo lektinai Dektinas{4}} dalyvauja šeimininko gynybos mechanizmuose nuo grybelinės infekcijos, skatina uždegiminius ir adaptyvius imuninius atsakus. Dektinas{5}} yra C tipo lektino receptorius, aptinkantis gliukanus [43]. Tai veda prie nuo Syk priklausomo NF-κB aktyvacijos ir NLRP3 uždegimo susidarymo, o Th17 atsakai suteikia imuninę apsaugą nuo patogeno [44]. Pažymėtina, kad dektino{14}} signalizacija taip pat suaktyvina IL-1 gamybą per nekanoninę kaspazės{16}} uždegimą [45].
Skirtingi IL{0}} ir IL-18 vaidmenys adaptyvaus imuniteto kūrime atkreipė daug dėmesio į uždegimus kaip vakcinų adjuvantus. Th1-tarpininkaujamas humoralinis atsakas, citotoksinis T ląstelių/Th1/Th17 imunitetas ir imuninė atmintis gali būti manipuliuojami naudojant uždegimą aktyvuojančius ligandus [46]. I tipo interferonai slopina pro-IL-1 sintezę, skatina IL-18 brendimą ir kartu su uždegimo aktyvavimu gali padėti modeliuoti apsauginius Th1 atsakus [47]. Vakcinos adjuvantas chitozanas yra katijoninis polisacharidas, sukeliantis I tipo IFN gamybą, NLRP3 uždegimo aktyvavimą ir intensyvų Th1 atsaką. Reikia daugiau tyrimų, kad būtų galima geriau suprasti uždegimų vaidmenį patologiniame ir apsauginiame imunitete.

Apoptozė ir piroptozė yra du gerai ištirti ląstelių mirties modeliai, kurie tradiciškai laikomi nesusijusiais. Nauji įrodymai rodo, kad jų platus tarpusavio ryšys yra susiliejantys keliai, aktyvuojantys tą patį ląstelių mirties efektorių – poras formuojantį baltymą Gasdermin D [48].
Piroptozė yra uždegiminė ląstelių mirtis, kurią sukelia tarpląstelinis pažeidimo ar patogenų aptikimas [49]. Piroptozinėse ląstelėse pasireiškia patinimas, genetinės medžiagos fragmentacija, membranos porų susidarymas, plazmos membranos plyšimas ir uždegiminių mediatorių bei citoplazminio turinio išsiskyrimas į tarpląstelinę erdvę [50]. Lipopolisacharidas, gramneigiamų bakterijų ląstelės sienelės požymis, yra prototipinis imuninių ląstelių piroptozės sukėlėjas. Piroptozė prasideda įgimtu TLR4 aktyvinimo žingsniu. Tai skatina NF-κB aktyvaciją ir perkėlimą į branduolį, kad padidėtų pirmtakų pro-IL-1, pro-IL-18 ir procaspazių genų transkripcija bei tarpląstelinių Nod tipo receptorių transkripcija. Atrodo, kad esant psoriaziniams pažeidimams, dektino{10}} reguliavimą kontroliuoja su psoriaze susiję citokinai, o jo vaidmuo odos uždegimų ir infekcijų biologijoje turi būti ištirtas [51].
Antrasis signalas sukelia intracelulinių kompleksų, vadinamų uždegiminėmis [52], oligomerizaciją, kuri palengvina pro-IL-1 ir procaspazės-1 brendimą į aktyvias formas. Nors IL-1 išsiskiria ir sukelia priešuždegiminę būseną, kaspazė-1 suardo citoplazminį gasderminą D, suformuodama poras membranoje ir sukeldama ląstelių mirtį dėl citoplazminių komponentų nutekėjimo.
Autofagija yra savaime ardantis procesas, reikalingas ląstelių homeostazei atkurti, kai aptinkami grėsmingi veiksniai [53]. Šis visur esantis lizosomų skaidymo mechanizmas pašalina pažeistus baltymus ir organelius, prisideda prie antigeno pateikimo ląstelės paviršiuje, apsaugo nuo genomo nestabilumo ir apsaugo nuo audinių pažeidimo. Autofagija yra fiziologiškai svarbi, nes ji padeda apsisaugoti nuo žalingo streso ir sukelia patologiją, kai jos perteklius arba trūkumas [54].
Kaip esminis homeostatinis mechanizmas, autofagija yra reguliuojama reaguojant į aplinkos ir farmakologinius veiksnius. Jis turi labai svarbų vaidmenį sergant vėžiu, neurodegeneracija, diabetu, kepenų ir autoimuninėmis ligomis. Molekuliniai elementai, lemiantys tokio tipo ląstelių mirtį, taip pat bendradarbiauja reaguojant į stresą.
Imuninėje sistemoje autofagija yra antigeno pateikimo peptidų šaltinis [55], užtikrina tarpląstelinių patogenų absorbcijos ir skilimo mechanizmą ir yra pagrindinis uždegiminių citokinų reguliatorius. Jis taip pat dalyvauja reguliuojant uždegimo aktyvavimą ir padeda pašalinti uždegimo komponentus bei endogeninius aktyvatorius [56] ir vaidina vaidmenį nustatant IL-1 likimą autofagosomose. Dabartinis supratimas rodo, kad autofagija yra esminis uždegimo aktyvacijos ir IL-1 šeimos citokinų išsiskyrimo reguliatorius [57].
5. Uždegimo sukeltas IL-1 skatina IL-17-tarpininkaujantį atsaką
Inflammasoma yra daugelio baltymų kompleksas, padedantis apsisaugoti nuo patogenų ir atstatyti uždegiminių procesų metu, tuo pačiu sukeliantis uždegimines ligas esant nenormalioms lėtinėms ligoms. Uždegiminė sąranka suaktyvina kaspazes, sukeldama uždegiminius citokinus, įskaitant IL-1 aktyvavimą.
IL{0}} ir IL-17- išskiriančių T ląstelių atradimas pagerino mūsų supratimą apie T ląstelių vaidmenį sergant autoimuninėmis ir kitomis uždegiminėmis ligomis. Th1 ląstelės pirmiausia buvo laikomos pagrindinėmis patogeninėmis T ląstelėmis daugelyje autoimuninių ligų. Tačiau pelėms, kurioms stinga IFN arba IL-12 signalų, tam tikrų autoimuninių ligų simptomai paūmėjo [58].
Dendritinės ląstelės, susijusios su uždegiminiu hiperaktyvumu, padidina T limfocitų aktyvumą (Th1/Th17), padidindamos IL-1, IL-18 ir IL-23 išsiskyrimą. IL-18 sustiprina Th1 ląstelių IFN gamybą ir sustiprina Th1 diferenciaciją, o IL-1 skatina Th17 poliarizaciją ir IL-17 išsiskyrimą, sukeldamas patologinį autouždegiminį ir autoimuninį profilį.
Be to, IL-1 ir IL-23 (4 pav.) gali sukelti ir aktyvuoti žmogaus Th1/Th17 ląstelių diferenciaciją. IL-1 gali paskatinti įgimtos imuninės sistemos ląsteles gaminti IL-6, o tai skatina naivių T ląstelių diferenciaciją iki Th17 [59].
6. Išvados
Žvelgiant iš patogeninės perspektyvos, dauguma autouždegiminių ir autoimuninių ligų pasižymi lėtiniu nenormaliu imuninės sistemos aktyvavimu, kuris sukelia audinių uždegimą ir įvairaus masto pažeidimus genetiškai linkusiems asmenims. IL-1 išaugo į sudėtingą, daugialypę citokinų šeimą su sudėtingais reguliavimo mechanizmais ir įvairiomis sveikatos bei ligų funkcijomis.
IL-1 ir uždegimas yra stipriai susiję su adaptaciniais ir autoimuniniais sutrikimais. Su uždegimu susijusių IL-1 citokinų šeimos vaidmuo formuojant adaptyvųjį imuninį atsaką dabar yra gerai žinomas dėl Th17 ląstelių diferenciacijos ir Th1 ląstelių bei CD8 T ląstelių efektorinių funkcijų skatinimo. Be to, ląstelių lizė sukelia uždegiminį aktyvavimą, išskirdama papildomus DAMP ir savaiminius antigenus, susiejančius autouždegimą ir autoimunitetą. Reikia ištirti IL-1 ir susijusių molekulių indėlį į uždegimo reguliavimą, kad galėtume geriau suprasti uždegimines ligas.
Su IL1-susijusių citokinų svarba pranoko klasikinę imunopatologiją ir yra svarbus tiltas siekiant suprasti mišrias ligas.
Pagilinus mūsų supratimą apie uždegiminius sutrikimus ir autouždegimo, autoimuniteto ir imuninės homeostazės reguliavimo molekulinius kelius, galima tikėtis naujų terapinės intervencijos strategijų.

Duomenų prieinamumas
Duomenys, patvirtinantys šią apžvalgą, yra iš anksčiau pateiktų tyrimų, kurie buvo cituoti.
Interesų konfliktai
Autoriai deklaruoja, kad nėra interesų konflikto.

Autorių įnašai
Rodolfo Kölliker Frers ir Tamara Kobiec pasidalino autoriais.
Padėkos
Šį darbą parėmė Grants of CONICET (PIP 0779 2016–2022), Universidad de Buenos Aires (UBACyT 2017–2022) ir FONCyT (PICD 0031 2016-2022), Argentina.
Nuorodos
[1] DE Smilek ir EW St Clair, „Autoimuniteto galvosūkio sprendimas: kritiniai klausimai“, F1000Prime Reports, t. 7, p. 2015 m. 17 d.
[2] D. McGonagle ir MF McDermott, „Siūloma imunologinių ligų klasifikacija“, PLoS Medicine, vol. 3, Nr. 8, e297 straipsnis, 2006 m.
[3] G. Lopalco, L. Cantarini, A. Vitale ir kt., "Interleukinas{1}} kaip bendras vardiklis nuo autouždegiminių iki autoimuninių sutrikimų: patalpos, pavojai ir perspektyvos", Mediators of Inflammation, t. 2015 m., Straipsnio ID 194864, 21 psl., 2015 m.
[4] S. Tartey ir TD Kanneganti, „Uždegimai autouždegiminių sindromų patofiziologijoje“, Journal of Leukocyte Biology, vol. 107, Nr. 3, p. 379–391, 2020 m.
[5] CA Dinarello, IL-1 citokinų ir receptorių šeima sergant reumatinėmis ligomis, Nature Reviews Rheumatology, vol. 15, Nr. 10, 612–632 p., 2019 m.
[6] C. Garlanda, F. Riva, E. Bonavita ir A. Mantovani, „Neigiami IL-1 šeimos reguliavimo receptoriai“, Seminars in Immunology, t. 25, Nr. 6, p. 408–415, 2013 m.
[7] A. Mantovani, CA Dinarello, M. Molgora ir C. Garlanda, "Interleukin-1 and Related Cytokines in the Regulation of Inflammation and Immunity", Imunity, t. 50, Nr. 4, p. 778–795, 2019 m.
[8] WH Boehncke ir W. Sterry, „Psoriazė – sisteminis uždegiminis sutrikimas: klinika, patogenezė ir gydymo perspektyvos“, Journal der Deutschen Dermatologischen Gesellschaft, vol. 7, Nr. 11, p. 946–952, 2009 m.
[9] K. Schäkel, MP Schön ir K. Ghoreschi, „Pathogenese der psoriazė vulgaris [psoriazės patogenezė]“, Der Hautarzt, vol. 67, Nr. 6, p. 422–431, 2016 m.
[10] WH Boehncke ir MP Schön, „Psoriasis“, Lancet, t. 386, Nr. 9997, 983–994 p., 2015 m.
[11] JC Prinz, „Žmogaus leukocitų antigeno I klasės aleliai ir autoreaktyvus T ląstelių atsakas psoriazės patogenezėje“, Frontiers in Immunology, vol. 9, p. 954, 2018 m.
[12] Y. Liang, MK Sarkar, LC Tsoi ir JE Gudjonsson, „Psoriazė: mišri autoimuninė ir uždegiminė liga“, Current Opinion in Immunology, vol. 49, 1–8 p., 2017 m.
[13] AM Foster, J. Baliwag, CS Chen ir kt., „IL-36 skatina mieloidinių ląstelių infiltraciją, aktyvaciją ir uždegiminį aktyvumą odoje“, Journal of Immunology, vol. 192, Nr. 12, 6053–6061 p., 2014 m.
[14] B. Germán, R. Wei, P. Hener ir kt., „IL-36 ir IL-23/IL-17 kilpos sutrikimas yra kalcipotriolio ir kortikosteroidų terapijos veiksmingumo pagrindas. psoriazei“, JCI Insight, t. 4, Nr. 2, straipsnis e123390, 2019 m.
[15] MP Schön ir L. Erpenbeck, „Interleukino-23/interleukino-17 ašis jungia adaptyvųjį ir įgimtą imunitetą sergant psoriaze“, Frontiers in Immunology, vol. 9, p. 1323, 2018. [16] DJ Woodsworth ir M. Castellarin, "Holt apžvalgos sekų analizė T-ląstelių repertuaruose sveikatos ir ligų srityje", Genome Medicine, vol. 5, Nr. 10, p. 98, 2013 m.
[17] SM Kim, L. Bhonsle, P. Besgen ir kt., "Pavienių žmogaus T ląstelių suporuotų TCR ir grandinių analizė", PLoS One, t. 7, Nr. 5, straipsnis e37338, 2012 m.
[18] M. Roszkiewicz, K. Dopytalska, E. Szymańska, A. Jakimiuk ir I. Walecka, "Aplinkos rizikos veiksniai ir epigenetiniai psoriazės pokyčiai", Annals of Agricultural and Environmental Medicine, vol. 27, Nr. 3, p. 335–342, 2020 m.
[19] H. Valdimarsson, RH Thorleifsdottir, SL Sigurdardottir, JE Gudjonsson ir A. Johnston, „Psoriazė – kaip autoimuninė liga, kurią sukelia molekulinė mimikrija“, Trends in Immunology, vol. 30, Nr. 10, 494–501 p., 2009 m.
[20] JM Kahlenberg ir MJ Kaplan, „Mažai peptidų, didelis poveikis: LL-37 vaidmuo uždegime ir autoimuninėse ligose“, Journal of Immunology, t. 191, Nr. 10, 4895–4901 p., 2013 m.
For more information:1950477648nn@gmail.com
