2 dalis: Natūralių ir sintetinių chalkonų priešvėžinė veikla
Mar 16, 2022
Spustelėkite nuorodą, kad gautumėte 1 dalį:https://www.xjcistanche.com/news/part1-anticancer-activity-of-natural-and-synt-54977104.html
Norėdami gauti daugiau informacijos, kreipkitėstina.xiang@wecistanche.com
3. Priešvėžinė veikla
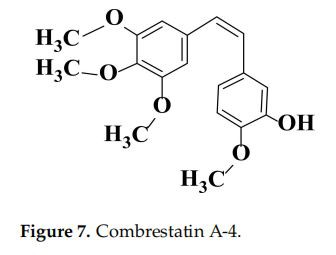
Chalkonasdariniai veikia įvairius taikinius, tokius kaip aromatazė, ATP surišimo kasetės pošeimys G narys 2 (ABCG2), krūties vėžiui atsparus baltymas (BCRP), aktyvuotas branduolio B ląstelių augimo faktorius (NF-kB), kraujagyslių endotelio augimo faktorius (VEGF) ir tirozino kinazės receptoriai (epiderminio augimo faktoriaus receptorius (EGFR) ir mezenchiminio epitelio pereinamojo laikotarpio faktorius (MET), pasižymintys svarbiu aktyvumu in vitro ir in vivo sergant jautriais ir terapijai atspariais vėžiais [161,162]. Svarbus chalkonų antiproliferacinio aktyvumo mechanizmas yra slopinimas tubulino ir šių junginių įsikišimo į mikrotubulių, elementų, būtinų palaikyti ląstelių formą ir funkciją mitozės ir ląstelių replikacijos procesuose, sankaupą. Chalkonai blokuoja ląstelių ciklą ir skatinaapoptozė. Trimetoksifenilo liekanos buvimas chalkono molekulėse yra palankus šių junginių negrįžtamam antimitoziniam aktyvumui, kurie gali sąveikauti su cisteino liekanomis tubuline per Michael tipo adityvinę reakciją [163]. Be to, trimetoksifenilo likučių pakeitimas chalkonuose chinolinu arba chinazolinu yra palankus antitubulino aktyvumui. Šie heterocikliniai chalkonai sudaro vandenilinius ryšius su likusia Cys241 dalimi ir stipriai jungiasi prie kolchicino surišimo vietos (panašiai kaip kombretastatinas A-4, 7 pav.) [164,165].

3.1. Natūralūs chalkonai, turintys priešvėžinių savybių 3.1.1. Likochalkonai (AD)
Kai kurių Glycyrrhiza rūšių šaknys ir šakniastiebiai naudojami tradicinėje medicinoje skrandžio opoms, astmai ir uždegimams gydyti. Iš saldymedžio išskirta daugiau nei 600 junginių, kurių pagrindinės biologiškai aktyvios sudedamosios dalys yra saponinai irflavonoidų. Tarp flavonoidų buvo nustatyta keletas retrochalkonų, A, B, C, D, E ir G bei schemos. Yra daug tyrimų apie saldymedžio veikliųjų junginių biologinį poveikį, iš kurių svarbiausiapriešuždegiminis, antimikrobinės, antioksidacinės, priešopinės, citoprotekcinės ir citotoksinės savybės [166,167].
3.1.2. Likochalkonas A
Likochalkonas A (LA, S1 ir S2 lentelės, 1 junginys) yra flavonoidas, išskirtas iš Glycyrrhiza urakensis, G.glabra ir G.inflata (Fabaceae). Tai turipriešnavikinis, priešuždegiminės, antimikrobinės, antiparazitinės, nutukimą mažinančios, antioksidacinės ir antiosteoporozės savybės,PriešvėžinisLA poveikis buvo įrodytas įvairių tipų vėžio ląstelėms, įskaitant skrandžio vėžio ląsteles BCG-823, HepG2, OVCAR-3 ir SK-OV-3 (kiaušidžių vėžio ląsteles) MCF{{ 5}} ir A549 [168-171]. Tyrimai rodo, kad LA sukelia U87 gliomos ląstelių, nosiaryklės vėžio ląstelių, epitelio kiaušidžių karcinomos ląstelių ir šlapimo pūslės vėžio ląstelių apoptozę. Chalkonas taip pat turi savybę padidinti autofagiją ir blokuoti ląstelių ciklą krūties vėžio ląstelėse. Be to, jis sukelia apoptozę slopindamas specifinį baltymą 1 sergant krūties vėžiu [172]. LA turi mažą citotoksiškumą embrioninėms plaučių fibroblastų ląstelėms. Be to, jis gali slopinti naviko augimą ir susilpninti cis-platinos sukeltą toksiškumą[173]. Mechanizmai, kuriais flavonoidai veikia kaip priešvėžiniai vaistai, apima Akt aktyvumo slopinimą slopinant heksokinazės -2-sukeliamą naviko glikolizę sergant skrandžio vėžiu, metaloproteinazės 2 ekspresijos reguliavimą ir apoptozės indukciją burnos vėžio ląstelėse, padidintą miR{16} }p sukelti stresą endoplazminiame tinkle ir sukelti apoptozę žmogaus plaučių ląstelėse, sumažinti PI3K/Akt/mTor aktyvaciją ir autofagiją sergant krūties vėžiu, blokuoti ląstelių ciklo G2/M fazę, slopinti MEK/ERKand ląstelių invaziją. ADAM9 signalizacijos keliai žmogaus gliomos ląstelėse ir nuo kaspazės priklausomos apoptozės sukėlimas žmogaus kepenų ląstelėse [174]. Kitas mechanizmas, kuriuo LA turi stiprų citotoksinį poveikį, yra ROS sukelta apoptozė. Pavyzdžiui, chalkonas sukelia oksidacinį stresą ir atitinkamai T24 ląstelių (ląstelių linijų, gautų iš žmogaus šlapimo pūslės karcinomos) apoptozę per nuo mitochondrijų priklausančius kelius ir sukeldamas oksidacinius procesus endoplazminiame tinkle [175]. Kitas LA citotoksiškumo ir genotoksiškumo tyrimas buvo atliktas Bortolotto ir kt. LA buvo lyginamas su trans-chalkonu (S1 ir S2 lentelės, 2 junginys). Natūralių chalkonų (LA ir trans-chalkono) citotoksiškumas MCF-7 ir 3T3 (embrioninių fibroblastų ląstelių linijos) buvo nustatytas 24 ir 48 val. Rezultatai rodo ryškų citotoksinį aktyvumą po 48 valandų gydymo. Citotoksiškumo MTT (3-[4,5-dimetiltiazol-2-il]-2,5-difeniltetrazolio bromidas) tyrimas parodė nuo dozės priklausomą atsaką į MCF{ {45}} ląstelės, apdorotos trans-chalkonu ir LA. Nustatyta, kad analizuotų junginių genotoksiškumas MCF-7 ląstelėse yra geresnis, palyginti su 3T3 ląstelėmis. DNR iškraipymas sukeliaImuninė sistemaaktyvuoti, kad būtų pašalintos sunaikintos ląstelės. Tačiau imuninės sistemos aktyvinimas, siekiant sumažinti degradavusias DNR ląsteles, prisideda prie lėtinio uždegiminio proceso. Be to, ląstelių atsakas į degraduotą DNR gali būti koreguojamas sukeliant vidinį apoptotinį kelią. G1 fazė yra būsena prieš DNR replikaciją, kai tokie veiksniai kaip ląstelių sąlygos (medžiagų apykaita, signalizacija ir ląstelės dydis) turi įtakos ląstelių ciklo progresui, sukeldami DNR atkūrimą ląstelėse arba inicijuodami apoptozės procesą. LA IC50 yra 60,46 uM. Trans-chalkonas sukelia ląstelių ciklo blokadą G1 fazėje ir sustiprina ląstelių apoptozę. Buvo pasiūlyta, kad gydymas LA ir trans-chalkonu sukelia apoptozę per mitochondrijų kelią, atsižvelgiant į tai, kad esminiai šio kelio genai, tokie kaip baltymo apoptozės proteazės aktyvatoriaus 1 faktorius ir baltymas X, susiję su Bcl{{, įvyksta po 24 valandų. 9}}. Nors žinoma, kad MCF-7 ląstelių linijose trūksta kaspazės 3, tyrimas parodė, kad gydymas šiais chalkonais skatina poli (ADP-ribozės) polimerazės (PARP) skilimą – polimerazę, kurios skilimas į du fragmentus yra rodiklis. apoptozės. Represijos
Bcl-2 genas LA ir trans-chalkonas eksperimentinės PGR analizės metu parodė, kad baltymų lygiu į MCF-7 ląsteles patenka nuo dozės priklausomas poveikis ir vidinis tarpininkavimas. Ciklinas D1 yra dar vienas baltymas, slopinamas MCF{5}} ląstelių linijose esant chalkonams. Šis baltymas yra labai svarbus progresuojant nuo G1 iki S fazės ir yra svarbus kai kurių vėžio rūšių, įskaitant krūties vėžį, biomarkeris. Dėl šių priežasčių ciklino D1 skilimas yra patrauklus taikinys naujų priešnavikinių medžiagų identifikavimui ir koreliuoja su ląstelių ciklo blokada [176].
Qui ir kt. taip pat ištyrė LA poveikį plaučių vėžio ląstelėms in vitro. Gydymas flavonoidais reikšmingai sumažino A549 ir H460 ląstelių gyvybingumą (žmogaus nesmulkialąstelinė plaučių karcinoma), šį pokytį stipriai įtakoja dozė. Iš viso 40 μM likohalkono slopina plaučių vėžio ląstelių augimą 45-80 proc. po 24 arba 48 valandų gydymo. Be to, junginys pasižymi mažu citotoksiškumu normalioms žmogaus plaučių epitelio ląstelėms. Siekiant pabrėžti, ar vienas iš LA slopinimo plaučių vėžio ląstelių augimą mechanizmų yra ląstelių ciklo blokada, ląstelių linijos buvo apdorotos skirtingais junginio koncentracijos 16 val., tada ląstelių ciklas buvo analizuojamas srauto citometrija. Rezultatai rodo, kad, priklausomai nuo dozės, chalkonas blokuoja G2/M fazę ant A549 ir H460 ląstelių. Vėliau LAin vaidmuo, sukeliantis apoptozę, buvo įvertintas naudojant aneksiną. /propidžio jodido kolorimetrinis metodas. Rezultatai rodo, kad LA gydytoje grupėje yra apoptozinių ląstelių kaupimasis, kuris priklauso nuo naudojamos koncentracijos. Be to, baltymų kiekiai su apoptoze buvo tiriami Western blot metodu. Skaldyto PARP ir suskaldytos kaspazės 3 lygis yra padidėjęs, o prieškaspazės 3 antiapopotiniai baltymai PARP, Bcl-xL ir Bcl-2 sumažėja praėjus 20 val. po gydymo chalkonu. Šie rezultatai rodo, kad LA sukelta apoptozė yra susijusi su PARP/Bcl{20}} keliu[177]. Molekuliniai modeliai parodė, kad LA buvo pritvirtinta prie ATP surišimo EGFR kišenėse, įskaitant 19 egzono delecijos mutaciją, L858R vienos vietos mutaciją, L858R / T790M dvigubą mutaciją ir laukinį tipą. L858R/790M mutacijose LA turi galimybę sąveikauti su Lys745 per katijono-II sąveiką. Vandenilio ryšiai susidaro tarp WT EGFR ir likohalkono Met793, Lvs745 ir Asp 855. Exon 19 delecija gali pakeisti kišenės, kurioje, kaip manoma, vyksta sąveika su likochalkonu, formą, suformuojant vandenilinius ryšius su Met793, Glu792 ir Glu790, . Duomenys, gauti atliekant LA analizę in silico, yra svarbus taškas nustatant naujus, selektyvius EGFR inhibitorius skirtingų tipų mutacijose [178].

Spustelėkite norėdami gauti daugiau informacijos. apie imunitetą
3.1.3. Likochalkonas B
PriešvėžinisLikohalkono B (LB, S1 ir S2 lentelės, 3 junginys) poveikis buvo įrodytas analizuojant skirtingas ląstelių linijas, įskaitant žmogaus ląsteles nuo šlapimo pūslės vėžio T24 ir EJ, burnos vėžio ląsteles HN22 ir HSC4, MCF-7, A375 (žmogaus melanomos ląstelių linija) ir A431 (plokščialąstelinė karcinoma). Tyrimai parodė, kad LB veikia vėžinių ląstelių augimą, slopina metastazių susidarymą, blokuoja ląstelių ciklą ir skatina apoptozę[161]. Kang ir kt. ištyrė molekulinį mechanizmą, kuriuo LB sukelia apoptozę žmogaus melanomos ir ląstelių plokščiųjų ląstelių karcinomose. Įrodyta, kad likochalkonas sukelia A375 ir A431 ląstelių apoptozę tiek vidiniais, tiek išoriniais būdais. Tiriant chalkono antiproliferacinį poveikį dažant tripano mėlynuoju, buvo pastebėta, kad LB sukelia reikšmingą ląstelių gyvybingumo sumažėjimą, šis sumažėjimas koreliuoja su koncentracija Pridėjus LB, buvo pastebėti reikšmingi ląstelių charakteristikų pokyčiai, įskaitant ląstelių susitraukimas, ląstelių membranų plyšimas ir suskaidytų branduolio ląstelių procento padidėjimas. Taip pat buvo pastebėtas padidėjęs priešG1-fazės ląstelių ir apoptozinių ląstelių procentas [38]. Kitas tyrimas parodė, kad LB reikšmingai blokuoja ląstelių ciklą G2/M fazėje HepG2-tipo vėžio ląstelių linijų atveju, o šlapimo pūslės ir krūties navikų ląstelių atveju junginys blokuoja S fazę [179]. Song ir kt. pabrėžė slopinamąjį LB poveikį JAK{19}}tipo stemplės karcinomos plokščiųjų ląstelių augimui. Prijungimo tyrimai buvo atlikti naudojant „Autodock Vina“ programinę įrangą, kuri buvo naudojama rišimo režimui numatyti. JAK2 receptoriaus, turinčio slopinimo potencialą, struktūrą galima rasti baltymų duomenų banke (PDB įrašas 2B7A, liekanos 840-1.132). IAK2 vaidina svarbų vaidmenį, nes yra tarpląstelinis citokinų signalizacijos tarpininkas ir yra JAK šeimos tirozino kinazės baltymas. ATP stipriai jungiasi su
magnio jonai tirozino kinazių katalizinėje srityje. Prijungimo parametre tiriamos erdvės dydis apima ATP surišimo vietą, kuriai būdingi likučiai 855-863 ir 822, kur ATP buvo apskaičiuotas naudojant įvairius potencialius JAK2 inhibitorius. Numatytose prognozėse LB ligandas buvo sukurtas naudojant Marvin Sketch programinę įrangą. Po prijungimo buvo surinkti trys geriausi galimi surišimo variantai, kurių giminingumas yra panašus. Prognozių išvados buvo palankios dėl LB sąveikos su ATP surišimo kišene JAK2 [180, 181].
3.1.4. Likochalkonas C
Likochalkonas C (LC, S1 ir S2 lentelės, 4 junginys) sumažina monocitų ląstelių linijų uždegiminį atsaką. Taip yra dėl iNOS ekspresijos sumažėjimo ir superoksido dismutazės, katalazės ir glutationo peroksidazės antioksidacinio tinklo aktyvumo atkūrimo. Kwak ir kt. atliko tyrimą, skirtą apibūdinti ryšį tarp ROS, c-Jun NH2 galinės kinazės (INK) ir p38mitogeno aktyvuotos baltymų kinazės (MAPK) ir nustatė LC poveikį stemplės vėžio ląstelių linijoms KYSE 30 ir KYSE450 skatinant apoptozę. Ankstesniais tyrimais buvo nustatytos IC50 vertės gydant LC (45 ug/ml) po 24 val., siekiant slopinti A549, MCF-7 ir T24 ląstelių linijų proliferaciją. Trims ląstelių linijoms buvo gautas 40, 47 ir 68 procentų slopinimas. Kwak ir kt. gautas nuo dozės ir laiko priklausomas stemplės vėžio ląstelių proliferacijos slopinimas in vitro. Iš penkių analizuotų ląstelių tipų KYSE30 ir KYSE450, turintys bendrą genetinę paramą, turėjo panašų atsaką į gydymą LC. Analizuojant nuo tvirtinimo vietos nepriklausomą augimą minkštame agare, rezultatai rodo, kad žymiai sumažėjo KYSE30 ir KYSE450 ląstelių gebėjimas formuoti kolonijas. Priklausomai nuo koncentracijos, chalkonai sukėlė apoptozę abiejose ląstelių linijose. Junginys taip pat sukėlė p24 ir p27 (neigiamų pereinamųjų reguliatorių ląstelių ciklo G1 ir S fazėse) reguliavimą ir reguliuojamą cikliną D. LC taip pat padidino ROS susidarymą KYSE30 ir KYSE450 ląstelėse. ROS aktyvuoja mitogeno aktyvuotos proteinkinazės (MAPK) kelią ir sukelialąstelių apoptozė. Be to, junginys padidino JNK, c-Jun ir p38 fosforilinimo lygį ir suaktyvino apoptotinius kelius [182]. Panašus į doko tyrimą, kurį atliko Song ir kt. LB[180], Oh ir kt. pabrėžė surišimo sąveiką tarp LC ir žmogaus JAK2 ląstelių. Prijungimo modeliavimas buvo atliktas naudojant „Autodock Vina“. Norint pradėti doko tyrimą, JAK2 receptoriaus struktūra, kuri buvo išskirta atliekant rentgeno eksperimentą, buvo gauta iš baltymų duomenų banko (PDB įrašas 2B7A). LC ligando struktūra buvo modeliuojama Marvin Sketch programine įranga ir optimizuota Chimera programine įranga. Katalizinė JAK2 vieta buvo koreliuojama su vyrių sritimi (likučiai 929-935), DFGloop (likučiai 994-996) ir Ploop (likučiai 858-865). Kilpos formos vyrių sritis yra būtina ATP atpažinimui ir sudaro vandenilinius ryšius su medžiagomis. DFGloop turi tris aminorūgštis (asparto rūgštį, fenilalaniną ir gliciną) ir yra susijusi su metalo, reikalingo kataliziniam fosforilinimui, surišimu. Ploop yra naudingas stabilizuojant ir formuojant sąveiką su ligandais. Kaip matyti, galimo surišimo prognozė buvo atlikta trijose funkcinėse vietose. Docking tyrimas parodė, kad LC sąveikauja su ATP surišimo vieta prie JAK2 ir nurodė, kad JAK2 yra tiesioginis jos taikinys. Chalkonas taip pat slopino JAK2 autofosforilinimą, prisijungdamas prie p-JAK2 ATP kišenės [183, 184].
3.1.5. Likochalkonas D
Licochalcone D (LD, S1 ir S2 lentelės, 5 junginys) yra aktyvus flavonoidas, išskirtas iš Glycyrrhiza inflata. Buvo atliktas tyrimas, siekiant įvertinti LD gebėjimą slopinti ląstelių proliferaciją dviem taikiniais plaučių vėžio ląstelėms (EGFR ir MET), naudojant jautrias ir gefitinibui atsparias žmogaus ląsteles. Norint suprasti tiesioginį chalkono prisijungimą prie EGFR ir MET, buvo naudojamos gefitinibui jautrios ląstelių linijos (HCC827) ir gefitinibui atsparios ląstelių linijos (HCC827GR). Vertinimų rezultatai rodo, kad flavonoidas jungiasi prie dviejų receptorių, slopindamas EGFR ir MET kinazių aktyvumą kaip konkurencinį ATP inhibitorių. EGFR komplekse chalkone yra dvi vandenilinės jungtys, kurias sudaro Met793 kaip pagrindinis Asp855 taškas ir šoninis kampas DFG kilpoje.4-Hidroksi-3-(3-metilo bet{{13} }enil)fenilo grupė ir 3,4-dihidroksi-2-metoksifenilo grupė yra fiksuotos toje pačioje plokštumoje ir užblokuotos tarp P kilpos ir Leu 844 hidrofobinių liekanų Leu718, Val726 ir Ala743. Met komplekse keto
chalkono grupė sudaro vandenilinę jungtį su Met1160. Tyr1159 kaip pagrindinis taškas ir le1084, Vall092, Ala1108 ir Lys1110 iš Ploop buvo panašiai uždengti dangteliu. Luisą taip pat stipriai palaiko šoninės hidrofobinės Met1160 pagrindinio taško grandinės ir apatinės ATP kišenės Leu1140, Met1211 ir Ala1221. EGFR surišimo padėtis labai panaši į MET surišimo padėtį, formuojant vandenilio ryšius ir hidrofobinę sąveiką. Chalkonas yra identiškai dviejų receptorių surišimo srityje. Komplekso stabilizavimą gali padidinti hidrofobinė sąveika. Numatyti rezultatai buvo lyginami su eksperimentiniais duomenimis, rodančiais, kad flavonoidas konkurenciškai slopina du receptorius [185].
3.1.6. Ksantohumolis
Prenilo chalkonai dėl savo struktūrinės įvairovės turi skirtingas biologines savybes, įskaitant priešuždegiminį, priešvėžinį ir antimutageninį poveikį [186]. Tyrimai parodė, kad natūralūs chalkonai su prenilo grupėmis gali trukdyti p53. Pavyzdžiui, A549 ląstelių gydymas prenilkalkono ksantohumoliu (XN, S1 ir S2 lentelės, 6 junginys) sukelia apoptotinę ląstelių mirtį ir blokuoja ląstelių ciklą G1 fazėje. Ši veikla atsiranda dėl padidėjusio p53 ir p21 reguliavimo iš ląstelių ciklo ir sumažėjusio ciklino D1 reguliavimo. Apoptozę sukelia kaspazės 3 aktyvacija [187].
XN((3'-(3,3-dimetilalilas)-2',A',4-trihidroksi-6'metoksichalkonas) yra labiausiai paplitęs prenilintas flavonoidas ({{7) }}.1-1 % sausos masės) moteriškų apynių žiedynų (Humulus lupulus)[180]. XN taip pat yra alaus sudedamoji dalis, pagrindinis prenilinto maisto šaltinis.flavonoidų, kur jo koncentracija didesnė nei 0,96 mg/l. Dėl unikalaus biologinio aktyvumo ir palankaus poveikio sveikatai prenilchalkonas pastaruoju metu buvo plačiai tiriamas [188]. Junginys pasižymi terapiniu saugumu ir įvairiu biologiniu aktyvumu, įskaitant priešvėžines, antidiabetines, priešuždegimines, antioksidacines ir antibakterines savybes. Pastaraisiais metais vis daugiau tyrimų parodė platų XN priešvėžinio aktyvumo spektrą sergant plaučių vėžiu, kepenų ląstelių karcinoma, krūties vėžiu, leukemija, prostatos vėžiu, kasos vėžiu, gaubtinės žarnos vėžiu, kasos vėžiu ir glioblastomos vėžiu. Vėžio ląstelių poveikis XN slopina jų dauginimąsi, migraciją ir invaziją bei moduliuoja autofagiją. Chalkonas taip pat gali sukelti apoptozę ir blokuoti ląstelių ciklą [189-193]. Be to, chalkonas sukelia apoptozę, priklausomai nuo kaspazės aktyvumo ir nepriklausomai nuo jo, ir slopina vėžio ląstelių invaziją bei angiogenezę [194]. Jo priešuždegiminės, antioksidacinės ir priešvėžinės savybės koreliuoja su cheminiu prevenciniu junginio poveikiu [195]. Prenilchalkonas taip pat metabolizuojamas į 8-prenilnaringeniną – stipriausią iki šiol žinomą fitoestrogeną [196].
Akt (taip pat vadinamas proteinkinaze B arba PKB) yra specifinė serino/treonino-proteino kinazė ir svarbus ląstelių signalizacijos kelių taškas. Akt aktyvumas yra pakitęs daugelio vėžio tipų atveju ir dalyvauja įvairiuose biologiniuose procesuose, įskaitant ląstelių proliferaciją, apoptozę, transkripciją, migraciją ir invaziją. Siekiant patvirtinti XN gebėjimą prisijungti prie Akt, buvo atliktas in silico prijungimo tyrimas naudojant Schrodinger Suite 2015 programinę įrangą. Vandens molekulės buvo pašalintos, o vandenilio atomų pH buvo 7. Sujungimo tyrimui buvo sukurta ATP surišimo vieta. XN buvo paruoštas prijungti be parametrų naudojant LigPrep programą. Vėliau XN prijungimo su Aktl ir Akt2 tyrimus lydėjo nebuvę parametrai, naudojant papildomo tikslumo metodą naudojant „Glide“ programą, siekiant gauti geriausius struktūrinius vaizdus. Dokų tyrimo rezultatai rodo, kad XN sudaro vandenilinius ryšius su Akt1 Ala230, Glu228, Glu234 ir Lys158 bei Akt2 su Glu236, Thr213 ir Lvs181. Buvo nustatyti ksenografiniai (PDX) modeliai, skirti pagrindiniams tyrimams pritaikyti klinikiniais tikslais. Manoma, kad PDX modeliai išsaugo donorų pacientų biologines ir genetines savybes, o tai yra pagrindinis pranašumas, palyginti su ląstelių linijos modeliais. PDX modeliai buvo naudojami analizuojant biomarkerius ir prognozuojant atsaką į XN terapiją klinikinių tyrimų metu. Chemoprevencinis prenilchalkono poveikis buvo lyginamas remiantis Akt lygiais. Rezultatai rodo, kad naviko modeliai, išreiškiantys aukštą Akt lygį, žymiai sumažina naviko tūrį ir svorį gydant XN [197]. Guo ir kt. tyrė in vitro ir in vivo XN poveikį sergant skrandžio vėžiu, parodydamas, kad prenilchalkonas sukelia apoptozę aktyvindamas kaspazes, reguliuodamas Bcl-2 ir paveikdamas PI3K/Akt/mTOR kinazę. XN slopina skrandžio vėžio ląstelių gyvybingumą priklausomai nuo koncentracijos. Ląstelių linijose flavonoidas daro geriausią poveikį SGC-7901 ląstelių gyvybingumui ir nedaro įtakos šiam parametrui GES-1 ląstelėms esant 6, 8 ir 10 ug/mL chalkono. Iš srauto citometrinės analizės buvo pastebėta, kad prenilchalonas žymiai padidina apoptozinių ląstelių skaičių sergant skrandžio vėžiu. XN poveikis pro- ir anti-apoptotiniams baltymams buvo pabrėžtas Western blot analize. Bcl-2 ir Bcl-XL baltymų kiekis sumažėjo po flavonoidų vartojimo, šis sumažėjimas koreliuoja su vartojama koncentracija. XN taip pat padidino Bax ir Bid baltymų kiekį, o geriausias aktyvumas buvo stebimas esant 10 uM/mL chalkono. Be to, suskaidyto kaspazės 3 ir suskaidyto PARP baltymo lygis žymiai padidėjo esant chalkonui. Dėl šių priežasčių galima teigti, kad flavonoidai palankiai ir reikšmingai veikia pro- ir antiapoptotinių baltymų kiekį. Iš viso 10 uM/mL XN sukelia reikšmingą SGC-7901 ląstelių apoptozę. Iš viso 8 ir 6 uM/mL chalkono sukelia atitinkamai 34±3 procentų ląstelių ir 23±2 procentų ląstelių apoptozę. Be to, flavonoidas reikšmingai modifikuoja PI3K, Akt ir mTOR fosforilinimą, padidina p-PTEM lygį ir sumažina p-Akt (Thr308), p-Akt (Ser473) ir m-Tor (Ser2448) lygį. Gauti duomenys rodo, kad prenilchalkonas reikšmingos įtakos Akt, PTEN, GSK-3 ir mTOR lygiams nedaro. SGC7901 ksenografinių pelių nustatymas parodė, kad gydymas XN sumažino naviko tūrį santykinai priklausomai nuo koncentracijos. Siekiant patvirtinti PI3K / Akt signalizacijos slopinimą in vivo, buvo įvertinta fosforilinta Akt ir mTOR ekspresija ant ksenografinių navikų. Patologinis hematoksilino ir eozino sekcijų tyrimas atskleidė reikšmingus morfologinius pakitimus. Tačiau XN sumažina nuo koncentracijos priklausomą fosforilintą Akt ir mTOR lygį. Gydymas prenilchalkonu žymiai sumažino ląstelių proliferaciją ir padidino naviko ląstelių apoptozę, palyginti su kontrolinėmis ląstelėmis [198].
XN, kurio koncentracija didesnė nei 10 umol/L, slopina kasos vėžio ląstelių dauginimąsi in vitro. Esant mažesnėms nei 5 umol/L koncentracijoms, chalkonas slopina nuo NF-kB priklausomą angiogeninį aktyvumą kasos vėžio ląstelėse. Esant tokiai koncentracijai, WST-1 metodu kasos ląstelėse citotoksiškumo nepastebėta. Tačiau tyrimo išvada buvo tokia, kad XN veikia kasos vėžio sukeltą angiogenezę, sumažindamas VEGF ir IL-8 (interleukino) gamybą, kuri yra specifinė ir tarpininkauja NF-kB inaktyvacija [194]. įvertinti XN priešvėžinį aktyvumą, HepG2 ląstelių linijoms buvo atlikta MTT analizė, siekiant nustatyti ląstelių proliferaciją. Prenilchalkonas sumažino ląstelių proliferaciją priklausomai nuo koncentracijos ir laiko. Zhao ir kt. pastebėjo, kad ląstelių linijų veikimas 200 μM XN vieną dieną yra mažiau efektyvus, palyginti su jų apdorojimu 100-200 μM chalkono 2-3 dienų. Esant 50 uM chalkono, po 3 dienų buvo pastebėtas reikšmingas HepG2 ląstelių proliferacijos slopinimas. Tame pačiame tyrime buvo įrodyta, kad prenilchalkonas žymiai padidina kaspazės 3 aktyvumą. Be to, Western blot analize buvo įrodyta, kad 100-150 uM XN reikšmingai slopino NF-kBbaltymo ekspresiją ląstelių linijose. Šia analize taip pat buvo pastebėta, kad prenilchalkonas gali padidinti p53 baltymo ekspresiją, o 20 uM XN lėmė Bax signalizacijos sustiprėjimą, o tai koreliuoja su laiku [199]. XN saugumo profilio tyrimai rodo, kad 1000 mg/kg junginio nekeičia pelių gyvybiškai svarbių organų funkcionavimo ir homeostazės. Prenilchalkonas gali padidinti IL-2 gamybą T ląstelėse, o tai rodo jo gebėjimą skatinti The-medijuojamą imuninį atsaką. XN taip pat slopina -12. kuris netiesiogiai sukelia ląstelių diferenciaciją imuninėje sistemoje, aktyvuodamas transkripcijos molekules. Citotoksiniai Tlimfocitai yra ląstelių efektoriaus tipas, labai svarbus ląstelių imunitetui ir vaidina svarbų vaidmenį priešnavikinės imunologijos procese. CD8 ir T citotoksiniai limfocitai egzistuoja kaip CTL-P, neaktyvus ląstelių pirmtakas in vivo. Šį pirmtaką aktyvuoja antigenas, esant Th1 citokinams, o po to išsivysto į subrendusius citotoksinius T limfocitus. Buvo parodytas reikšmingas CD8 plus / CD25 plus padidėjimas, o po to Th2 perėjimas į Th1 naviko mikroklimate. CD8 plius /CD25* T ląstelių santykis labai padidėja, kai 4T1 ląstelių linijose CoCl2 aktyvuoja citotoksinius T limfocitus. Th1 ir Th2 ląstelių funkcija priklauso nuo įvairių citokinų sekrecijos. Norėdami ištirti XN poveikį Th1 ir Th2 citokinams, Zhang ir kt. nustatė Th1l ir Th{44}}susijusių citokinų koncentraciją serume naudojant ELISA rinkinius. Nustatyta, kad prenilo darinys žymiai padidina Th1 citokinų ekspresiją (įskaitant IL-2 ir IFN-y) ir sumažina Th2 citokinų kiekį (įskaitant IL-4 ir IL-10). Ši išvada paaiškinama tuo, kad Th1 ir Th2 yra abipusiai inhibitoriai. Be to, Th1 / Th2 santykis buvo nustatytas srauto citometrija, parodydamas, kad XN jį žymiai padidina. Panašūs tyrimai pranešė apie šią išvadą dėl įvairių navikų. Pacientams, sergantiems pažengusiomis kaklo ir galvos plokščialąstelinėmis karcinomomis, Th1 citokinų kiekis yra mažas, palyginti su pacientais, kurie yra ne tokie sunkūs ir kurių Th2 citokinų kiekis yra didelis. Kombinuotas gydymas sukelia Th2 perėjimą į Th1 citokinus naviko aplinkoje. Tyrimų rezultatai rodo Th1/Th2 citokinų santykio sutrikimą, šis pokytis stebimas kelių tipų navikams, dažniausiai galutiniuose vėžio etapuose. Siekiant patvirtinti galimą XN mechanizmą dėl Thl/'Th2 citokinų santykio, buvo nustatyta pagrindinių faktorių raiška Th1 ir Th2 diferenciacijos kelyje. Fiziologiškai Th0 ląstelės yra proporcingai diferencijuojamos į Thl ir Th2 ląsteles. Be to, 4 ir 6 transkripcijos molekulių aktyvinimas atlieka gyvybiškai svarbų vaidmenį diferencijuojant Th0 į Th1 ir Th2 ląsteles. T-bet ir GATA{72}} taip pat atlieka du pagrindinius vaidmenis. CpG-ODN (citozino-fosforotioato-guaninas, turintis oligodeoksinukleotidą), stiprus Th1 adjuvantas, sumažina GATA{77}} ekspresiją ir 6-osios transkripcijos molekulės aktyvavimą, aktyvuodamas T-bet ir transkripcijos 1 ir 4 molekules plaučių vėžio modeliuose. XN padidina T-bet išraišką ir sumažina GATA{83}} išraišką. 4 transkripcijos molekulės aktyvacija padidėja esant XN, tačiau tai neturi įtakos transkripcijos molekulės 6 aktyvacijai. Dėl šios priežasties galima teigti, kad transkripcijos molekulės 4 aktyvacija atlieka teigiamą vaidmenį reguliuojant Th1/Th2 citokiną. santykis XN [200].
Įpjovos signalizacijos kelias vaidina svarbų vaidmenį sergant krūties vėžiu, kuris yra terapinis jo gydymo tikslas. Jis yra susijęs su krūties vėžio atsiradimu ir progresavimu, o nenormalus šio kelio aktyvumas yra susijęs su šia patologija. Notch signalizacijos kelio slopinimas gama sekretazės inhibitoriais ir anti-delta tipo monokloniniais antikūnais 4 yra palankus ūminės limfoblastinės leukemijos ir solidinių navikų gydymui. Šių agentų mechanizmai apima ląstelių ciklo blokavimą arba apoptozę ir angiogenezės sutrikimą. Sun ir kt. ištyrė terapinį XN potencialą krūties vėžio ląstelių linijose, pabrėždamas jo gebėjimą slopinti ląstelių proliferaciją, blokuoti ląstelių ciklą ir sukelti apoptozę in vitro. Taip pat buvo nustatytas naviko augimo sumažėjimas in vivo. Be to, buvo ištirta prenilchalkono galimybė slopinti žmogaus krūties vėžio ląstelių augimą Notch signalizacijos keliu. Norint nustatyti, ar XN nukreiptas į Notch signalizacijos kelią, buvo naudojamas funkcionalizuotas Notch 1 metodas, naudojant gama sekretazės inhibitorių (DAPT) kaip kontrolę. Tyrimo tikslas buvo įvertinti galimybę, kad prenilchalkonas sumažina Notch1 prisijungimo prie CBF1 transgeno aktyvumą. Nustatyta, kad XN slopina proliferaciją ir sukelia apoptozę, slopindamas Notch 1 kelią. Be to, naudojant MTT metodą ir šviesos mikroskopiją, buvo įrodyta, kad prenilchalkonas slopina ląstelių dauginimąsi krūties vėžio ląstelių linijose. Ankstesni tyrimai parodė, kad Notch kelio inhibitoriai taip pat yra EGFR ekspresijos inhibitoriai, dar vienas kaltinantis krūties vėžio elementas. Be to, XN veikia baltymus, susijusius su naviko metastazėmis, ir slopina ląstelių migraciją, padidindamas šių baltymų ekspresiją. Tyrimas atskleidė ląstelių ciklo blokavimą G0/G1 fazėje ir apoptozės indukciją MCF-7 ir MDA-MB-231 ląstelėms XN [201].

3.1.7.Panduretinas A
Priešvėžinisbuvo ištirtas pandurato A (PA, S1 ir S2 lentelės, 7 junginys), cikloheksanilchalkono, išskirto iš Boesenbergia pandurate, aktyvumas. Šiame augale yra prenilo chalkonų ir kitų flavonoidų, kurie yra pagrindinės bioaktyvios molekulės, kurios literatūroje aprašytos turinčios pirmenybę citotoksinių savybių žmogaus kasos ląstelių linijai PANC{3}}. [202,203] PA veikia sergant melanoma, gaubtinės žarnos adenokarcinoma ir prostatos vėžiu. Proteominės analizės rodo, kad PA turi citotoksinį poveikį melanomos ląstelėms, kuris priklauso nuo mitochondrijų oksidacinio fosforilinimo proceso denatūracijos, sekrecijos kelio aktyvumui ir apoptozei, kurią sukelia oksidaciniai procesai. Šiuo atžvilgiu buvo įrodyta, kad oksidacinis stresas gali atsirasti dėl autofagijos, kaip antrinės reakcijos į padidėjusį ROS, stimuliavimo [204]. Literatūroje nurodoma, kad 9 ug/mL PA koncentracija visiškai slopina MCF-7 ląstelių ir HT-29 ląstelių (žmogaus gaubtinės žarnos vėžio ląstelių linijos) augimą[205]. Kalkonas turi priešvėžinių savybių įvairių tipų ląstelėms, įskaitant melanomą, gaubtinės žarnos adenokarcinomą ir prostatos vėžį [204]. Liu ir kt. pabrėžė citotoksinį chalkono poveikį MCF-7, T47D (žmogaus krūties vėžys) ir MCF-10A (ne naviko krūties ląstelės) ląstelių linijoms. PA IC50 reikšmės MCF-7 ląstelėse buvo 15 uM 24 val. ir 11,5 μM 48 val. T47D ląstelių atveju IC50 buvo 17,5 μM 24 val. ir 14,5 μM 48 val. PA neturi įtakos MCF-10A ląstelių dauginimuisi. Norint nustatyti mechanizmus, kuriais chalkonas sukelia ląstelių ciklo blokadą MCF-7 ląstelėse GO/G1 fazėje, buvo naudojama Western blot analizė, kurios tikslas buvo įvertinti reguliuojančių baltymų moduliavimą ląstelių cikle. Rezultatai rodo, kad gydymas PA sukelia ciklino D1 ir CDK4 ekspresijos sumažėjimą ir padidina p21Cip1 ir p27 ekspresiją, taip paaiškindamas blokadą G0 / Gl fazėje. Iš Kaempferia pandurate izoliuotas PA sukelia ląstelių ciklo blokadą nuo androgenų nepriklausomose PC-3 (prostatos adenokarcinomos) ląstelėse ir žmogaus DU145 (žmogaus prostatos vėžio ląstelių linija) ląstelėse. Internukleosominė DNR fragmentacija yra apoptozės žymuo. Kadangi mažos molekulinės masės DNR fragmentai ekstrahuojami dažant ląsteles vandeniniuose tirpaluose, apoptotines ląsteles galima identifikuoti pagal DNR turinio dažnio histogramas ląstelių su frakcionuotu DNR kiekiu. Buvo analizuojama sub-G1 fazės MCF{47}} ląstelių populiacija. G1 fazės kiekis ląstelėse buvo 1,17 ± 0,11, o ląstelėse, apdorotose PA (10, 15 ir 20 μM), jis buvo atitinkamai 1,84 ± 0,18, 2,62 ± 0,21 ir 4,52 ± 0,28. Gydymo chalkonu padidėjimą lėmė DNR suskaidymas MCF{68}} linijose, o tai patvirtina sub-G1 fazės ląstelių populiacija [206].
Tarp pagrindinių vėžio ląstelių invazijos ir metastazių baltymų indukcija yra matricos metaloproteinazės. Jie skaido tarpląstelinės matricos komponentus ir palengvina ląstelių invaziją bei migraciją. Be to, per didelė metaloproteinazių ekspresija gali sukelti epitelio-mezenchiminį perėjimą. PA slopina metaloproteinazės 2 sekreciją ir aktyvavimą, slopindamas endotelio ląstelių migraciją, invaziją ir morfogenezę žmogaus bambos venų endotelio ląstelėse (HUVEC). Be to, subtoksinių chalkonų dozių pakanka, kad sumažėtų metaloproteinazės 2 kiekis plaučių vėžio ląstelėse [207].
3.1.8. Kardamoninas
Kardamonas (CD, S1 ir S2 lentelės, 8 junginys), chalkonas iš Campomanesia adamantium (Myrtaceae), padidina DNR fragmentaciją ir sumažina NF-kB aktyvumą PC-3 ląstelėse. Šie rezultatai rodo terapinį chalkono potencialą gydant prostatos vėžį [20]. CD laikomas vienu iš aktyviausių priešnavikinių junginių, kuriame dalyvauja Epstein-Barr viruso aktyvacija [208]. CD priešvėžinis poveikis yra susijęs su apoptozės indukcija, ląstelių proliferacijos ir migracijos slopinimu bei įtaka ląstelių ciklui. Chalkonas taip pat gali sumažinti vėžio ląstelių atsparumą terapijai. Kartu su 5-fluorouracilu arba cis-platina padidinamas priešnavikinis aktyvumas. Pavyzdžiui, CD turi galimybę reikšmingai slopinti gaubtinės žarnos vėžio ląstelių atsparumą chemoterapijai, sukelia apoptozę, aktyvina 3 ir 9 kaspazes, palengvina Bax baltymo ekspresiją, reikšmingai slopina c-myc ir turi specifinių 50 ir NF-kB [209]. ]. Hou ir kt. ištyrė CD terapinį potencialą ir molekulinius mechanizmus 5-fluorouracilui atspariose skrandžio vėžio ląstelėse. BGC-823/5-fluorouracilo jautrumas 5-fluorouracilui buvo patvirtintas padidinus apoptozę ir blokuojant ląstelių ciklą esant CD. Kalkonas padidina vėžio ląstelių jautrumą 5-fluorouracilui, nes slopina Wnt/-catenin signalizacijos kelią (kuris vaidina svarbų vaidmenį navikogenezėje), o aktyvuotos Wnt/-katenino genų mutacijos yra susijusios su atsparumu priešvėžiniam gydymui. . Jis slopina P-glikoproteino, -katenino ir TCF-4 ekspresiją. Be to, CD specifiškai blokuoja -catenin/TCF-4 komplekso susidarymą, taip sukeldamas aberrantišką Wnt/-catenin signalizaciją [210]. Miegamasis ir kt. ištyrė antiproliferacinį ir apoptotinį CD poveikį HepG2 ląstelėms. Slopinamasis poveikis
chalkonas HepG2 ląstelių proliferacijoje buvo reikšmingas po 72 val., citotoksiškumas buvo panašus į 5-fluorouracilo. Kitų chemoterapinių preparatų, naudojamų kaip standartas (pvz., sorafenibo), vertės buvo daug mažesnės. Be to, junginio citotoksinis poveikis yra selektyvus naviko ląstelėms ir nedaro neigiamos įtakos normalioms ląstelėms, o tai yra CD pranašumas, palyginti su 5-fluorouracilu. CD kaupimasis ląstelių ciklo G1 fazėje buvo pastebėtas po 72 valandų ir rodo HepG2 ląstelių augimo slopinimą, užkertant kelią ląstelių dalijimuisi [211].
Lyginamieji CD ir 5-fluorouracilo bei jo sąveikos su BaxBH3 tyrimai rodo, kad 5-fluorouracilo surišimo energija yra didesnė nei CD. Chalkonas sudaro tris vandenilio ryšius (Phe30, Val50 ir Gln52). CD ir Bcl sąveika pasiekiama trimis vandenilio jungtimis (Asp15, Gln18 ir Ser28), o 5-fluorouracilo atveju – keturiomis jungtimis. Be to, šios sąveikos atveju CD surišimo energija yra mažesnė nei 5-fluorouracilo. Tai gali būti siejama su aromatinėmis likučiais chalkono struktūroje, dalyvaujančiomis II jungtimis, kurios turi savybę stabilizuoti aktyviąją kišenę ir sumažinti surišimo energiją. In silico tyrimų rezultatai rodo, kad 5-fluoruracilo jungimosi energija yra didesnė nei kaspazės 3, palyginti su CD. CD rodo dvi vandenilio jungtis sąveikaujant su kaspaze 3 (Cys163 ir Arg64). Chalkonas taip pat turi II-II ryšius su TYR204. 5-Fluorouracilo laisvoji jungimosi energija yra pranašesnė už CD, o tai paaiškinama aktyviosios kišenės stabilizavimu dviem aromatinėmis liekanomis chalkono struktūroje [212].
3.1.9. Lonchokarpinas
Lonchokarpinas (S1 ir S2 lentelės, 9 junginys) yra natūralus chalkonas, išgautas iš Lonchiocarpus sericeus. Šio chalkono citotoksinis poveikis aprašytas neuroblastomos ir leukemijos ląstelių linijoms. Yra žinoma, kad 24 val. po gydymo 50 uM lonchokarpinu SK-N-SH neuroblastomos linijose vyksta AMPK fosforilinimo indukcija, kuri padidina gliukozės absorbciją ir slopina baltymų sintezę. Chalkonas taip pat turi savybę sumažinti ląstelių gyvybingumą. Kolorektalinio vėžio ląstelių linijose HCT116, SW480 ir DLD lonchokarpinas sumažina ląstelių gyvybingumą 20 μM. Tyrimai rodo, kad lonchokarpinas gali slopinti H292 plaučių vėžio ląsteles in vitro dėl kaspazės{11}}sukeliamos ląstelių mirties, kuri vyksta prieš apoptozę. Be to, buvo pastebėta, kad lonchokarpinas slopina Wnt/-catenin signalizaciją in vivo Xenopus laevis embrioniniuose modeliuose. Chalkono injekcija į kartu sušvirkštą Wnt8-specifinio receptoriaus modelį (SO1234) lėmė 82 proc. slopinimą Wnt/-katenino signalizacijos receptorių geno aktyvacijai [213].
Chen ir kt. atliktame tyrime 3D-QSAR analizės rezultatai rodo hidrofobinį C-4, C-5, C-11, C-1/ ir C. -2 sąveika lonchokarpine. Ši sąveika padidina šio junginio citotoksinį pajėgumą, o jo indėlis į modelį sudaro 23 procentus. Lonchokarpino prijungimo tyrimai davė tuos pačius rezultatus kaip ir hidrofobinis 3D-QSAR modelis, kai hidrofobinis paviršius yra C-4, C-5, C-11, C-1' ir lonkokarpino C-2sritys, sąveikaujančios su Bcl-2 kompleksu. Hidrofobinė Bcl-2 baltymo kilpa sudaro kompleksą su BaxBH3 peptidu, kurį gali nutraukti sintetiniai navitoklakso arba lonchokarpino junginiai. Tai rodo, kad Bcl-2 šeimos narių hidrofobinė kilpa yra lonkokarpino sukeltos apoptozės H292 ląstelėse taikinys, taigi ir kaspazės 3 aktyvacija [214].
Kiti natūralūs chalkonai, turintys priešvėžinių savybių, yra buteinas (S1 ir S2 lentelės, 10 junginys), izoliquiritigeninas (S1 ir S2 lentelės, 11 junginys), flavokavinas (S1 ir S2 lentelės, 12 junginys) ir izobavachalkonas (S1 ir S2 lentelės, 13 junginys). [155].

Spustelėkite nuorodą, kad gautumėte 3 dalį:https://www.xjcistanche.com/news/part3-anticancer-activity-of-natural-and-synt-54978140.html
